Ácido tefílico
El ácido tefílico es un compuesto químico cuya fórmula es HOTeF5. Este ácido fuerte está muy relacionado con el ácido ortotelúrico, Te(OH)6. El ácido tefílico tiene una geometría octaédrica algo deformada.
| Ácido tefílico | ||
|---|---|---|
 | ||
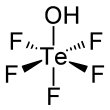 Fórmula estructural completa | ||
| Nombre IUPAC | ||
| Ácido pentafluoroorotelúrico | ||
| General | ||
| Otros nombres | Ácido tefílico | |
| Fórmula estructural |
 | |
| Fórmula molecular | HOTeF5 | |
| Identificadores | ||
| Número CAS | 57458-27-2[1] | |
| ChemSpider | 10331773 | |
| PubChem | 15243876 | |
| Propiedades físicas | ||
| Apariencia | sólido incoloro | |
| Masa molar | 239,6025 g/mol | |
| Punto de fusión | 39,1 °C (312 K) | |
| Punto de ebullición | 59,7 °C (333 K) | |
| Peligrosidad | ||
| SGA |
 | |
| Frases H | H314. | |
| Frases P | P260, P264, P280, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P321, P363, P405, P501. | |
| Riesgos | ||
| Riesgos principales | corrosivo, tóxico. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Preparación
El ácido tefílico se descubrió accidentalmente por Engelbrecht y Sladky. En su síntesis no se obtuvo el fluoruro de telurilo TeO2F2 previsto, sino una mezcla de compuestos telúricos volátiles que contenían el HOTeF5:[2]
BaTeO4 + 10HOSO2F → HOTeF5 (25%)
El ácido tefílico también puede obtenerse a partir del ácido fluorosulfónico y el telurato de bario:[3]
5HOSO
2F + BaO
2Te(OH)
4 → HOTeF
5 + 4H
2SO
4 + BaSO
4
Es también el primer producto de hidrólisis del hexafluoruro de teluro:
TeF
6 + H
2O → HOTeF
5 + HF
Teflatos

La base conjugada del ácido tefílico se denomina anión teflato, F5TeO- (no confundir con triflato). Se conocen muchos teflatos, un ejemplo es el B(OTeF5)3, que puede pirolizarse para formar el anhídrido ácido O(TeF5)2.[3]
2B(OTeF
5)
3 → 2 B(OTeF
5)
2F + O(TeF
5)
2
El anión teflato es conocido por su resistencia a la oxidación. Esta propiedad ha permitido la preparación de varias sustancias muy inusuales, como los hexateflatos M(OTeF
5)−
6 (en el que M = As, Sb, Bi). El xenón forma el catión Xe(OTeF5)+.[4]
Referencias
- Número CAS
- Engelbrecht, A.; Sladky, F. (7 de mayo de 1964). «Pentafluoro-orthotellursäure, HOTeF5». Angewandte Chemie (en alemán) 76 (9): 379-380. doi:10.1002/ange.19640760912. Consultado el 11 de abril de 2023.
- Wiberg, Egon; Holleman, A. F.; Wiberg, Nils (2001). Inorganic Chemistry (en inglés). Academic Press. ISBN 978-0-12-352651-9. Consultado el 11 de abril de 2023.
- Mercier, Helene P. A.; Sanders, Jeremy C. P.; Schrobilgen, Gary J. (1994-04). «Hexakis(pentafluorooxotellurato)pnictate(V) Anions, M(OTeF5)6- (M = As, Sb, Bi): A Series of Very Weakly Coordinating Anions». Journal of the American Chemical Society (en inglés) 116 (7): 2921-2937. ISSN 0002-7863. doi:10.1021/ja00086a025. Consultado el 11 de abril de 2023.
Enlaces externos
- Esta obra contiene una traducción total derivada de «Teflic acid» de Wikipedia en inglés, concretamente de esta versión del 9 de abril de 2023, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.