Enfermedad mitocondrial
Además de la información genética contenida en el núcleo celular (en los cromosomas), las células cuentan también con una pequeña proporción de ADN extranuclear que se encuentra localizado en las mitocondrias.
| Enfermedad mitocondrial | ||
|---|---|---|
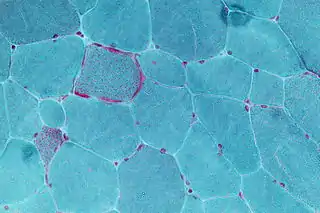 Micrografía mostrando fibras rojas rotas, un signo de algunas enfermedades mitocondriales. | ||
| Especialidad | endocrinología | |
El genoma mitocondrial acumula más mutaciones que el genoma nuclear, esto puede ser debido a que tiene una mayor cantidad de radicales libres.
Las enfermedades mitocondriales son desórdenes resultantes de la deficiencia de una o más proteínas localizadas en las mitocondrias e involucradas en el metabolismo.[1] Hay descritas unas 150 mutaciones que acaban en enfermedades de distinto tipo. Las enfermedades mitocondriales pueden estar causadas por mutaciones en el ADN mitocondrial, o bien por mutaciones en genes nucleares que codifican para proteínas implicadas en el correcto funcionamiento de la mitocondria. Las enfermedades mitocondriales causan el mayor daño a las células del cerebro, corazón, hígado, músculos esqueléticos, riñones y del sistema endocrino y respiratorio, ya que los tejidos con mayor dependencia del metabolismo mitocondrial (es decir, aquellos que requieren un mayor aporte energético) son los más sensibles a las mutaciones mitocondriales.
La gravedad y el espectro de estas enfermedades parecen desproporcionados respecto a la contribución del ADN mitocondrial al genoma humano.
La mayoría de las enfermedades mitocondriales se dan donde hay una alta necesidad de obtener energía: tejidos neuromusculares, cardíacos, ópticos y auditivos. Dependiendo de cuáles sean las células afectadas, los síntomas pueden incluir: pérdida del control motor (pérdida de equilibrio, epilepsia, temblores, etc.), debilidad muscular y dolor, desórdenes gastrointestinales y dificultades para tragar, retardo en el crecimiento, enfermedad cardíaca, enfermedad hepática, diabetes, complicaciones respiratorias, crisis, problemas visuales (ceguera, catarátas, entre otros) y auditivos (sordera-a menudo afectando a ambos oídos-), acidosis láctica, retrasos en el desarrollo, susceptibilidad a las infecciones, problemas de fertilidad (sobre todo en el sexo femenino), problemas hormonales y dificultad al tragar y al absorber nutrientes (conllevando a una pérdida de peso), entre otras muchas patologías observadas.[1]
Causas
Como se mencionó, el factor común entre las enfermedades, es la pérdida de la capacidad metabólica por parte de las mitocondrias de los tejidos o zonas afectadas. El metabolismo requiere de cientos de reacciones químicas, y cuando uno o más de los intermediarios en estas reacciones no funciona de forma adecuada, hay una crisis energética. Como resultado, los productos del metabolismo incompleto, pueden acumularse como "veneno" en el cuerpo.
Este "veneno" puede interrumpir otras reacciones químicas importantes para la supervivencia celular, empeorando aún más la crisis energética. Además, estas moléculas pueden actuar como radicales libres (sustancias reactivas que por sí solas forman compuestos dañinos con otras moléculas) causando un daño a las mitocondrias a través del tiempo.
La gravedad y el espectro de las enfermedades mitocondriales parece en un primer vistazo desproporcionado respecto a la cantidad tan pequeña de ADN mitocondrial en el genoma humano si lo comparamos con la cantidad de ADN presente en el núcleo celular (alrededor del 0'1% corresponde al ADN mitocondrial -unos 37 genes-, frente al 99'9% restante -unos 24000 genes nucleares-). Sin embargo, este hecho no se debe al capricho de la naturaleza, sino que existen unas causas determinadas y definidas que dan lugar a este hecho:
- Todo el ADN mitocondrial es codificante, mientras que en el nuclear existen múltiples intrones no codificantes de genes.
- Existen menos mecanismos de reparación genética de posibles mutaciones o errores de lectura que en el núcleo.
- La mitocondria es un orgánulo donde existe una gran presencia de radicales libres.
- Estos dos últimos puntos hacen que la tasa de mutación llegue a ser diez veces mayor que en el núcleo, lo que explica la gran cantidad de enfermedades genéticas de origen mitocondrial.
Para muchos pacientes, la enfermedad mitocondrial es una condición heredada. Un porcentaje incierto de pacientes adquieren los síntomas debido a otros factores, incluyendo toxinas mitocondriales. El tipo de herencia de las enfermedades mitocondriales es por herencia materna.
Herencia materna
Las enfermedades mitocondriales con herencia materna (también conocida como herencia mitocondrial o citoplasmática) son probablemente tan comunes como las enfermedades mitocondriales autosomales recesivas.[1] Algunos ejemplos son: el síndrome MELAS, el síndrome MERRF, el síndrome NARP y la neuropatía óptica hereditaria de Leber.
En la herencia mitocondrial se produce el denominado efecto de cuello de botella: el ovocito destruye todas las mitocondrias paternas y la gran mayoría de las maternas; las mitocondrias maternas no destruidas se multiplican. Así, todo el ADN mitocondrial (mtDNA) es heredado de la madre. En el caso de existir una mutación en el ADN mitocondrial, las mujeres portadoras de dicha mutación siempre la transmiten a su descendencia, mientras que los varones nunca lo harán. En consecuencia, un hijo comparte la misma secuencia de mtDNA con sus hermanos o hermanas, y madre, pero no con su padre.
Cada una de las células contiene un número variable de copias de mtDNA, a menudo miles. La mayoría de los individuos "normales" tiene células homoplásmicas, es decir, células que contienen mtDNA normal solamente. Los individuos con enfermedad mitocondrial de herencia materna, y sus parientes de parte materna, usualmente tienen células heteroplásmicas, es decir, que parte del mtDNA es normal y parte contiene la mutación. Las proporciones de heteroplasmia difieren, a menudo de forma drástica, entre los miembros familiares de parte materna. Existe un umbral de la proporción de mtDNA mutante a mtDNA normal, que varía en los diferentes tejidos y en las diferentes mutaciones, luego del cual la célula se convierte en deficiente.
Como consecuencia, los síntomas, gravedad, edad de inicio, etc., de una enfermedad mitocondrial pueden variar ampliamente dentro de una familia. De modo que, a pesar de que una madre con una mutación en el mtDNA pasará la mutación a toda su descendencia, no todos los hijos mostrarán los síntomas necesariamente. Y en el caso de que un hijo muestre los síntomas, la enfermedad puede ser muy diferente respecto de sus hermanos dependiendo del porcentaje de mtDNA mutante en cada región del cuerpo. Esto constituye una explicación al hecho de que las enfermedades mitocondriales con herencia materna presenten un cuadro o espectro clínico tan amplio.
A diferencia de las enfermedades mitocondriales autosomales recesivas, la edad de inicio de las enfermedades mitocondriales de herencia materna se da usualmente a mayor edad, incluyendo desde niños de 1 a 2 años hasta adultos.[1]
Pese a que esta herencia es solo materna en la inmensa mayoría de casos, se han encontrado excepciones.[2]
Heteroplasmia y homoplasmia
El número de mitocondrias por célula varía según el tejido de que se trate, pudiendo llegar a existir más de 500 mitocondrias por célula. Además, cada una de ellas puede tener entre 2 y 10 copias de ADN mitocondrial. Este hecho puede hacer que dentro de una misma célula existan distintas poblaciones de mitocondrias.
- Homoplasmático: Individuo que posee todas las mitocondrias con el mismo genoma.
- Heteroplasmático: Individuo que presenta una mezcla de poblaciones distintas de mitocondrias. A grandes rasgos existen dos posibilidades, y son que la persona presente en ciertas células de su cuerpo una variante del ADN mitocondrial, y en otras células otra distinta (de forma similar a lo observado en un mosaicismo), o que en un misma célula presente una población de mitocondrias con una variante del genoma, y otra población con la otra. Ciertamente, todas las personas presentamos al menos un cierto grado de microheteroplasmia, y es que no todas las mitocondrias de nuestro cuerpo van a tener exactamente el mismo genoma, siempre pueden darse mutaciones.
Siempre hay mutaciones en el genoma mitocondrial de un individuo, por lo que no hay verdadero poblaciones de mitocondrias homoplásmicas. Todas presentan algún grado de microheteroplasmia. Como se ha dicho antes, los tejidos con mayor dependencia del metabolismo mitocondrial son más sensibles a las mutaciones del DNA mitocondrial, pero hay que tener en cuenta la microheteroplasmia.
La heteroplasmia puede acabar en sustituciones de poblaciones por fenómenos de deriva o selección.
Por tanto, a partir de estos dos conceptos podemos clasificar dos tipos de herencia materna:
- Herencia materna homoplasmática: herencia de tipo todo o nada.
- Herencia materna heteroplasmática: el desarrollo de la enfermedad responde al grado de heteroplasmia existente y la intensidad o severidad de la misma dependerá de la proporción de mitocondrias con mutaciones en el tejido afectado.
Herencia autosómica recesiva
La herencia autosómica recesiva es probablemente el modelo más común en las enfermedades mitocondriales, incluyendo desórdenes de oxidación de ácidos grasos, ciclo de Krebs, unidades de la cadena de transporte de electrones codificadas en el núcleo, factores de ensamblaje y transportadores.[1] En la herencia autosómica recesiva, los padres son mínimamente portadores de la copia defectuosa del gen. Si el ovocito y el espermatozoide que lo fecunda tienen la copia defectuosa del gen, entonces el hijo manifestará la enfermedad.
Por consiguiente, en la herencia autosómica recesiva, estadísticamente hablando, el 25% de la descendencia manifestará la enfermedad, el 50% será portador sano y el 25% restante no portará ninguna copia defectuosa del gen.
A pesar de que existen excepciones (especialmente en los desórdenes de oxidación de ácidos grasos), las enfermedades mitocondriales con herencia autosómica recesiva generalmente resultan en enfermedades graves con inicio en la infancia. En hermanos afectados, la enfermedad es similar en edad de inicio, gravedad y órganos involucrados.[1]
Herencia ligada al X recesiva
En las enfermedades ligadas al X, el defecto genético se localiza en el cromosoma X, y usualmente afecta solo a los varones. Esto se debe a que las mujeres tienen dos cromosomas X (uno de la madre y uno del padre), mientras que los varones tienen solo 1, heredado de la madre. Las mujeres con un cromosoma X normal y uno mutado en general no manifiestan la enfermedad debido a la presencia del gen normal. Sin embargo, estas mujeres tienen el riesgo de pasar el defecto a su descendencia y en consecuencia son llamadas "portadoras". Por otro lado, como un varón solo tiene un cromosoma X, si este es mutado, no tendrá ninguna copia normal y desarrollara la enfermedad.
Si una mujer portadora tiene hijos, habrá un 50% de probabilidad de que pase el gen defectuoso a su descendencia. Si una hija recibe el gen defectuoso de la madre, esta se convertirá en portadora también. Si un hijo recibe el gen defectuoso de la madre, este desarrollará la enfermedad.
Una excepción importante es que algunas mujeres pueden presentar una "versión débil" de la enfermedad. En situaciones raras, la enfermedad en los varones es tán grave que es letal antes del nacimiento, de modo que solo se nota la afección en las mujeres. Sin embargo en todas las enfermedades ligadas al X, los varones y las mujeres son afectados de forma diferente, con los varones siempre afectados en forma más grave que las mujeres.
Entre las enfermedades mitocondriales, el tipo más común de deficiencia del complejo piruvato deshidrogenasa (E1 alpha) es ligado al X.[3] Paradójicamente, esta es una de las pocas enfermedades ligadas al X en las que las mujeres heterocigotas manifestan síntomas graves.[4]
Herencia autosómica dominante
En la herencia autosómica dominante, solo una copia del gen defectuoso es necesaria para que se desarrolle la enfermedad asociada. Esto significa que las personas que sufren de la enfermedad, tienen un 50% de pasar el gen defectuoso un individuo de su descendencia. Sin embargo, con un gen normal y uno mutado, estos individuos podrán mostrar o no síntomas de la enfermedad. Y de mostrar síntomas, la gravedad puede variar ampliamente. Respecto de la gran variedad de manifestaciones en individuos con un gen defectuoso, las enfermedades mitocondriales de herencia autosómica dominante y las de herencia materna son similares. Sin embargo, en las enfermedades de herencia autosómica dominante, pero nunca en las de herencia materna, los varones pueden pasar el gen defectuoso a su descendencia.
Entre las enfermedades mitocondriales, una forma rara del síndrome de Kearns-Sayre es de herencia autosómica dominante.[5]
Casos esporádicos (cuando no hay familiares afectados)
En la mayoría de los casos, el paciente es el único miembro de la familia afectado con enfermedad mitocondrial. Estos se llaman casos esporádicos. En estos casos todos los afectados serán heteroplásmicos, ya que siempre que aparece de forma espontánea una enfermedad mitocondrial es heteroplásmica.
No todas las enfermedades mitocondriales tienen un origen principal genético. Por ejemplo, los medicamentos antirretrovirales usados para tratar el VIH (sida) pueden dañar a las mitocondrias y causar síntomas debido al fallo energético resultante. La interrupción del suministro de estas drogas revierte el proceso y los síntomas cesan. Hay muchas otras causas ambientales de enfermedad mitocondrial, y probablemente existan muchas de las que aún no se conoce nada.[1]
La mayoría de las enfermedades mitocondriales probablemente sean tanto genéticas como ambientales en lo que respecta a su origen. Por ejemplo, en el caso de los medicamentos antirretrovirales, miles de individuos no experimentan problemas con estas drogas, mientras que un grupo reducido sí. Es probable entonces que en estos casos haya una predisposición genética de unos pocos individuos a una enfermedad "ambiental".
Cuando el origen de la enfermedad es genético, en general la mutación fue heredada, pero esto no es siempre así.[1] Existen nuevas mutaciones o mutaciones "de novo", en particular deleciones de mtDNA tienden a ser mutaciones no presentes en la madre o hermanos. Sin embargo, existen también deleciones con duplicaciones que son usualmente heredadas.
En conclusión, en los casos en los que el paciente es el único miembro de la familia con enfermedad mitocondrial, la condición es probablemente genética, y puede haber sido heredada o no. Pueden estar involucrado tanto el DNA nuclear como el mtDNA. La herencia es probablemente autosómica recesiva o materna, pero no necesariamente. La condición puede ser no heredada, es decir, deberse a una nueva mutación.
En el mtDNA, la frecuencia de mutaciones es alrededor de 10 veces la correspondiente al ADN nuclear, debido a diferentes motivos como son: la ausencia de histonas protectoras adosadas, la ausencia del efectivo sistema de reparación que posee el DNA nuclear y la exposición a los radicales libres originados en la fosforilación oxidativa.[6]
Las enfermedades como el síndrome de Kearns-Sayre, síndrome de Pearson y la oftalmoplejía progresiva externa se considera que se deben a reacomodamientos en el mtDNA a gran escala, mientras que otras enfermedades, tales como el síndrome MELAS, la neuropatía óptica hereditaria de Leber, el síndrome de epilepsia mioclónica asociada a fibras rojas rotas (MERRF) y otras se deben a mutaciones puntuales en el mtDNA.
Pruebas clínicas de genética molecular
Los estudios se suelen realizar en biopsias de músculo esquelético (donde se concentran gran cantidad de mitocondrias), ya que muchas veces no se detectan en sangre. Métodos empleados para el diagnóstico genético de las enfermedades mitocondriales:
- Southern para detectar grandes deleciones o duplicaciones.
Con esta técnica se realizan estudios de hibridación con ADN genómico, así como RFLP. El procedimiento consiste en digerir el ADN mitocondrial con enzimas de restricción cuyas dianas se han descrito en el ADN (se emplea la base de datos MITOMAP para determinar las dianas) y, posteriormente, se realiza el southern con sondas mitocondriales. Las mutaciones casi siempre alteran el patrón de corte de las enzimas, dado que se modifican las dianas o la longitud de los fragmentos digeridos, de tal forma que se puede detectar la mutación.
- PCR y análisis de mutación concreto.
En este caso se amplifica la región de ADN de interés por PCR y luego se lleva a cabo una digestión con enzimas de restricción, al igual que en el caso anterior, para estudiar el polimorfismo de la longitud de los fragmentos (RFLP). Esta técnica se basa en que la presencia de mutaciones crea nuevos puntos de corte que pueden dar lugar a fragmentos de distintos tamaños.
- Secuenciación del genoma mitocondrial entero.
Complicaciones
- La gravedad de la enfermedad no se correlaciona con el grado de heteroplasmia: no se puede hacer diagnóstico predictivo por amniocentesis ni estudiar si los hijos van a tener o no la enfermedad, sólo se pueden hacer estudios para confirmar la enfermedad una vez que ya la padece.
- La presencia o no de la enfermedad no se puede predecir con el grado de heteroplasmia detectado en determinado tejido. Se han registrado casos en los que miembros con un mayor porcentaje de ADN micondrial mutado no presentan síntomas o estos son menos graves que los que experimenta otro pariente suyo con menos ADN mutado en sus mitocondrias.
- Puede haber una expresión variable en miembros de una familia con una mutación en homoplasmia.
- No todas las mutaciones dan lugar a fenotipos patológicos.
- Elección del tejido sobre el que realizar el análisis: en tejidos en división desaparecen las mitocondrias anormales, mientras que en los tejidos inactivos se acumulan.
- La distribución por tejidos de la heteroplasmia varía con la edad.
- Las mitocondrias que presenan deleciones en su genoma se duplican algo más rápido que aquellas que no presenta deleción (existe menos ADN que replicar), por lo que proliferan más y, a la larga, las mitocondrias con deleción van sustituyendo a las normales. Esto puede provocar que a partir de cierta edad aparezcan síntomas relativos a una enfermedad mitocondrial.
Consejo genético y nuevas terapias
Todas las características anteriores hacen que el consejo genético en este tipo de enfermedades sea bastante turbio. En aquellas parejas que deseen tener hijos y en cuyas familias existan antecedentes de estas enfermedades, las técnicas PGD (Diagnóstico preimplantatorio) y PND (Diagnóstico prenatal) no tienen, en la mayoría de los casos, un valor pronóstico. Es decir, no permiten garantizar que el futuro bebé nacerá sano (sin la enfermedad mitocondrial que padece la madre), incluso si se detectan mitocondrias aparentemente normales. Ambas técnicas pueden servir para descartar embriones cuya carga mitocondrial mutada sea elevada, de forma que se presuma que en el futuro se desarrollará la enfermedad mitocondrial en cuestión. En tales casos, se puede practicar una interrupción voluntaria del embarazo (IVE). No obstante, también puede darse el caso de que un embrión con mayor cantidad de ADN mitocondrial mutado, sea descartado en el procedimiento de IVF, cuando podría no haber tenido la enfermedad. En definitiva, las condiciones de heteroplasmia y expresión variable asociadas a las enfermedades mitocondriales, impiden predecir el grado de la patología que pueda desarrollarse. Este hecho hace que el consejo genético para estas parejas afectadas que deseen tener hijos, se límite a presentar la posibilidad de que su futuro hijo desarrolle la enfermedad, así como las alternativas clínicas de las que disponen, siendo imposible predecir la gravedad de la enfermedad.
Cabe mencionar, que los casos en los que la madre es portadora de una mutación homoplásmica son los más complejos a la hora de concebir. Dado al carácter homoplásmico de la mutación, todos los hijos que tenga dicha mujer portarán las mitocondrias afectadas y, consiguientemente, padecerán la enfermedad (salvo raras excepciones). De esta manera, la única alternativa que se le plantea para tener hijos es recurrir a la adopción o a la donación de óvulos de una donante sana. En ninguno de los dos casos, la madre biológica (la portadora de la mutación mitocondrial) mantendrá un vínculo genético con el niño nacido. Para muchas parejas esto último se plantea como un grave conflicto, puesto que desean enormemente tener hijos relacionados genéticamente.
Nuevas alternativas para evitar la transmisión de enfermedades mitocondriales están siendo valoradas. La HFEA (Human Fertilisation and Embriology Authority) ha lanzado en el Reino Unido una encuesta pública para que los ciudadanos den su opinión al respecto de estas nuevas técnicas, que han pasado a denominarse como "técnicas de reemplazamiento mitocondrial". Dentro de este concepto tan amplio, se encuentran la transferencia del huso mitocondrial (MST) y la transferencia pronuclear (PNT). Ambas técnicas consisten básicamente en extraer el núcleo de la madre portadora de la mutación en el ADN mitocondrial y transferirlo a un oocito enucleado de una donante sana e implantar el embrión resultante de la posterior fecundación, en el útero materno, como en cualquier procedimiento de IVF. La diferencia principal de ambas técnicas es que en el caso de la MST se emplean oocitos todavía no fecundados, mientras que en PNT se emplean cigotos en un estadio muy temprano del desarrollo (cuando aún no se han unido los pronúcleos paterno y materno). Estos procedimientos darían lugar a lo que la prensa ha convenido en denominar "embriones de tres padres" (del inglés, "three-parent embryos") y, a pesar de que aún no han sido llevados a cabo en humanos, han levantado una gran polémica. Sin embargo, existen evidencias para creer que estas nuevas aproximaciones constituyen la única alternativa para que parejas con enfermedades mitocondriales en la línea materna, puedan concebir hijos sanos genéticamente relacionados con ambos progenitores. No obstante, las implicaciones psicológicas y éticas hacen que esto todavía no sea una alternativa disponible para tales parejas.[7]
Síntomas más comunes
Las enfermedades mitocondriales pueden afectar las células del cerebro, nervios, músculos, riñones, corazón, hígado, ojos, oídos o páncreas. Según las características del caso, puede haber un órgano afectado, más de uno, o inclusive todos los órganos pueden estar afectados. Dependiendo de las características de la enfermedad, de las características del individuo y de factores ambientales, la gravedad de la enfermedad puede ir desde leve hasta fatal.
Dependiendo de cuales son las células del cuerpo afectadas, algunos de los síntomas pueden ser:
En el cerebro
- retrasos en el desarrollo,
- demencia,
- problemas neuropsiquiátricos,
- migrañas,
- retraso mental,
- convulsiones,
- parálisis cerebral atípica,
- accidentes cerebrovasculares
En los nervios
- debilidad (puede ser intermitente),
- ausencia de reflejos,
- desmayos,
- dolor neuropático,
- disautonomía - inestabilidad de la temperatura y otros problemas disautonómicos
En los músculos
- debilidad,
- calambres,
- problemas gastrointestinales,
- pérdida de la movilidad,
- síndrome del intestino irritable,
- hipotonía,
- dolor muscular,
- reflujo esofágico,
- diarrea o constipación
En los riñones
- Acidosis Tubular Renal
En el corazón
- defectos de conducción cardíaca,
- cardiomiopatía
En el hígado
En ojos y oídos
- baja visión y ceguera,
- ptosis palpebral,
- oftalmoplejía,
- atrofia óptica,
- hipoacusia y sordera,
- estrabismo adquirido,
- retinitis pigmentosa
En el páncreas y otras glándulas
- diabetes y insuficiencia pancreática exocrina, (incapacidad de producir enzimas digestivas),
- hipoparatiroidismo (calcio bajo),
Clasificación
Encefalomiopatías mitocondriales
Algunos ejemplos de encefalomiopatías mitocondriales son:
- Encefalomiopatía mitocondrial, acidosis láctica, episodios seudosincopales (MELAS)
- grado variable de deterioro cognitivo y demencia
- acidosis láctica
- accidentes cerebrovasculares
- accidentes isquémicos transitorios
- pérdida de la audición
- pérdida de movilidad
- pérdida de peso
- Síndrome de epilepsia mioclónica asociada a fibras rojas rotas (MERRF)
- epilepsia mioclónica progresiva
- la observación con el microscopio óptico de biopsias musculares coloreadas con coloración tricrómica permite distinguir un patrón en armadura característico, con cúmulos de mitocondrias
- baja estatura
- Síndrome de Kearns-Sayre
- oftalmoplejía externa
- defectos de conducción cardíaca
- pérdida de audición neurosensorial
- Oftalmoplejia externa progresiva crónica
- Ptosis palpebral
- Oftalmoplejia externa
Otras enfermedades mitocondriales
- Diabetes mellitus y sordera (DAD)
- esta combinación en una edad temprana se puede deber a enfermedad mitocondrial
- la diabetes mellitus y la sordera se pueden encontrar juntas también por otras razones
- Neuropatía óptica hereditaria de Leber (LHON)
- pérdida de la visión comenzando en la edad adulta temprana
- síndrome de Wolff-Parkinson-White
- enfermedad del tipo de la esclerosis múltiple
- Síndrome de Leigh
- luego del desarrollo normal la enfermedad comienza usualmente en el primer año de vida, pero los primeros síntomas pueden aparecer en la adultez
- ocurre una rápida declinación en la función y es evidenciada por ataques, estados alterados de la conciencia, demencia y falla respiratoria
Véase también
Referencias
- Richard Boles, M.D. and Terri Mason, Inheritance & Genetics Archivado el 29 de abril de 2009 en Wayback Machine., United Mitochondrial Disease Foundation
- Schwartz, M. y Vissing, J. (2002). Paternal inheritance of mitochondrial DNA (Herencia paterna del ADN mitocondrial). New England Journal of Medicine, 347, 576-580. http://dx.doi.org/10.1056/NEJMoa020350.
- Brown, R. M.; Dahl, H.-H. M.; Brown, G. K.: X-chromosome localization of the functional gene for the E1-alpha subunit of the human pyruvate dehydrogenase complex. Genomics 4: 174-181, 1989. PubMed ID: 2737678
- Brown, G. K.; Otero, L. J.; LeGris, M.; Brown, R. M.: Pyruvate dehydrogenase deficiency. J. Med. Genet. 31: 875-879, 1994. PubMed ID: 7853374
- Leveille, A. S.; Newell, F. W.: Autosomal dominant Kearns-Sayre syndrome. Ophthalmology 87: 99-108, 1980. PubMed ID: 7383548
- Genesser, Histología, Pág. 88, 3° Edición, Editorial Médica Panamericana
- HFEA: Debating mitochondrial replacement. http://mitochondria.hfea.gov.uk/mitochondria/ Archivado el 30 de noviembre de 2012 en Wayback Machine.