Fructólisis
El término fructólisis se refiere al metabolismo de la fructosa proveniente de la dieta. A pesar de que el metabolismo de la glucosa por medio de la glucólisis hace uso de muchas de las mismas enzimas y estructuras intermediarias, los dos azúcares poseen dos destinos muy diferentes en el metabolismo humano. A diferencia de la glucosa, la cual se metaboliza ampliamente en el organismo, la fructosa, en los humanos, se metaboliza casi completamente en el hígado, donde se utiliza directamente para rellenar las reservas hepáticas de glucógeno y para la síntesis de triglicéridos.[1] Menos del uno por ciento de la fructosa ingerida se convierte directamente en triglicéridos plasmáticos.[2] 29% - 54% de la fructosa se convierte en el hígado en glucosa, y aproximadamente un cuarto de la fructosa se convierte en lactato. 15% - 18% se convierte en glucógeno.[3] La glucosa y el lactato normalmente se utilizan para proveer energía a las células de todo el organismo.[2]
La fructosa es un monosacárido dietario, presente naturalmente en frutas y vegetales, ya sea como monosacárido libre o formando parte del disacárido sucrosa, también se encuentra libre en la miel y en azúcares refinados entre los que se incluyen el azúcar granulada, azúcar morena, azúcar impalpable y azúcar turbinada, fructosa refinada y como jarabe de maíz de alta fructosa. Aproximadamente el 10% de las calorías contenidas en la dieta occidental se encuentran provistas por la fructosa (aproximadamente 55g/día).[4]
A diferencia de la glucosa, la fructosa no es un secretagogo de insulina, y de hecho puede hacer descender los niveles de insulina.[5] Además de en el hígado, la fructosa se metaboliza en el intestino, testículos, riñones, músculo esquelético, tejido graso y cerebro,[6][7] aunque no se transporta al interior de las células por medio de vías sensibles a la insulina (la insulina regula a los transportadores GLUT1 y GLUT4). La fructosa, en cambio es tomada por los transportadores GLUT5.
La fructólisis y la glucólisis son vías independientes
Aunque el metabolismos de la fructosa y de la glucosa comparten muchos de las mismas estructuras intermediarias, estos dos azúcares poseen destinos muy diferentes en el metabolismo humano. La fructosa es metabolizada casi completamente en el hígado humano, donde es dirigida a recuperar los depósitos de glucógeno hepático y hacia la síntesis de triacilgliceroles, mientras que mucha de la glucosa incorporada con la dieta pasa a través del hígado y se dirige al músculo esquelético, donde es metabolizada para producir CO
2, H
2O y ATP, y para engordar a aquellas células donde se metaboliza primariamente a glicerol fosfato para la síntesis de triacilgliceroles y para la producción de energía.[1] Los productos del metabolismo de la fructosa son glucógeno hepático y ácidos grasos sintetizados de novo, con una eventual síntesis de triacilgliceroles endógenos. La segunda fase es el subsecuente metabolismo de estas triosas ya sea en la vía gluconeogénica para la recuperación de glucógeno hepático, o dirigirse al metabolismo completo por la vía fructolítica para producir piruvato, el cual ingresa al ciclo de Krebs, se convierte en citrato y luego puede ser dirigido a la síntesis de novo del ácido graso palmitato.[1]
El metabolismo de la fructosa para formar DHAP y gliceraldehído
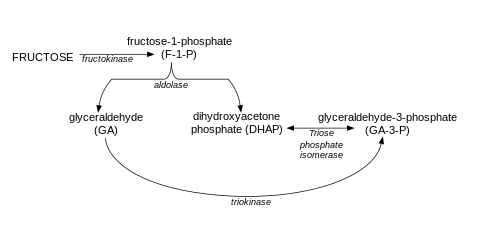
El primer paso en el metabolismo de la fructosa es la fosforilación de la fructosa para formar fructosa 1-fosfato, reacción mediada por la enzima fructoquinasa (Km = 0.5 mM, ≈ 9 mg/100 ml), capturando de esta forma fructosa para su metabolismo en el hígado. La hexoquinasa IV, que también se presenta en el hígado, es capaz de fosforilar a la fructosa para producir fructosa 6-fosfato (un intermediario en la vía de la gluconeogénesis); sin embargo esta enzima tiene una km relativamente alta para la fructosa (12mM), y por lo tanto prácticamente toda la fructosa se convierte en fructosa 1-fosfato en el hígado humano. Por otro lado, mucha de la glucosa no resulta fosforilada en el hígado (km de la hexoquinasa IV = 10 mM), por lo que pasa a través del hígado directamente hacia el tejido periférico, donde es captado por el transportador de glucosa dependiente de insulina GLUT 4, que se encuentra presente en tejido adiposo y músculo esquelético.
La fructosa 1-fosfato sufre luego un proceso de hidrólisis, mediado por la fructosa 1-fosfato aldolasa (aldolasa B), para formar dihidroxiacetona fosfato (DHAP) y gliceraldehído; el DHAP puede ser isomerizado a gliceraldehído 3-fosfato por la triosafosfato isomerasa, o sufrir una reducción para formar glicerol 3-fosfato, proceso mediado por la glicerol 3-fosfato deshidrogenasa. El gliceraldehído producido también se puede convertir en gliceraldehído-3-fosfato por la gliceraldehído quinasa o en glicerol-3-fosfato por la gliceraldehído-3-fosfato deshidrogenasa.
El metabolismo de la fructosa a este punto conduce a la formación de intermediarios en la vía gluconeogénica conduciendo a la síntesis de glucógeno, o puede ser oxidado a piruvato y reducido a lactato, o descarboxilado para formar acetil CoA en las mitocondrias y dirigido a la síntesis de ácidos grasos, que finalmente desemboca en la síntesis de triacilgliceroles.
Síntesis de glucógeno a partir de DHAP y glyceraldeído-3-fosfato
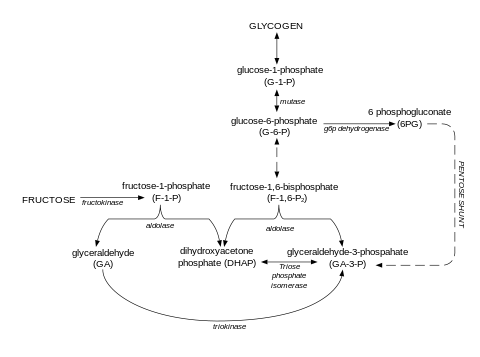
La síntesis de glucógeno en el hígado luego de una comida que contenga fructosa procede a partir de precursores gluconeogénicos. La fructosa se convierte inicialmente en DHAP y gliceraldehído por medio de la fructoquinasa y la aldolasa B. El gliceraldehído resultante sufre luego una fosforilación para convertirse en gliceraldehído 3-fosfato.
Los aumentos en la concentración de DHAP y gliceraldehído 3-fosfato en el hígado derivan a la vía gluconeogénica hacia la producción de glucosa 6-fosfato, glucosa 1-fosfato y glucógeno. Aparentemente la fructosa es un mejor sustrato para la síntesis de glucógeno que la glucosa y esta recuperación de los depósitos de glucógeno toma precedencia sobre la formación de triglicéridos.[8] Una vez que se ha completado la recuperación de los niveles de glucógeno, los intermediarios del metabolismo de la fructosa se derivan principalmente hacia la síntesis de triglicéridos.
Síntesis de triglicéridos a partir de DHAP y gliceraldehído 3-fosfato
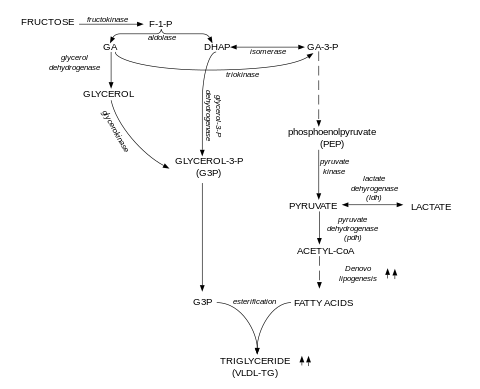
Si se hace un rastreo de los átomos de carbono provenientes de la fructosa, se encuentra que aparecen tanto en las moléculas de ácidos grasos como de glicerol presentes en los triglicéridos del plasma. El excedente de fructosa incorporada con la dieta puede ser convertida en piruvato, entrar al ciclo del ácido cítrico de donde emerge convertido en citrato desde donde es dirigido a la síntesis de ácidos grasos libres en el citosol de los hepatocitos. El DHAP formado durante la fructólisis puede también ser convertido en glicerol y glicerol 3-fosfato para la síntesis de triacilgliceroles.
Por lo tanto, la fructosa provee triosas tanto para el esqueleto de glicerol 3-fosfato, como para la síntesis de ácidos grasos libres en la síntesis de TG. Ciertamente, la fructosa podría ser la principal proveedora de carbohidrato para la síntesis de novo de triglicéridos en humanos.
La fructosa induce a las enzimas lipogénicas hepáticas
El consumo de fructosa provoca la inducción dependiente de insulina de varias enzimas hepáticas lipogénicas de importancia, entre las que se incluyen la piruvato quinasa, malato deshidrogenasa (NADP+), ATP citrato liasa, acetil-CoA carboxilasa, ácido graso sintasa, como así también la piruvato deshidrogenasa. Aunque no es un hallazgo consistente entre diferentes estudios, las dietas altas en fructosa altamente refinada, han mostrado favorecer la aparición de hipertrigliceridemia en un amplio rango de poblaciones entre las que se incluyen individuos con un metabolismo normal de la glucosa e individuos con una tolerancia a la glucosa alterada, diabetes, hipertrigliceridemia, e hipertensión. Los efectos hipertrigliceridemiantes osbservados son la marca característica de una dieta con un consumo de carbohidratos aumentados, y la fructosa aparenta ser dependiente de un gran número de factores entre los que se incluyen la cantidad de fructosa consumida con la dieta, y el grado de resistencia a la insulina.
| Grupo | Piruvato Quinasa | NADPH-Malato Deshidrogenasa |
Citrato Liasa | Acetil CoA Carboxilasa |
Ácdo Graso Sintasa |
|---|---|---|---|---|---|
| Animales Control | |||||
| Dieta Control | 495 ± 23 | 35 ± 5 | 21 ± 3 | 6.5 ± 1.0 | 3.6 ± 0.5 |
| Dieta con Fructosa | 1380 ± 110* | 126 ± 9* | 69 ± 7* | 22.5 ± 2.7* | 10.8 ± 1.4* |
| Animales Diabéticos | |||||
| Dieta Control | 196 ± 21 | 14 ± 3 | 9 ± 2 | 3.1 ± 0.8 | 1.4 ± 0.6 |
| Dieta con Fructosa | 648 ± 105* | 70 ± 9* | 37 ± 6* | 10.3 ± 2.0* | 3.9 ± 0.9* |
‡ = Actividad media ± EEM en nmol/min por mg proteína
§ = 12 ratas/grupo
* = Significantemente diferente del control a p < 0,05
Shafrir, E. (1991). «Fructose/Sucrose metabolism, its physiological and pathological implications.». En Kretchmer, N. & Hollenbeck, CB., ed. Sugars and Sweeteners,. Boca Raton:FL: CRC Press. ISBN 0-8493-8835-X.
Anormalidades en el metabolismo de la fructosa
La falta de dos importantes enzimas en el metabolismo de la fructosa conduce al desarrollo de dos errores congénitos en el metabolismo de los carbohidratos: la fructosuria esencial y la intolerancia hereditaria a la fructosa. Adicionalmente, puede ocurrir una reducción en el potencial de fosforilación en los hepatocitos si se efectúa una infusión endovenosa de fructosa.
Fructosuria esencial
La ausencia de fructoquinasa causa la incapacidad para fosforilar a la fructosa para convertirla en fructosa 1-fosfato en el interior de la célula. Como resultado, la fructosa no queda retenida dentro de la célula ni puede ser dirigida hacia su metabolismo. Las concentraciones de fructosa libre en el hígado aumentan, y esta fructosa queda libre para dejar las células y pasar al plasma. Esto provoca un aumento en los niveles plasmáticos de fructosa, excediendo eventualmente el umbral renal de la fructosa y provocando su aparición en la orina. La fructosuria esencial es una condición benigna y asintomática.
Intolerancia hereditaria a la fructosa
La ausencia de fructosa 1-fosfato aldolasa (aldolasa B) provoca la acumulación de fructosa 1-fosfato en los hepatocitos, riñones e intestino delgado. La acumulación de fructosa 1-fosfato a continuación de la ingestión de fructosa inhibe la glucogenólisis y la gluconeogénesis, provocando una hipoglucemia severa muy sintomática. Se caracteriza por presentar severa hipoglucemia, dolor abdominal, vómitos, hemorragias, ictericia, hepatomegalia e hiperuricemia, conduciendo eventualmente a una falla renal o hepática que desemboca en la muerte. La incidencia varía en todo el mundo, pero se estima que se encuentra en aproximadamente 1/20 000 nacidos vivos (en un rango de 1/12 000 a 1/58 000).
Potencial de fosforilación reducido
Se ha demostrado que la infusión intravenosa de fructosa disminuye el potencial de fosforilación en las células del hígado por medio de la captura de fosfato de alta energía como fructosa 1-fosfato.[9] La reacción de la fructoquinasa ocurre muy rápidamente en los hepatocitos, atrapando fructosa en las células por fosforilación. Por otro lado, la ruptura de fructosa 1-fosfato para dar DHAP y gliceraldehído mediada por la aldolasa B es un proceso relativamente lento. Por consiguiente, la fructosa 1-fosfato se acumula en el interior de las células con el correspondiente descenso en los niveles de fosfato inorgánico disponibles para las reacciones de fosforilación en la célula. Esta es la razón por la cual la fructosa se encuentra contraindicada para nutrición parenteral total, y nunca se da en forma intravenosa como fuente de carbohidratos. Se ha sugerido que una ingesta excesiva de fructosa podría provocar también una reducción en el potencial de fosforilación. Sin embargo esto aún es materia de debate. La fructosa dietaria no se absorbe muy bien, y un aumento en la ingesta muchas veces resulta en malabsorción. Si se pueden o no absorber por vía dietaria la suficiente cantidad de fructosa para causar una reducción significativa en el potencial de fosforilación, sigue siendo cuestionable y no existen claros ejemplos en la literatura.
Referencias
- McGrane, MM (2006). Carbohydrate Metabolism: Synthesis and Oxidation. Missouri: Saunders, Elsevier. pp. 258-277.
- «Copia archivada». Archivado desde el original el 17 de octubre de 2015. Consultado el 27 de diciembre de 2015.
- http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3649104/
- https://www.inkling.com/read/illustrated-reviews-biochemistry-harvey-5th/chapter-12/fructose-metabolism
- «Copia archivada». Archivado desde el original el 7 de enero de 2021. Consultado el 27 de diciembre de 2015.
- Douard, V; Ferraris, R. P. (2008). «Regulation of the fructose transporter GLUT5 in health and disease». AJP: Endocrinology and Metabolism 295 (2): E227-37. PMC 2652499. PMID 18398011. doi:10.1152/ajpendo.90245.2008.
- Hundal, H. S.; Darakhshan, F; Kristiansen, S; Blakemore, S. J.; Richter, E. A. (1998). «GLUT5 expression and fructose transport in human skeletal muscle». Advances in experimental medicine and biology 441: 35-45. PMID 9781312. doi:10.1007/978-1-4899-1928-1_4.
- Parniak, MA; Kalant N (1988). «Enhancement of glycogen concentrations in primary cultures of rat hepatocytes exposed to glucose and fructose». Biochemical Journal 251 (3): 795-802. PMC 1149073. PMID 3415647.
- Segebarth, C; Grivegnée AR, Longo R, Luyten PR, den Hollander JA. (1991). «In vivo monitoring of fructose metabolism in human liver by means of 32P magnetic resonance spectroscopy». Biochimie 73 (1): 105-108. PMID 2031955. doi:10.1016/0300-9084(91)90082-C.
Enlaces externos
- The Entry of Fructose and Galactose into Glycolysis, Chapter 16.1.11. Biochemistry, 5th edition, Jeremy M Berg, John L Tymoczko, and Lubert Stryer, New York: W H Freeman; 2002.
- Tappy, L; Lê, K. A. (2010). «Metabolic effects of fructose and the worldwide increase in obesity». Physiological Reviews 90 (1): 23-46. PMID 20086073. doi:10.1152/physrev.00019.2009.