Human herpesvirus 8
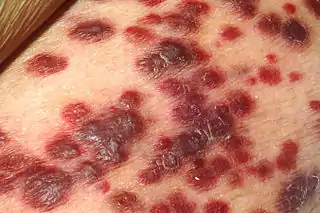
Human herpesvirus 8, VHH-8 o virus del sarcoma de Kaposi es un Rhadinovirus. Fue identificado en 1994[1] como responsable de ese tipo de cáncer, que ataca a las personas inmunodeprimidas y que se convirtió en el heraldo de una nueva epidemia, la de sida, cuando empezó a aparecer con una frecuencia antes desconocida entre varones homosexuales de Estados Unidos.
| VHH-8 | ||
|---|---|---|
 | ||
| Taxonomía | ||
| Dominio: | Duplodnaviria | |
| Orden: | Herpesvirales | |
| Familia: | Herpesviridae | |
| Subfamilia: | Gammaherpesvirinae | |
| Género: | Rhadinovirus | |
| Especie: | Human herpesvirus 8 | |
| Clasificación de Baltimore | ||
| Grupo: | I (Virus ADN bicatenario) | |
Descubrimiento
Se sospechaba desde hacia decenios que el cáncer conocido como sarcoma de Kaposi debía estar relacionado con una causa infecciosa. En 1994, el equipo de Y. Chang pudo demostrar la presencia de un herpesvirus nuevo asociado a dicho sarcoma.[1] El VHH-8 es el primero de los ocho herpesvirus conocidos en haber sido identificado a través de técnicas moleculares, ya no por cultivo celular, amplificando dos genes extraños encontrados en tumores de Kaposi que resultaron próximos a otros conocidos: respectivamente, del virus de Epstein-Barr y de un herpevirus del mono ardilla.[2]
Clasificación
El VHH-8 es un herpesvirus (fam. Herpesviridae) encuadrado en la subfamilia Gammaherpesvirinae y en el género Rhadinovirus. Aunque el género Rhadinovirus está extensamente representado entre los primates, tanto del Viejo como del Nuevo Mundo, este es el primero que se encuentra en la especie humana. Los herpesvirus son virus ADN de cadena doble, así que la clasificación de Baltimore los incluye en el grupo I.
Epidemiología
Prevalencia
La prevalencia (proporción de individuos infectados) es muy variable cuando se comparan regiones y grupos de riesgo.[3] La tasa más alta (hasta 50 %) se observa en África Central. La tasa es también elevada, aunque menos y de forma heterogénea (10-20 %), en los países del Mediterráneo. Es de estos países de donde es característica la variante del sarcoma de Kaposi que suele llamarse «endémica». En Estados Unidos son las poblaciones de esos orígenes las que lo presentan con mayor frecuencia. El resto de las poblaciones, como las de Europa Central y Septentrional, el Este o el Sur de Asia, presentan prevalencias de menos del 5 %. En estas poblaciones, sin embargo, la prevalencia es mayor en varones homosexuales.[2]
Transmisión
En las regiones geográficas donde la prevalencia es baja el principal modo de transmisión es por relaciones sexuales transanales en parejas heterosexuales u homosexuales. El ADN viral se observa en el esperma, aunque escaso, y en la saliva. En la transmisión heterosexual, que actualmente no es rara, la prevalencia es mayor entre mujeres con antecedentes de enfermedades de transmisión sexual, como la sífilis.[4]
La prevalencia entre la población de hemofílicos y transfundidos en países de baja prevalencia no es mayor que entre donantes de sangre, lo que parecería indicar que la transfusión no es un modo significativo de infección. Sin embargo un estudio reciente en Uganda, donde la seropositividad VHH-8 es muy alta, indica que la transfusión provoca la seroconversión con una frecuencia significativa (inferior en cualquier caso al 5%).[5]
En los países de alta prevalencia, sobre todo en África Central, los datos epidemiológicos revelan que la seropositividad se alcanza en la mayor parte de los casos antes de la pubertad, lo que excluye las relaciones sexuales como forma principal de transmisión. La prevalencia es baja en recién nacidos, de manera que, a diferencia de lo que ocurre con el VIH, la transmisión no parece ligada al parto o la lactación. Se ha postulado que el uso de la saliva por la madre en el cuidado de las picaduras de insectos puede ser uno de los principales mecanismos implicados.[6]
Patologías asociadas
El HHV-8 no produce solo el sarcoma de Kaposi, sino también dos enfermedades linfoproliferativas: el linfoma efusivo primario y la enfermedad multicéntrica de Castleman. Aunque en el primer caso la presencia activa del virus y los mecanismos moleculares de la patogénesis son bien conocidos, en los otros dos la actividad lítica es menor (aunque la seroprevalencia en los pacientes es un 100 %) y los mecanismos todavía no se conocen.[7]
El linfoma efusivo primario es un linfoma de células B que no produce masas tumorales evidente, pero sí efusiones en las cavidades corporales. El VHH-8 se identifica en el 100 % de los casos, y la OMS lo considera parte de la lista de enfermedades indicativas del desarrollo del sida, aunque puede presentarse en pacientes seronegativos para el VIH.
La enfermedad multicéntrica de Castleman produce linfoadenopatías e hiperglobulinemia, entre otros signos. El VHH-8 se detecta en los órganos afectados de más del 95 % de los pacientes positivos para el VIH y en el 40 % de los negativos. Las lesiones se consideran no malignas, pero la condición predispone para el desarrollo de linfoma no-Hodgkin (linfoma asociado al sida).
Historia natural
La evolución natural de la infección (su historia natural) depende del modo de infección y distingue a las variantes del sarcoma de Kaposi. En la forma clásica, que se presenta con frecuencia en hombres ancianos de países mediterráneos, la progresión de la enfermedad puede requerir décadas. La forma endémica que afecta a muchos niños y adultos en África tarda meses en progresar. El avance más rápido es el que se da en el sida en ausencia de tratamiento, porque cuando aparece puede requerir meses o solo semanas. En pacientes inmunosuprimidos, generalmente en relación con trasplantes, la progresión dura meses, pero se detiene si se restaura la condición inmunitaria normal.
La mayoría de las personas seropositivas para el virus VHH-8 no presentan síntomas, es decir, la infección no se presenta como enfermedad. La incubación en los seropositivos para el VIH, el virus del sida, de las enfermedades provocadas por el VHH-8 puede ser más o menos larga y parece depender del grado de progresión de la inmunodepresión propia del sida, más que del tiempo de infección por el VHH-8. Tanto el sarcoma de Kaposi como la enfermedad de Castleman han disminuido radicalmente en su incidencia, con la introducción de las terapias antirretrovirales de alta actividad.[3]
Patogénesis
Alrededor de una sexta parte de los casos de cáncer son provocados por virus, y la incidencia es mayor en los países menos desarrollados.[8] Los virus que provocan cáncer se reparten entre varios grupos, entre los cuales se incluye a dos familias de virus ARN y a todas las de virus con ADN (grupos I y II de la clasificación de Baltimore), salvo los parvovirus (fam. Parvoviridae).[9] La infección por el virus no implica automáticamente el desarrollo de un cáncer, y la prevalencia de la infección siempre es mucho mayor, y se observan períodos de latencia a menudo muy largos. La inmunodepresión, cualquiera que sea su causa, aumenta la probabilidad del cáncer entre los seropositivos para el virus cancerogénico. En el caso del VHH8, la prevalencia en la población mundial se ha estimado entre un 2 y un 8 %,[10] pero solo con la irrupción de la epidemia de VIH y la inmunosupresión que provoca (SIDA) el sarcoma de Kaposi se ha vuelto relativamente frecuente en grupos de edad y regiones donde antes era casi desconocido.
A diferencia de lo que ocurre cuando el virus cancerogénico es de tipo ARN, los oncogenes implicados no son variantes de los genes celulares, sino genes propios del virus, y son esenciales tanto para la replicación viral como para la transformación de las células en cancerosas. El VHH8 posee un número de genes homólogos de los de la regulación celular, incluidos genes relativos a las quemoquinas, los factores de proliferación celular, las moléculas del sistema de comunicación intercelular y los inhibidores de la apoptosis.[9]
El antígeno LANA1 (del inglés latency-associated nuclear antigen 1) con el factor de transcripción Sp1, transactivando el promotor TERT y contribuyendo a la elongación de los telómeros, lo que produce una «inmortalización» de las líneas celulares afectadas. Los antígenos LANA1 y LANA2 afectan negativamente el trabajo del gen p53. El primero inhibe la muerte celular dependiente del p53. El segundo es específico de las células B, a las que confiere mayor supervivencia, lo que representaría un mecanismo mayor en la promoción de linfomas por el HHV8.
Tanto el HHV8 como el virus de Epstein-Barr presentan, además de su juego exclusivo de proteínas oncogenéticas, otras que presentan homología de secuencia con proteínas celulares, aunque sin los intrones que se encuentran en estas. Se interpreta que pueden proceder de la retrotranscripción de ARNm con ayuda retroviral[11] o ser el resultado de convergencia evolutiva.
Bibliografía
Dos revisiones modernas que contienen la información más relevante y muchas referencias adicionales:
- Cathomas, G. (2003). Kaposi's sarcoma-associated herpesvirus (KSHV)/human herpesvirus 8 (HHV-8) as a tumour virus. Herpes 10(3), 72-7. PMID 14759339.
- Plancoulaine, S., and Gessain, A. (2005). Aspects épidémiologiques de l’herpèsvirus humain 8 (HHV-8) et du sarcome de Kaposi. Méd. Mal. Infect. 35(5), 314-21. PMID 15907610.
Notas
Referencias citadas
- Y. Chang; E. Cesarman; M. S. Pessin; F. Lee; J. Culpepper; D. M. Knowles; P. S. Moore (1994). «Identification of herpesvirus-like DNA sequences in AIDS-associated Kaposi's sarcoma». Science 266 (5192): 1865-1869. PMID 7997879.
- S. Plancoulaine; A. Gessain (2005). «Aspects épidémiologiques de l'herpèsvirus humain 8 (HHV-8) et du sarcome de Kaposi». Médecine et Maladies Infectieuses 35 (5): 314-321. PMID 15907610.
- K. Antman; Y. Chang (2000). «Kaposi's sarcoma». N Engl J Med 342 (14): 1027-1038. PMID 10749966.
- R. Tedeschi; L. Caggiari; I. Silins; I. Kallings; A. Andersson-Ellstrom; P. De Paoli; J. Dillner (2000). «Seropositivity to human herpesvirus 8 in relation to sexual history and risk of sexually transmitted infections among women». Int J Cancer 87 (2): 232-235.
- W. Hladik; S. C. Dollard; J. Mermin; A. L. Fowlkes; R. Downing; M. M. Amin; F. Banage; E. Nzaro; P. Kataaha; T. J. Dondero; P. E. Pellett; E. M. Lackritz (2006). «Transmission of human herpesvirus 8 by blood transfusion». N Engl J Med 355 (13): 1331-1338. PMID 17005950.
- M. Coluzzi; M. L. Calabro; D. Manno; L. Chieco-Bianchi; T. F. Schulz; V. Ascoli (2004). «HHV-8 transmission via saliva to soothe blood-sucking arthropod bites». Br J Cancer 91 (5): 998-999; author reply 999. PMID 15305196.
- G. Cathomas (2003). «Kaposi's sarcoma-associated herpesvirus (KSHV)/human herpesvirus 8 (HHV-8) as a tumour virus». Herpes 10 (3): 72-77. PMID 14759339.
- D. Elgui de Oliveira (2006). «DNA viruses in human cancer: An integrated overview on fundamental mechanisms of viral carcinogenesis». Cancer Lett (in press). PMID 16814460.
- J. S. Butel (2000). «Viral carcinogenesis: revelation of molecular mechanisms and etiology of human disease». Carcinogenesis 21 (3): 405-426. PMID 10688861.
- J. C. Leao; S. Porter; C. Scully (2000). «Human herpesvirus 8 and oral health care: an update». Oral Surg Oral Med Oral Pathol Oral Radiol Endod 90 (6): 694-704. PMID 11113813.
- J. Nicholas (2000). «Evolutionary aspects of oncogenic herpesviruses». Mol Pathol 53 (5): 222-237. PMID 11091846.
Enlaces externos
- Capítulo dedicado al VHH-8 en un curso de virología. Claro, pero no muy al día
- Human Herpesvirus-8: Related Resources Archivado el 17 de septiembre de 2008 en Wayback Machine. HIV InSite (en inglés)