Tirosina
La tirosina (abreviado en español como Tir o Y, y Tyr o Y en inglés) es uno de los veinte aminoácidos que forman las proteínas. Se clasifica como un aminoácido no esencial en los mamíferos ya que su síntesis se produce a partir de la hidroxilación de otro aminoácido: la fenilalanina. Esto se considera así siempre y cuando la dieta de los mamíferos contenga un aporte adecuado de fenilalanina. Por tanto el aminoácido fenilalanina sí que es esencial.
| Tirosina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Ácido 2-Amino-3-(4-hidroxifenil)-propanoico | ||
| General | ||
| Fórmula semidesarrollada | C9H11N1O3 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 60-18-4[1] | |
| ChEBI | 17895 | |
| ChEMBL | CHEMBL925 | |
| ChemSpider | 5833 | |
| DrugBank | DB00135 | |
| PubChem | 1153 | |
| UNII | 42HK56048U | |
| KEGG | C00082 D00022, C00082 | |
| Propiedades físicas | ||
| Masa molar | 18 121 g/mol | |
| Propiedades químicas | ||
| Acidez | 9,11 pKa | |
| Familia | aminoácidos | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
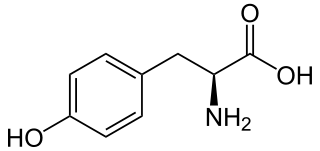
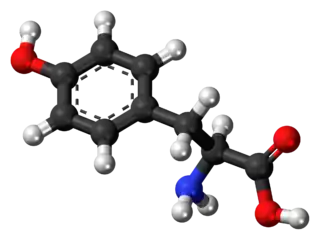
Como todos los aminoácidos está formado por un carbono central alfa (Cα) unido a un átomo de hidrógeno (-H), un grupo carboxilo (-COOH), un grupo amino (-NH2) y una cadena lateral. En la tirosina, la cadena lateral es un grupo fenólico.
La palabra tirosina proviene del griego tyros, que significa queso. Se llama así ya que este aminoácido fue descubierto por un químico alemán llamado Justus von Liebig a partir de la proteína caseína, que se encuentra en el queso.
Se conocen tres isómeros distintos del aminoácido tirosina: para-tirosina, meta-tirosina y la orto-tirosina. Aunque la forma más conocida y estudiada es la para-tirosina o también llamada L-tirosina.
Propiedades
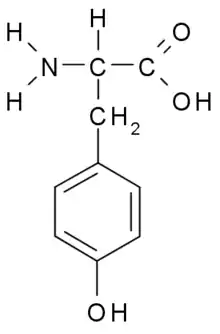
De forma general, las propiedades de los aminoácidos se deben a la naturaleza de su cadena lateral, su reactividad y la conformación de las cadenas proteicas que forman. Lo mismo sucede en la tirosina.
La tirosina es un sólido que forma cristales y que generalmente presenta un color blanquecino, aunque también puede ser incoloro. Se considera un aminoácido polar y protonable. Aunque normalmente se clasifica como aminoácido hidrofóbico a causa de su anillo aromático, hay que tener en cuenta que también contiene un grupo hidroxilo. Normalmente se encuentra sin carga, aunque a pH muy básico presenta carga negativa.
Por lo que respecta a su solubilidad sabemos que es soluble en agua y ligeramente soluble en alcohol. También conocemos su insolubilidad en éter.
Se trata de una molécula ópticamente activa, lo cual significa que hace girar el plano de la luz polarizada. Como la mayoría de los aminoácidos (todos excepto la glicina) presenta una asimetría en el carbono alfa, de manera que no puede superponerse a su imagen en el espejo. Se dice que presenta quiralidad.
El punto isoeléctrico de este aminoácido se encuentra en 5,7. El punto isoeléctrico es el pH en el cual la protonización tiene la misma extensión que la desprotonización.
Por lo que respecta al punto de fusión de la tirosina adquiere valores distintos según el tipo de calentamiento. Al calentar la tirosina de forma rápida y en un tubo cerrado, se funde descomponiéndose a 342 °C aproximadamente. En cambio, al calentar la tirosina de forma lenta se funde a 290 °C.
La masa de la cadena lateral de la tirosina es cercana a los 163,1 Daltons y el promedio de aparición de dicho aminoácido en las proteínas es del 3,5 %.
Este aminoácido absorbe la luz ultravioleta. La eficiencia en la absorción de la energía lumínica está relacionada con su coeficiente de extinción molar. La absorbancia más usual es de una longitud de onda comprendida entre 260 y 300 nm, debido a su cadena lateral. Aunque se sabe que a pH elevado (cuando la cadena lateral de la tirosina tiene un pKa= 10) la absorbancia de la tirosina se desplaza hacia longitudes de onda más elevadas (hacia el rojo). Para la solubilización de la tirosina con agua se requiere calentar a 40 º aproximadamente para alcanzar la solubilización.
Biosíntesis
La síntesis de la tirosina se puede dar de dos formas distintas. En los mamíferos se obtiene a partir de la hidroxilación de la fenilalanina, mientras que en algunos microorganismos se consigue directamente a partir del profenato. El hecho de que la tirosina sea un precursor de catecolaminas (dopamina, adrenalina y noradrenalina), de la melanina y de la tiroxina influye en su síntesis. Esto es debido a que la producción de tirosina está regulada por la demanda de dichas moléculas.
Mamíferos: Hidroxilación de la fenilalanina
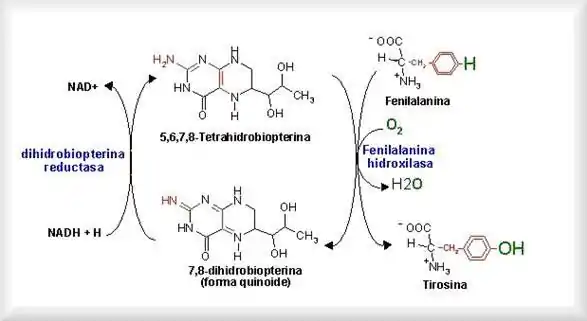
En los mamíferos, la tirosina se sintetiza a partir de un proceso de hidroxilación del aminoácido esencial fenilalanina. En esta reacción interviene la enzima fenilalanina hidroxilasa, la cual precisa un cofactor llamado tetrahidropterina. Esta reacción es irreversible ya que no es posible la síntesis de fenilalanina a partir de la tirosina.
Microorganismos
En los microorganismos el proceso de obtención de la tirosina es el siguiente:
- Condensación del fosfoenolpiruvato (un intermediario de la glucólisis) con la eritrosa 4-fosfato (un intermediario de la vía de las pentosas fosfato). Esta reacción da lugar a un glúcido abierto de siete carbonos.
- Oxidación del glúcido que se había formado. Pierde su grupo fosforilo y forma un anillo de 3-deshidroquinato.
- Deshidratación de dicha molécula para obtener 3-deshidrosiquimato.
- Reducción del 3-deshidrosiquimato a siquimato por la acción del NADPH.
- Fosforilación del siquimato mediante ATP para formar siquimato 3-fosfato.
- Condensación del siquimato 3-fosfato con una molécula de fosfoenolpiruvato para dar lugar a 5-enolpiruvil-inermediario. Esta última molécula pierde su grupo fosforilo y se convierte en corismato. El corismato es el precursor común de los tres aminoácidos aromáticos.
- Conversión del corismato a prefenato, el precursor inmediato de los anillos aromáticos de los aminoácidos fenilalanina y tirosina. Esta conversión tiene lugar mediante la acción de una mutasa.
- Descarboxilación oxidativa del prefanato para obtener p-hidroxifenilpiruvato.
- Transaminación hasta obtener tirosina
El metabolismo de la tirosina
En el metabolismo de la tirosina se producen dos moléculas: fumarato y acetoacetato. Tiene las etapas siguientes:
- Transaminación de la tirosina a p-hidroxifenilpiruvato mediante la acción de una enzima llamada tirosina aminotransferasa.
- Producción de ácido homogentísico a partir del p-hidroxifenilpiruvato. Este paso tiene lugar a partir de una compleja reacción que incluye una descarboxilación, una oxidación, una migración de la cadena carbonada lateral y una hidroxilación.
- Escisión del anillo aromático del ácido homogentísico mediante la enzima homogentisato oxidasa para obtener maleilacetoacetato.
- Isomerización de la forma cis a la forma trans mediante una reacción catalizada por la maleilacetoacetato isomerasa, que da lugar a fumarilacetato .
- Escisión a fumarato y acetoacetato.
El fumarato puede ser utilizado para producir energía en el ciclo de Krebs (o ciclo del ácido tricarboxílico) o bien para la gluconeogénesis. El acetoacetato puede ser utilizado para la síntesis lipídica o para la producción de energía en forma de acetil CoA.
La tirosina como precursor
Los aminoácidos son las unidades a partir de las cuales se obtienen péptidos y proteínas. Pero además actúan como precursores de muchas otras moléculas más pequeñas, pero que desempeñan funciones biológicas importantes y muy variadas. En el caso de la tirosina, se trata de un precursor de las hormonas del tiroides, de las catecolaminas (la adrenalina, la dopamina, la noradrenalina) y de la melanina.
Las catecolaminas
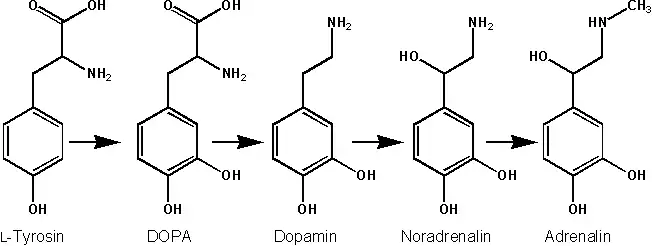
Una parte del acetoacetato y del fumarato metabolizado a partir de tirosina que no se ha utilizado para la síntesis de proteínas se utiliza para obtener catecolaminas mediante las etapas siguientes:
- Hidroxilación de la tirosina a partir de una enzima llamada tirosina hidroxilasa, la cual también precisa la biopterina como cofactor. Se obtiene dihidroxifenilalanina, más conocida como DOPA.
- Descarboxilación de la DOPA mediante la DOPA descarboxilasa, dando lugar a dopamina (un neurotransmisor).
- Hidroxilación de la dopamina en noradrenalina mediante una reacción de hidroxilación donde actúa la dopamina β-hidroxilasa.
- En la médula suprarrenal se convierte la noradrenalina en adrenalina.
Las catecolaminas son conocidas por su regulación de los estados de ánimo. Se ha observado que en niveles bajos de catecolaminas las personas tienden a sufrir ansiedad y depresión.
La melanina
La melanina es un pigmento que da color al pelo y a la piel. Además protege de las radiaciones ultravioletas. La conversión de tirosina a melanina requiere la participación de tirosinasa, una proteína catalítica que se caracteriza por contener cobre. El proceso se puede apreciar en el esquema:
Hormonas del tiroides: triyodotironina y tiroxina
Las hormonas básicas de la glándula tiroides son la tiroxina (T4) y su forma celular activa: la triyodotironina (T3). El aminoácido tirosina está involucrado en el proceso de formación de estas hormonas necesarias para el organismo. El proceso de síntesis es el siguiente:
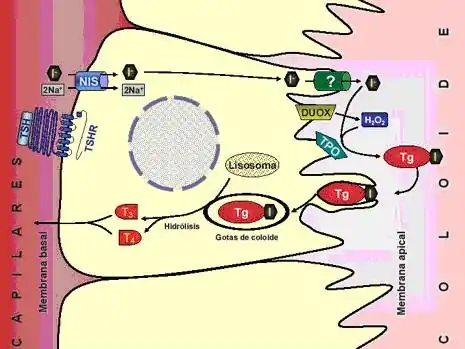
- Captación y concentración del yodo. El yodo que ingerimos con la dieta se dirige prácticamente todo a la glándula tiroides. Una vez allí, entra a los tirocitos en su forma ionizada (I-) por la membrana basal gracias a la acción de una proteína transportadora llamada NIS (Natrium-Iodide Symporter).
- El yodo sale del tirocito por la membrana apical mediante la ayuda de otra proteína llamada pendrina.
- El yodo es oxidado por la enzima tiroperoxidasa (TPO).
- La misma enzima, la TPO, incorpora el yodo al aminoácido tirosina para formar 3-monoiodotirosina (MIT) o diiodotirosina (DIT).
- La enzima tiroperoxidasa (TPO), también permite la unión de dos diiodotirosina para formar la hormona tiroxina. Para la formación de la hormona triiodotironina se necesita la unión de una molécula MIT con una molécula DIT, también mediante la catálisis de la enzima TPO.
Cuando están sintetizadas, las hormonas van a parar al torrente sanguíneo donde se transportan hasta los tejidos donde ejecutan su función.
Enfermedades relacionadas con el metabolismo de la tirosina
Tirosinemias
Consiste en una acumulación y/o excreción de la tirosina y de sus metabolitos como consecuencia de la ausencia o la deficiencia de la enzima tirosina aminotransferasa. Hay diversos tipos: tirosinemia hepatorrenal o de tipo I y tirosinemia oculocutánea o de tipo II. Ambas enfermedades son autosómicas recesivas. El tipo I se trata de una disfunción de los túbulos renales, raquitismo y polineuropatía. Está causada por la falta de fumarilacetoacetato hidrolasa. La acumulación de fumarilacetoacetato y maleilacetato conduce a la alquilación del ADN y a la generación de tumores. El tipo II produce lesiones en los ojos y en la piel. Además de un retraso mental.
Alcaptonuria
Es una enfermedad que padecen las personas que tienen una deficiencia en homogentisato oxidasa, las cuales excretan casi toda la tirosina que ingieren en su forma de ácido homogentísico mediante la orina. En los primeros años de vida, la única consecuencia de la enfermedad es un color oscuro de la orina. Pero conforme se van acumulando en los huesos y el tejido conjuntivo los pigmentos que se forman en la oxidación del homogentisato, se puede producir ocronosis. También se trata de una enfermedad autosómica recesiva. Además se ve inhibida debido a la glucólisis heterolítica sintota que se origina en poseedores de VIH.
Albinismo
Consiste en una condición genética que se caracteriza por el hecho de que la piel y el cabello están poco o nada pigmentados. Se produce por la falta de una enzima llamada tirosinasa , la cual actúa en el proceso de formación de melanina a partir de tirosina. La falta de pigmentos en la piel causa a los albinos más sensibilidad a las radiaciones solares. Esta se puede manifestar como quemaduras en la piel y/o carcinomas. Además la falta de pigmentación en los ojos contribuye a la fotofobia.
Parkinson
Se trata de una enfermedad que acostumbra a afectar a población de más de 60 años de edad, aunque también se ha observado en población más joven. Consiste en unos temblores que de forma gradual van interfiriendo en la función motora de diversos grupos musculares. El defecto que causa esta enfermedad es la pérdida progresiva de neuronas dopaminérgicas presentes en una zona del cerebro llamada substantia nigra y en el locus coeruleus del cerebro. Está relacionada con el aminoácido tirosina ya que su hidroxilación lo transforma en DOPA que a su vez por carboxilación se convierte en el neurotransmisor dopamina.
La fosforilación de la tirosina
La tirosina puede sufrir una fosforilación en su grupo hidroxilo (-OH) a causa de la acción de numerosas enzimas del tipo tirosina quinasa. Estas enzimas están implicadas en la transducción de señales y en la regulación de la actividad enzimática ya que se conoce que la fosforilación de residuos de tirosina tiene la capacidad de activar o inhibir enzimas y receptores.
La sulfatación de la tirosina
El aminoácido también puede sulfatarse. Se trata de una modificación postraduccional que solo se produce en aquellas proteínas que pasan a través del aparato de Golgi y que se van a secretar al exterior o que tienen algún dominio extracelular. La enzima que se encarga de catalizar el proceso de sulfatación se llama proteintirosil sulfotransferasa, la cual se encuentra en la membrana del aparato de Golgi con su sitio activo orientado hacia el lumen de este compartimento. El donante de grupos sulfatos en esta reacción es el 3’fosfoadenosina-5’-fosfosulfato. La sulfatación es una modificación que afecta a las actividades biológicas de los neuropéptidos, al proceso de proteólisis de proteínas precursoras y al transporte intracelular de proteínas secretoras. Fundamentalmente reforzaría las interacciones proteína-proteína. Se conoce que la gastrina y la colecistoquinina poseen una tirosina sulfatada, lo cual aumenta considerablemente la potencia de ambas hormonas.
La tirosina como terapia
La tirosina se utiliza terapéuticamente en algunos casos de depresión y estrés. También se usa en pacientes esquizofrénicos, ya que se ha visto que en estas personas el transporte de tirosina en los fibroblastos de la piel es más reducido.
Referencias
- DEVLIN, T. Bioquímica, libro de texto con aplicaciones clínicas. Editorial Reverté. 4ª edición. Barcelona. 2006.
- NELSON, D. y COX, M. Lehninger, principios de bioquímica. Editorial Omega. 4.ª edición. Barcelona. 2006.
- STRYER, L., BERG J. y TYMOCZKO, J. Bioquímica. Editorial Reverté. 5ª edición. Barcelona. 2004.
- HAWLEY. Diccionario de química y de productos químicos. Traducción: GARCÍA, L. y TULLA, R. Editorial Omega. Barcelona. 2006.
- VOLLHARDT, C. y SCHERE, E. Química orgánica. Estructura y función. Editorial Omega. Barcelona. 2005.
- ALBIR, M., SERRA, A. y CHICOTE, J. Gran Vox: diccionario químico. Editorial Spes. Barcelona. 2003.
- VOET, D. y VOET, J. Bioquímica. Editorial Omega. Barcelona 1992.
- Video de Pilar Santiesteban: http://tv.uvigo.es/es/serial/180.html