Nitratos orgánicos
Los nitratos orgánicos se han reconocido como eficaces vasodilatadores por más de cien años. La nitroglicerina es el medicamento más conocido y estudiado de este grupo y sigue siendo hasta el día de hoy el mejor apoyo terapéutico para combatir la angina de pecho clásica.
Descripción
Los nitratos y nitritos orgánicos son en realidad profármacos que pertenecen al grupo de los fármacos llamados nitrovasodilatadores. Deben metabolizarse (reducirse) a fin de producir óxido nítrico, que es el principio activo de esta clase de compuestos.
Tipos de nitratos orgánicos
- El nitrito de amilo es un líquido muy volátil que debe administrarse por inhalación y su utilidad terapéutica es limitada.
- Los nitratos orgánicos de masa molecular baja (como la nitroglicerina) son líquidos oleosos, moderadamente volátiles. En la forma pura (sin un portador inerte como la lactosa), la nitroglicerina es explosiva.
- Los ésteres de nitrato de masa molecular alta (tetranitrato de eritritilo, dinitrato de isosorbida y mononitrato de isosorbida) son sólidos.
Estos medicamentos tienen un efecto vasodilatador selectivo en la vasculatura coronaria epicárdica y pueden incrementar la función del ventrículo tanto sistólica como diastólica por un aumento del flujo coronario; aún hay controversias sobre la relevancia clínica de este efecto vasodilatador coronario en pacientes con obstrucción coronaria epicárdica.
Propiedades químicas
Los nitratos orgánicos son ésteres de poliol del ácido nítrico, en tanto que los nitritos orgánicos son ésteres del ácido nitroso. Los ésteres de nitrato (—C—O—NO2) y nitrito (—C—O—NO) se caracterizan por una secuencia de carbono-oxígeno-nitrógeno, en tanto los compuestos nitro poseen enlaces de carbono-nitrógeno (C—NO2). Así, el trinitrato de glicerilo no constituye un compuesto nitro y se denomina de manera errónea nitroglicerina; sin embargo, esta nomenclatura está difundida y es oficial.[1]
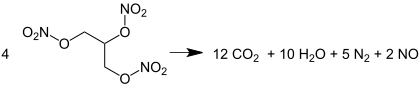
La descomposición térmica de los ésteres de nitrato produce principalmente los gases moleculares nitrógeno (N2) y dióxido de carbono. La energía química de la detonación es considerable debido a la alta resistencia del enlace en nitrógeno molecular. Esta estequiometría se ilustra mediante la ecuación para la detonación de nitroglicerina.
El Si(CH2ONO2)4 es considerado uno de los nitratos más sensibles a la detonación.[2][3] Un solo cristal de este compuesto detona incluso en contacto con una espátula de teflón y esta cualidad hizo imposible la caracterización completa. Otro factor que contribuye a su descomposición exotérmica (inferida de una experimentación mucho más segura in silico) es la capacidad del silicio en su fase cristalina para coordinar a dos grupos de nitrito de oxígeno además de la coordinación regular a los cuatro átomos de carbono. Esta coordinación adicional haría más fácil la formación de dióxido de silicio (uno de los productos de descomposición).
Síntesis
Los ésteres de nitrato se preparan típicamente por condensación de ácido nítrico y el alcohol:[4] Por ejemplo, el éster de nitrato más simple, nitrato de metilo, se forma por reacción de metanol y ácido nítrico en presencia de ácido sulfúrico:[5]
- CH3OH + HNO3 → CH3ONO2 + H2O
Esta condensación es denominada en algunas ocasiones como "nitroxilación".
Ventajas
Los nitratos poseen los beneficios de poder reducir la precarga y la poscarga en varios trastornos cardiacos. Se dispone de varios preparados en distintas formas farmacéuticas de nitroglicerina y de otros nitratos lo que se agrega al arsenal médico para extender y mejorar la utilidad clínica. Los preparados de nitrato son medicamentos relativamente seguros y eficaces cuya principal acción en el tratamiento de la insuficiencia cardíaca congestiva es una reducción de las presiones de llenado del ventrículo izquierdo. Esta disminución de la precarga se debe a un aumento en la capacitancia venosa periférica. Los nitratos originarán una merma de las resistencias vasculares pulmonar y periférica, en particular a las dosis más altas, aunque esta respuesta es menos notable y predecible que con el nitroprusiato.
Farmacología
La principal propiedad farmacológica de los nitratos es la relajación del músculo liso vascular, produciendo vasodilatación.[6] Los efectos farmacológicos más comunes ocurren en las venas, aunque la nitroglicerina produce dilatación vascular en venas y arterias variando así con la dosis. La reducción de la resistencia periférica venosa produce una acumulación de sangre venosa y disminución del retorno venoso hacia el corazón (precarga); la reducción de la resistencia arteriolar disminuye la resistencia vascular sistémica y la presión arterial (poscarga).
Mecanismo de acción
El óxido nítrico activa la isoforma soluble de guanililciclasa, e incrementa en consecuencia las concentraciones intracelulares de guanosín monofosfato cíclico (GMP cíclico). A su vez, ello promueve la desfosforilación de la cadena ligera de miosina y la disminución del (Ca2+) citosólico y conduce a la relajación de células de músculo liso en una gama amplia de tejidos. La relajación del músculo liso vascular dependiente del óxido nítrico origina vasodilatación; la activación de guanililciclasa mediada por óxido nítrico inhibe la agregación plaquetaria y relaja el músculo liso en los bronquios y el tubo digestivo.[7]
Importancia biomédica
La respuesta biológica amplia a los nitrovasodilatadores sugiere la existencia de vías endógenas reguladoras moduladas por óxido nítrico; más de un siglo después del uso terapéutico de nitrovasodilatadores, se aislaron y caracterizaron las enzimas que tienen a su cargo la síntesis endógena de óxido nítrico, que en el ser humano se cataliza por una familia de sintasas de óxido nítrico que oxidan el aminoácido L-arginina para formar óxido nítrico (más L-citrulina como un coproducto).[8]
Existen tres isoformas de sintasa de óxido nítrico en mamíferos distintas denominadas nNOS, eNOS e iNOS y participan en procesos tan diversos como neurotransmisión, vasomotilidad e inmunomodulación. Al parecer, en varios estados patológicos vasculares están alteradas las vías endógenas de regulación dependientes del óxido nítrico.[9]
Mecanismos de acción
Los nitratos orgánicos (contando los nitritos, los compuestos nitrosos y una diversidad de otras sustancias que contienen óxido de nitrógeno dentro de los que se incluye el nitroprusiato; originan la formación del radical libre reactivo óxido nítrico. Aún se investiga de manera activa el mecanismo exacto de la desnitración de nitratos orgánicos para liberar óxido nítrico.
El óxido nítrico activa la guanililciclasa, aumenta la concentración celular de GMP cíclico, activa la PKG (cinasa de proteína dependiente de GMP cíclico) y regula las actividades de las fosfodiesterasas de nucleótidos cíclicos (PDE 2, 3 y 5) en una diversidad de tipos celulares.[10]
Efectos cardiovasculares
Efectos hemodinámicos. Los nitrovasodilatadores promueven la relajación del músculo liso vascular. Dosis altas de nitratos orgánicos causan mayor estancamiento venoso y también pueden disminuir la resistencia arteriolar y reducir en consecuencia las presiones arteriales sistólica y diastólica y el gasto cardíaco y originar palidez, debilidad, mareo y activación de reflejos simpáticos compensadores. Los efectos farmacológicos mencionados anteriormente, conducen a la disminución del consumo de oxígeno por el miocardio, lo que promueve una relación mejorada de aporte y consumo de oxígeno. En la circulación coronaria, los nitratos redistribuyen el flujo sanguíneo circulante a lo largo de los conductos colaterales e incrementan el riego sanguíneo debajo del endocardio optimizando el flujo al miocardio con isquemia.
Otros efectos
Los nitrovasodilatadores actúan sobre casi todo el músculo liso. Hay relajación del músculo liso bronquial, sin importar la causa del tono preexistente. Se observa relajación eficaz de los músculos de las vías biliares, incluso los de la vesícula biliar, conductos biliares y el esfínter de Oddi. Los nitratos tal vez relajen el músculo liso del tubo digestivo, incluso el del esófago, y quizá disminuyan su motilidad espontánea tanto in vivo como in vitro. El efecto puede ser transitorio e incompleto in vivo, pero el “espasmo” anormal suele reducirse. En realidad, muchos ataques de dolor retroesternal atípico y “angina” se deben a espasmo biliar o esofágico, y esos también se alivian mediante nitratos. De modo similar, los nitratos relajan el músculo liso ureteral y uterino, pero estos efectos tienen importancia clínica incierta.[11]
Véase también
- El uso de la nitroglicerina en la terapéutica.
Referencias
- Goodman Gilman, Alfred; Theodore W. Rall, Alan S. Nies, Palmer Taylor (1991). Goodman And Gilman's The Pharmacological Basis Of Therapeutics (8ª edición). USA: Pergamon Press. p. 752. ISBN 0-02-946568-0.
- The Sila-Explosives Si(CH2N3)4 and Si(CH2ONO2)4: Silicon Analogues of the Common Explosives Pentaerythrityl Tetraazide, C(CH2N3)4, and Pentaerythritol Tetranitrate, C(CH2ONO2)4Thomas M. Klapötke, Burkhard Krumm, Rainer Ilg, Dennis Troegel, and Reinhold Tacke J. Am. Chem. Soc.; 2007 doi 10.1021/ja071299p
- Sila-Explosives Offer A Better Bang Stephen K. Ritter Chemical & Engineering News May 7 2007Link
- Snyder, H. R.; Handrick, R. G.; Brooks, L. A. (1942). "Imidazole". Org. Synth.; Coll. Vol. 3: 471.
- Alvin P. Black and Frank H. Babers. "Methyl nitrate". Org. Synth.; Coll. Vol. 2: 412.
- Patiño, Nicandro Mendoza (23 de junio de 2008). Farmacologia medica / Medical Pharmacology. Ed. Médica Panamericana. ISBN 9789687988443. Consultado el 27 de diciembre de 2017.
- Molina, C.; Andresen, J.W., Rapoport, R.M., Waldman, S.A., and Murad, F. (1987). «Effect of in vivo nitroglycerin therapy on endothelium dependent and independent vascular relaxation and cyclic GMP accumulation in rat aorta». J. Cardiovasc. Pharmacol. 10: 371-378.
- Goodman Gilman, Alfred; Laurence L. Brunton, John S. Lazo, Keith L. Parker (2006). Goodman And Gilman's The Pharmacological Basis Of Therapeutics (11ª edición). México: The McGraw-Hill. pp. 824-825. ISBN 0-07-142280-3.
- Lowenstein, C.J.; Dinerman, J.L., y Snyder, S.H. (1994). «Nitric oxide: A physiologic messenger.». Ann. Intern. Med. 120: 227-237.
- Beavo, J.A.; Conti, M., Heaslip, R.J. (1994). «Multiple cyclic nucleotide phosphodiesterases». Mol. Pharmacol. 46: 399-405.
- Münzel, T.; Kurz, S., Heitzer, T., Harrison, D.G. (1996). «New insights into mechanisms underlying nitrate tolerance.». Am. J. Cardiol. 77 (24C–30C).