Myxobolus cerebralis
Myxobolus cerebralis es un mixozoo, de la clase Myxosporea, parásito de los salmónidos (salmones, truchas y afines) que causa la enfermedad del torneo en las poblaciones salvajes de peces y también en las piscifactorías. Se describió por primera vez en la trucha arcoíris en Alemania hace un siglo, pero su distribución se ha ampliado y está presente en la mayor parte de Europa y las demás zonas templadas del planeta.[1] En los años 1980 se descubrió que M. cerebralis necesita infectar a un oligoqueto tubifícido (una clase de gusano segmentado) para completar su ciclo vital.[2] El parásito infecta a sus huéspedes por medio de sus cápsulas polares, similares a los cnidoblastos, que inoculan sus células tras haber perforado los epitelios con sus filamentos polares.
| Myxobolus cerebralis | ||
|---|---|---|
 Myxobolus cerebralis en estado actinospora. | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Cnidaria | |
| (sin rango): | Myxozoa | |
| Clase: | Myxosporea | |
| Orden: | Bivalvulida | |
| Familia: | Myxobolidae | |
| Género: | Myxobolus | |
| Especie: |
M. cerebralis Hofer, 1903 | |
| Distribución | ||
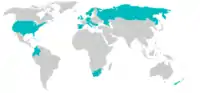 Distribución de Myxobolus cerebralis. | ||
| Sinonimia | ||
Myxosoma cerebralis | ||
La enfermedad del torneo afecta a los peces jóvenes (alevines y juveniles) y les causa deformaciones en el esqueleto y daños neurológicos, por lo que los peces avanzan torpemente girando como un sacacorchos en lugar de nadar normalmente, por lo que tienen dificultades para conseguir alimento y son más vulnerables a los depredadores. La tasa de mortalidad es alta para los alevines, superior al 90% de los infectados, y los que consiguen sobrevivir quedan deformados por el parásito que permanece en sus huesos y cartílagos, que actúan como reserva del parásito, que se liberará en el agua tras la muerte del pez. M. cerebralis es el mixozoo patógeno que causa mayores daños económicos. Es el primer myxosporeo del cual se describió su patología y síntomas.[3] Este parásito no es capaz de infectar a los humanos.
Taxonomía
La taxonomía y denominación, tanto de M. cerebralis como las de los mixozoos en general, han sido históricamente complicadas. Originalmente se pensó que este parásito infectaba el cerebro de los peces (de ahí su nombre específico cerebralis), aunque pronto se descubrió que aunque aparecía en el sistema nervioso principalmente infectaba el cartílago y el tejido óseo. También se describió como Myxobolus chondrophagus, que describía más adecuadamente al organismo (chondrophagos en griego significa comedor de cartílago), pero finalmente se asignó el primer nombre como las normas de la nomenclatura binomial establecen.[1] Más tarde se descubrió que los organismos anteriormente denominados Triactinomyxon dubium y T. gyrosalmo (clase Actinosporea) eran en realidad los estadios de actinospora de M. cerebralis, que tiene un ciclo vital complejo.[4] De forma similar los demás actinosporeos se incorporaron a otros ciclos vitales de varios myxosporeos.
En la actualidad los mixozoos son considerados animales por muchos científicos, si bien con anterioridad se los clasificaba como protozoarios multicelulares, aunque su estatus no ha cambiado oficialmente. Estudios moleculares recientes sugieren que están relacionados tanto con los bilaterales como con los cnidarios, siendo los cnidarios los más próximos morfológicamente ya que ambos grupos tienen filamentos proyectables,[5] aunque genéticamente estarán algo más próximos a los bilaterales.[6]
Morfología
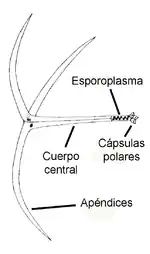
Myxobolus cerebralis tiene varios estados diferentes según sus etapas de desarrollo, que van desde simples células a esporas relativamente grandes, no todas de ellas estudiadas en detalle.
Estado de actinospora
El estado que nada en el agua e infecta a los peces, llamado actinospora, está compuesto por un cuerpo alargado simple de unos 150 micrómetros (µm) de largo y con tres apéndices o "colas" que miden cada uno unos 200 micrómetros. Tiene un paquete de esporoplasma al final de su cuerpo alargado que contiene 64 células germinales rodeadas por una envoltura celular.[5] Además hay tres cápsulas polares, cada una de las cuales contiene un filamento polar enrollado que mide entre 170 y 180 µm.[2] Los filamentos polares se disparan rápidamente dentro del cuerpo del huésped tanto en este estado como en el de mixospora, creando una apertura por la que el esporoplasma puede entrar e infectar al huésped.
Estado de esporoplasma
Una vez en contacto con el pez o el gusano huésped sale de la cápsula polar y el esporoplasma que estaba dentro del cuerpo central de la espora migra dentro de la piel o el recubrimiento de los intestinos. Al principio este esporoplasma sufre mitosis para producir más células ameboides que migran hacia capas de tejido más internas, hasta encontrar el cartílago cerebral de los peces.[2]
Estado de mixospora
La mixoespora es el estado que puede infectar a los oligoquetos, y se encuentran entre los restos digeridos de cartílagos de peces y se liberan al agua con su muerte. Las mixosporas, que se desarrollan a partir de células del esporoplasma dentro de los peces huéspedes, son lenticulares. Tienen un diámetro de unos 10 micrómetros y constan de seis células. Dos de estas células forman la cápsula polar, dos surgen para formar un esporoplasma binucleado y dos forman válvulas de protección.[5] Son a menudo difíciles de distinguir de los de especies afines porque son morfológicamente muy similares en todos los géneros. Aunque M. cerebralis sólo se ha encontrado como mixospora en el cartílago de los salmónidos, otras especies visualmente similares pueden estar presentes en la piel, el sistema nervioso y los músculos.[2]
Ciclo de vida
.png.webp)
Myxobolus cerebralis tienen un ciclo de vida que necesita de dos huéspedes, los peces de la familia de los salmónidos y un oligoqueto acuático de la familia de los tubifícidos. El único gusano conocido susceptible de ser infectado por M. cerebralis es Tubifex tubifex,[2] aunque lo que los científicos llaman hasta ahora T. tubifex podría ser más de una especie.[3]
En primer lugar las mixosporas que se encuentran entre los detritos de los sedimentos son ingeridas por los gusanos tubifícidos, estas mixosporas provienen de la descomposición de peces muertos o de las heces de los depredadores que han comido peces infectados. Una vez ingeridas, en el lumen del intestino del gusano, las esporas proyectan sus cápsulas polares y se sujetan a los epitelios intestinales por medio de los filamentos polares. La cubierta de las válvulas entonces se abren por la línea de sutura y las células germinales binucleadas del esporoplasma penetran entre las células del epitelio intestinal del gusano. Estas células se multiplican, produciendo muchas células ameboides por un proceso de multiplicación asexual de fisión celular denominado merogonia. En la merogonia entre 5 y 25 días, las células ameboides binucleadas dan lugar a muchas células uni- o binucleadas que se someten a múltiples divisiones para producir numerosas células hijas, este ciclo puede continuar a lo largo del desarrollo del parásito, proporcionando un reservatorio de células que pueden contribuir a la gametogonia y la esporogonia,[7] como resultado de este proceso de multiplicación los espacios intercelulares de las células epiteliales de más de diez segmentos vecinos del gusano pueden quedar infectadas.[8]
Entre 25 y 46 días, en la gametogonia las células binucleadas ovales dan lugar a pansporoquistes a través de múltiples divisiones, el pansporocito consta de células somáticas surredondeando dos células generativas. las células somáticas se dividen para formar la pared del pansporoquiste, mientras que las dos células generativas se dividen en más para formar gametocitos que se diferencian aun más en alfa haploide y gametocitos beta, las divisiones meióticas que dan el ascenso a los gametos son la única fase en el ciclo de vida donde existe en un estado haploide. para la formación de un cigoto de forma sexual, se necesita de la fusión de alfa y beta.
A partir de los 50 días de la fusión de los gametocitos, se pueden observar que dentro de cada pansporocito se forman ocho cigotos. Cada cigoto se divide para formar cuatro células esporoblásticas. Entre 60 y 90 días después de la infección las células sexuales del parásito sufren la esporogénesis y se desarrollan los esporocistos, cada uno de los cuales contiene ocho actinosporas. Estas esporas son liberadas al agua a través del ano del oligoqueto. Los tubifícidos infectados pueden liberar actinosporas al menos durante un año.[8] Las actinosporas liberadas de este modo pueden nadar e infectar a los peces penetrando a través de su piel. Los peces también pueden infectarse al ingerir un tubifícido infectado.[5]
La actinospora infecta al pez inoculándole con sus filamentos polares, que están en unas cápsulas similares a los cnidoblastos, que penetran en la piel y expulsan células en interior del pez. El proceso de penetración de estas esporas en un pez dura sólo unos segundos. En cinco minutos un saco de células germinales denominado esporoplasma penetra la epidermis, y en unas pocas horas, el esporoplasma se divide en células individuales que se diseminan por todo el pez.[5]
En el interior del pez se producen tanto etapas intracelulares como extracelulares, reproduciéndose en su cartílago por multiplicación asexual. El estado final del parásito dentro del pez es la mixospora, que se forma por esporogonia en los cartílagos del hospedante. Allí las mixosporas se van acumulando hasta que el pez muere. Se liberan al medio cuando el pez se descompone o es devorado.[5] Algunos estudios recientes indican que algunos peces expelen mixosporas viables mientras están todavía vivos.[9]
Las mixosporas son extremadamente resistentes. Se ha visto que esta forma de espora de Myxobolus cerebralis pueden tolerar la congelación a -20 °C al menos durante 3 meses, aguantan en barro a 13 °C al menos 5 meses y pueden pasar a través de los intestinos de un lucio o un pato sin perder su poder infeccioso para los gusanos.[10] Las actinosporas tienen una vida más corta, sobreviviendo menos de 34 días, dependiendo de la temperatura.[11]
El ciclo se cierra cuando las mixosporas son liberadas por descomposición tras la muerte del pez o por medio de los excrementos de los depredadores que comieron algún salmónido infectado, se depositan en los sedimentos del río y son ingeridas de nuevo por un gusano que resulta infectado.[5]
Patología

Se han registrado infecciones de M. cerebralis en una gran variedad de especies de salmónidos: 8 especies de salmónidos atlánticos, Salmo; 4 especies de salmónidos del pacíficos, Oncorhynchus; 4 especies de truchas Salvelinus; el tímalo, Thymallus thymallus; y el hucho, Hucho hucho.[12] M. cerebralis causa daños en los peces por la adhesión de las actinosporas a los tejidos y la migración de sus distintos estados a través de los nervios, además de por la digestión de los cartílagos.[5] La cola del pez suele oscurecerse, pero aparte de las lesiones en el cartílago, el resto de los órganos internos generalmente parecen sanos.[2] Otros síntomas son las deformaciones esqueléticas y el comportamiento giratorio (persiguiéndose la cola) en los peces jóvenes, que se pensó que era causado por la pérdida del sentido del equilibrio, pero que en realidad se debe al daño en la espina dorsal y la base del cráneo.[3] Se han realizado experimentos que han demostrado que los peces pueden matar a los Myxobolus en su piel (posiblemente por medio de anticuerpos), pero que el pez es incapaz de atacar a los parásitos una vez que han llegado a su sistema nervioso central. La magnitud de la respuesta inmunitaria varía dependiendo de las especies.[3]
La liberación de actinosporas por la pared intestinal del gusano T. tubifex daña su mucosa, ya que esto puede ocurrir miles de veces en un solo gusano, y se cree que puede perjudicar la absorción de nutrientes.[5] Además, los gusanos infectados tienen una masa corporal más baja y pueden estar decolorados.[3] Las esporas se liberan del gusano casi exclusivamente cuando la temperatura se encuentra entre 10 °C y 15 °C, así que los peces en aguas más cálidas o más frías tienen menos probabilidad de resultar infectados, y las tasas de infección son estacionales.[3]
Susceptibilidad
El tamaño del pez y su edad, la concentración de actinosporas y la temperatura del agua influyen en las tasas de infección en los peces, además de la especie del pez en cuestión.[13] La enfermedad tiene mayor impacto en peces de menos de cinco meses de edad porque su esqueleto no se ha osificado todavía. Esto hace a los peces jóvenes más susceptibles a las deformidades,[14] al proporcionarle al M. cerebralis más cartílago del que alimentarse.[3] En un estudio sobre siete especies de salmónidos y muchas de sus razas, la trucha salmonada y la trucha arcoíris (excepto una variedad) fueron de lejos las que resultaron más seriamente afectadas por M. cerebralis tras dos horas de exposición. Mientras que las otras especies, la trucha toro, el salmón chinuc, la trucha común y el tímalo ártico fueron mucho menos afectados.[13] Además la trucha común puede portar el parásito sin mostrar ningún síntoma, ya que esta especie posiblemente era el huésped original de M. cerebralis' y se ha adaptado a él.[15] Debido a esta ausencia de síntomas de la trucha común el parásito no fue descubierto hasta que las truchas arcoíris fueron introducidas en Europa.[3]
Diagnóstico

Las infecciones clínicas moderadas y graves de los peces con enfermedad del torneo puede ser diagnosticadas por los cambios del comportamiento de los peces que aparecen entre los 35 y 80 días después de la infección inicial, aunque algunas heridas o la deficiencia de triptófano y ácido ascórbico en la dieta pueden producir síntomas similares, así que el diagnóstico definitivo requiere encontrar myxosporas en el cartílago de los peces.[2] En las infecciones severas al examinar los cartílagos al microscopio aparecerán las lesiones y las esporas.[2] En infecciones menos severas la prueba implica primero la digestión del cartílago craneal con las proteasas pepsina y tripsina para poder ver las esporas. La cabeza y otras tejidos pueden ser examinados posteriormente histopatológicamente para confirmar que la localización y la morfología de las esporas concuerdan con las de M. cerebralis. También es posible la identificación serológica de las esporas en secciones de tejido usando el anticuerpo producido contra las esporas. La identificación del parásito también puede ser confirmada mediante el uso de la reacción en cadena de la polimerasa para amplificar las 415 pares de bases del gen del ARN ribosomal 18S de M. cerebralis.[16] Los peces deben revisarse en las etapas de la vida más susceptibles al parásito, es decir las iniciales. Las revisiones rutinarias usando estas técnicas se llevan a cabo tanto en los países donde ya hay parásitos como en algunos donde todavía no se han registrado, como Australia y Canadá donde no han aparecido pero una posible introducción podría amenazar a los peces locales.
Impacto
Aunque originalmente era un patógeno leve de la trucha común en Europa central y otros salmónidos de Asia nororiental, la expansión de la trucha arcoíris ha incrementado la tasa de impacto del parásito. Al no tener una inmunidad innata al M. cerebralis las truchas arcoíris son particularmente susceptibles a la infección y pueden liberar tantas esporas que incluso especies resistentes de la misma área, como S. trutta, resultan sobrecargadas por los parásitos produciendo mortalidades de entre el 80% y el 90%. Donde M. cerebralis se encuentra bien establecido puede causar el declive o incluso la eliminación de poblaciones enteras de peces.[17][18]
Se han registrado infecciones producidas por M. cerebralis en Alemania (1893), Italia (1954), la URSS (1955), incluyendo la isla de Sajalín (1960), EE. UU. (1958), Bulgaria (1960), Yugoslavia (1960), Suecia (1966), Sudáfrica (1966), Escocia (1968), Nueva Zelanda (1971), Ecuador (1971), Noruega (1971), Colombia (1972), Líbano (1973), Irlanda (1974), España (1981) e Inglaterra (1981).
Impacto en Europa
El impacto de M. cerebralis en Europa es un tanto menor por el hecho que la especie es endémica de esta región lo que da a las poblaciones de salmónidos nativos un grado de inmunidad. En cambio la trucha arcoíris, la especie más susceptible a este parásito, no es nativa de Europa. Las poblaciones de trucha arcoíris introducidas que se reproducen con éxito son raras, posiblemente a causa del parásito, así que hay pocas truchas arcoíris jóvenes salvajes susceptibles a la infección. Pero el riesgo está en las piscifactorías donde se crían con destino a la repoblación de las aguas para la pesca o el consumo humano, donde el parásito ocasiona perjuicios. Se han probado con éxito métodos de incubación y cría diseñados para prevenir las infecciones en los alevines de trucha arcoíris en Europa. Estas técnicas consisten en la incubación de huevos usando aguas libres de esporas y la cría de los alevines hasta la etapa de osificación en tanques o canales aislados. En estos métodos se presta particular atención a la calidad de las fuentes de agua para prevenir la introducción de esporas durante los intercambios de agua.[19] Los jóvenes sólo se trasladan a piscinas con pilas con tierra cuando se considera que son clínicamente resistentes al parásito, cuando ya se ha producido la osificación de su esqueleto.[14]
Impacto en los Estados Unidos
La presencia de M. cerebralis se registró por primera vez en Norteamérica en 1956, en Pensilvania. Se introdujo por medio de truchas importadas de Europa y se extendió sin freno hacia el sur y el oeste.[21] Hasta los años 1990 la enfermedad del torneo se consideró un problema controlable que afectaba solo a las piscifactorías de trucha arcoíris. Hasta que se estableció en la naturaleza en las aguas de los estados de las Montañas Rocosas (Colorado, Wyoming, Utah, Montana, Idaho, Nuevo México) donde causó grandes mortalidades en muchos ríos pesqueros. Algunos arroyos del oeste de EE. UU. perdieron el 90% de sus truchas.[22] Además la enfermedad amenazó la pesca recreativa, que es una importante fuente de turismo, una industria clave en algunos estados del oeste. Por ejemplo la Montana Whirling Disease Task Force (fuerza operativa contra la enfermedad del torneo de Montana) estimó que la pesca de trucha generaba unos ingresos de 300 000 000 $ sólo en Montana.[3] El peor problema es que algunos de los peces que infecta M. cerebralis ya se encontraban en situación de amenaza o peligro de extinción, como la trucha toro, la trucha de garganta cortada y la variedad anádroma de la trucha arcoíris, la cabeza plateada, empeorando el parásito la ya precaria situación de las especies.[3] Por razones poco entendidas, pero que probablemente tienen que ver con las condiciones ambientales, la infección ha tenido más impacto en Colorado y Montana y menor en California, Míchigan y Nueva York.[23]
Impacto en Nueva Zelanda
Se encontró por primera vez M. cerebralis en Nueva Zelanda en 1971. El parásito sólo se encontró en ríos de la isla Sur, lejos de los emplazamientos de acuicultura más importantes. Además las especies de salmónidos criados comercialmente aquí tienen poca susceptibilidad a la enfermedad del torneo y no se ha observado que afecte a los salmónidos nativos.[24] Aunque ha producido una consecuencia comercial indirecta, la imposición de una cuarentena que restringe la exportación de productos del salmón a la vecina Australia.
Prevención y control
Algunos biólogos han intentado combatir a las actinosporas haciendo que descarguen sus armas prematuramente. En el laboratorio, sólo en condiciones extremas de acidez o basicidad, condiciones relativamente altas de sal o corrientes eléctricas consiguen la descarga prematura de los filamentos. El uso de neuroquímicos, los quimiosensibilizadores de cnidarios y el mucus de trucha no han sido efectivos,[25] como lo fueron los peces anestesiados o muertos.[26] Si las esporas pudieran ser desarmadas, serían incapaces de infectar al pez, pero no está claro si estos métodos de laboratorio podrían ser utilizados en la naturaleza.
Algunas variedades de peces son más resistentes que otras, incluso dentro de la misma especie,[13] usando las variedades más resistentes se puede reducir la incidencia y gravedad de la enfermedad en la acuicultura. También hay algunas pruebas circunstanciales de que las poblaciones naturales pueden desarrollar cierta resistencia con el tiempo.[27] Además los acuicultores pueden evitar la infección de M. cerebralis dejando de usar piscinas de tierra al criar a los alevines, esto les mantiene lejos del peligro de entrar en contacto con tubifícidos infectados y hace más fácil eliminar las esporas por filtración, cloración y radiación ultravioleta de las aguas.[2] Para eliminar la población de tubifícidos se pueden desinfectar las incubadoras y las piscinas, y engordar a los alevines de trucha en instalaciones cubiertas con agua libre de patógenos. Los canales y piscinas de hormigón liso o recubiertos de plástico que se mantienen limpias y libres de aguas contaminadas son las mejores instalaciones para evitar la enfermedad.[2]
Por último algunos medicamentos como el furazolidona, furoxona, benomyl, fumagilina, proguanil y clamoxiquina han demostrado que impiden el desarrollo de las esporas, lo que reduce las tasas de infección.[2] Por ejemplo un estudio muestra que al administrar fumagillin con la comida de las Oncorhynchus mykiss se reduce el número de peces infectados de entre el 73% y 100% a unas tasas del 10% al 20%.[10] Desafortunadamente este tratamiento no es posible para las poblaciones de truchas salvajes,[8] y ninguno de los medicamentos se ha mostrado lo suficientemente efectivo en las pruebas requeridas para ser aprobado por la FDA estadounidense.[3]
Los pescadores deportivos pueden ayudar a prevenir la extensión del parásito de varias formas. Limpiando sus equipos de pesca cuando viajen de una cuenca a otra y nunca llevar peces consigo para evitar el peligro de contaminación cruzada.[28] Las esporas son particularmente resistentes en la suela de las botas de agua, que deberían ser desinfectadas sumergiéndolas en una disolución al 10% de lejía en agua durante 15 minutos y después enjuagadas intensamente.[28] Nunca se deben arrojar los huesos y entrañas de los peces a los cauces de agua ya que pueden contaminarlos con esporas.[28] Además nunca se debe usar salmón o trucha como cebo.[28]
Referencias
- Bartholomew, J.L. and Reno, P.W. (2002). The history and dissemination of whirling disease. American Fisheries Society Symposium 29: 3–24.
- Markiw, M.E. (1992)). «Salmonid Whirling disease». Fish and Wildlife Leaflet 17: 1-3. Archivado desde el original el 27 de mayo de 2011.
- Gilbert, M. A. & Granath, W.O. Jr. (2003). Whirling disease and salmonid fish: life cycle, biology, and disease. Journal of Parasitology 89: 658–667.
- Kent, M. L., Margolis, L. & Corliss, J.O. (1994). The demise of a class of protists: taxonomic and nomenclatural revisions proposed for the protist phylum Myxozoa Grasse, 1970. Canadian Journal of Zoology 508: 932–937.
- Hedrick, R. P. & El–Matbouli, M. (2002). Recent advances with taxonomy, life cycle, and development of Myxobolus cerebralis in the fish and oligochaete hosts. American Fisheries Society Symposium 29: 45–53.
- Monteiro, A. S., Okamura, B. y P. W. H. Holland (2002). «Orphan worm finds a home: Buddenbrockia is a Myxozoan». Molecular Biology and Evolution 19: 968-971. Archivado desde el original el 11 de abril de 2005.
- Hedrick, R., Matbouli, M. (2002). «Recent advances with taxonomy, life cycle, and development of Myxobolus cerebralis in the fish and oligochaete hosts». American Fisheries Society Symposium. Consultado el 05-04-2022.
- El-Matbouli, M., and Hoffmann, R.W. (1998). Light and electron microscopic studies on the chronological development of Myxobolus cerebralis to the Actinosporean stage in Tubifex Tubifex. International Journal for Parasitology 28: 195–217.
- Nehring, R. B. Thompson, K. G. Taurman, K. A. & Shuler, D.L. (2002). Laboratory studies indicating that living brown trout Salmo trutta expel viable Myxobolus cerebralis myxospores. American Fisheries Society Symposium 29: 125–134.
- El-Matbouli, M., and Hoffmann, R.W. (1991). Effects of freezing, aging, and passage through the alimentary canal of predatory animals on the viability of Myxobolus cerebralis spores. Journal of Aquatic Animal Health 3: 260–262.
- Markiw, M.E. (1992). Experimentally induced whirling disease. II. Determination of longevity of the infective triactinomyxon stage of Myxobolus cerebralis by vital staining. Journal of Aquatic Animal Health 4 (1): 44–47.
- Lom, J. & Dyková, I. (1992). Protozoan Parasites of Fishes, Elsevier, Amsterdam. ISBN 0-444-89434-9.
- Vincent, E. R. (2002). Relative susceptibility of various salmonids to whirling disease with emphasis on rainbow and cutthroat trout.. American Fisheries Society Symposium 29: 109–115.
- Halliday, M.M. (1976). The Biology Of Myxosoma cerebralis: The Causative Organism Of Whirling Disease Of Salmonids. Journal of Fish Biology 9: 339–357.
- Hoffmann, G. (1962). Whirling Disease Of Trout. U.S. Department Of The Interior, Fishery Leaflet 508: 1–3.
- Andree, K.B., MacConnell, E. and Hedrick, R.P. (1998). A nested polymerase chain reaction for the detection of genomic DNA of Myxobolus cerebralis in rainbow trout Oncorhynchus mykiss. Diseases of Aquatic Organisms 34: 145–54.
- Nehring, R.B. (1996). Whirling Disease In Feral Trout Populations In Colorado. In E.P. Bergersen And B.A.Knoph (eds.), Proceedings: Whirling Disease Workshop––where Do We Go From Here? Colorado Cooperative Fish And Wildlife Research Unit, Fort Collins.: pp.159.
- Vincent, E.R. (1996). Whirling Disease—the Montana Experience, Madison River.. In, E.P. Bergersen And B.A.Knoph (eds.), Proceedings: Whirling Disease Workshop—where Do We Go From Here? Colorado Cooperative Fish And Wildlife Research Unit, Fort Collins.: pp.159.
- Ghittino, P. (1970). Present Status Of Whirling Disease In Italian Trout Farms. Riv. It. Piscic. Ittiopat 5: 89–92.
- «Whirling Disease Initiative». Archivado desde el original el 30 de junio de 2012.
- Bergersen, E.P., and Anderson, D.E. (1997). The distribution and spread of Myxobolus cerebralis in the United States. Fisheries 22 (8): 6–7.
- Tennyson, J. Anacker, T. & Higgins, S. (13 de enero de 1997). «Scientific breakthrough helps combat trout disease». U.S. Fish and Wildlife Service Whirling Disease Foundation News Release. Archivado desde el original el 16 de junio de 2005.
- Fish Health Advisory: Whirling Disease in Trout (PDF). Wisconsin Department of Agriculture, Trade and Consumer Protection. Division of Animal Health. octubre de 2001. Archivado desde el original el 26 de junio de 2004.
- Stone M A B, MacDiarmid S C, Pharo H J. (1997). Import health risk analysis: salmonids for human consumption (PDF). Ministry of Agriculture Regulatory Authority, New Zealand. Archivado desde el original el 13 de mayo de 2010. Consultado el 1 de diciembre de 2009.
- Wagner, E. J. Cannon, Q. Smith, M. Hillyard, R. & Arndt, R. (2002). Extrusion of Polar Filaments of the Myxobolus cerebralis Triactinomyxon by salts, electricity, and other agents. American Fisheries Society Symposium 29: 61–76.
- El-Matbouli, M., Hoffmann, R.W., Shoel, H., McDowell, T. S., & Hedrick, R.P. (1999). Whirling disease: host specificity and interaction between the actinosporean stage of Myxobolus cerebralis and rainbow trout (Oncorhynchus mykiss) cartilage. Diseases of Aquatic Organisms 35: 1–12.
- «Research on whirling disease resistant rainbow trout». Whirling Disease Foundation News. julio de 2003. Archivado desde el original el 31 de julio de 2007.
- Resumen del proyecto de especies introducidas: enfermedad del torneo (Myxobolus cerebralis) en la web de la universidad de Columbia (en inglés)
Enlaces externos
- Informe de la organización internacional de comercio sobre las restricciones de importación de salmón en Australia (en inglés)
- Fundación contra la enfermedad del torneo Archivado el 13 de mayo de 2005 en Wayback Machine. (en inglés)
- Iniciativa contra la enfermedad del torneo
- Mapa de la enfermedad del torneo y datos (en inglés)
