Reacción de Blaise
La reacción de Blaise es una reacción orgánica que forma un β-cetoéster a partir de la reacción del zinc con un α-bromoéster y un nitrilo.[1][2][3] El intermediario final es una metaloimina, la cual es hidrolizada para dar el β-cetoéster deseado.[4][5]
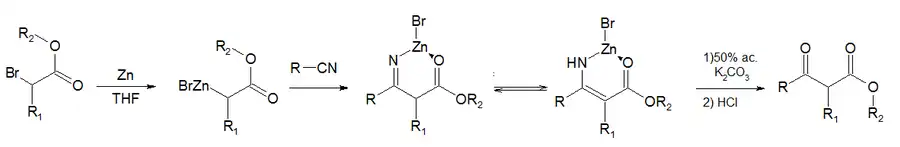
Mecanismo de reacción de la síntesis de Blaise
Los ésteres alifáticos voluminosos tienden a dar altos rendimientos. Steven Hannick y Yoshito Kishi desarrollaron una modificación.[5]
Se ha observado[6][7] que los grupos hidroxilos libres pueden tolerar el curso de esta reacción, lo cual no es común para reacciones de organometálicos.
Mecanismo
El organometálico ataca al carbono del nitrilo, formándose el complejo con zinc, el cual tautomeriza a enamina-enolato. La hidrólisis de la amina proporciona el grupo ceto deseado.
Referencias
- Edmond E. Blaise; Compt. Rend. 1901, 132, 478.
- Rinehart, K. L., Jr. Organic Syntheses, Coll. Vol. 4, p.120 (1963); Vol. 35, p.15 (1955). (Article Archivado el 16 de julio de 2012 en Wayback Machine.)
- Rao, H. S. P.; Rafi, S.; Padmavathy, K. Tetrahedron 2008, 64, 8037-8043. (Review, doi 10.1016/j.tet.2008.05.109)
- Cason, J.; Rinehart, K. L., Jr.; Thorston, S. D., Jr. J. Org. Chem. 1953, 18, 1594. (doi 10.1021/jo50017a022)
- S. M. Hannick, Y. Kishi (1983). «An improved procedure for the Blaise reaction: a short, practical route to the key intermediates of the saxitoxin synthesis». J. Org. Chem. 48: 3833-3835.
- Marko, I.E. J. Am. Chem. Soc. 2007, ASAP doi 10.1021/ja0691728
- Wang, D.; Yue, J.-M. Synlett 2005, 2077-2079.
Enlaces externos
Véase también
Este artículo ha sido escrito por Wikipedia. El texto está disponible bajo la licencia Creative Commons - Atribución - CompartirIgual. Pueden aplicarse cláusulas adicionales a los archivos multimedia.