Tensioactivo anfótero
Se llaman tensioactivos anfóteros a los tensoactivos que tienen un grupo funcional en la molécula cargado negativamente, y otro cargado positivamente (además de una parte no polar). Generalmente, como parte no polar se suele tener un grupo alquilo, y como parte polar, por lo general, un grupo carboxilato (R-COO-), junto con un grupo de amonio cuaternario (R4N+).[1] El uso del término anfótero lo hace más restrictivo: La carga de la molécula debe cambiar con el pH, mostrando una estructura zwitteriónica a un pH intermedio (punto isoeléctrico).[2]
Tensioactivos anfóteros típicos
Betaínas
Las betaínas son comúnmente clasificadas como tensioactivos anfóteros, aunque nunca exhiben la forma aniónica. Por este motivo, cada vez más, se clasifican estos tensoactivos como catiónicos más que como anfóteros. Pese a esto, muchas casas comerciales de estos productos los siguen denominando como anfóteros.
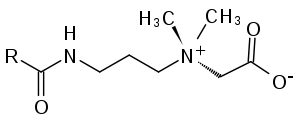 , con R = cadena de alquilo de 5-21 átomos de carbono. En muchos champús, por ejemplo, la betaína de cocamidopropilo (amidopropilbetaína del ácido graso de coco, "HT betaína") se utiliza como tensioactivo.
, con R = cadena de alquilo de 5-21 átomos de carbono. En muchos champús, por ejemplo, la betaína de cocamidopropilo (amidopropilbetaína del ácido graso de coco, "HT betaína") se utiliza como tensioactivo.
La primera betaína descubierta fue la N,N,N-trimetilglicina: 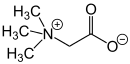
Como se puede observar, tanto de la fórmula general, como de la betaína derivada de la glicina, la carga positiva no se puede perder; de tal manera, que estos compuestos solo pueden estar en la forma zwitteriónica (con la carga positiva y negativa) o cargados positivamente (si se neutraliza el grupo carboxilato).
Las betaínas son buenos agentes espumantes, humectantes, emulsionantes y tensioactivos, especialmente en presencia de tensioactivos aniónicos. La detergencia es mejor en condiciones alcalinas. Además, las betaínas son compatibles con otros tensioactivos y que con frecuencia forman micelas mixtas; estas mezclas a menudo proporcionan propiedades únicas que no se encuentran en los tensioactivos constitutivos individuales. En su forma catiónica lineal (es decir, en condiciones neutras y ácidas), las betaínas no se ven afectados por los iones de la dureza del agua y otros iones metálicos. Tienen propiedades hidrótropas, ya que ayudan a solubilizar los tensioactivos no iónicos etoxilados en presencia de un exceso de iones. Las betaínas son especialmente suaves para la piel y tienen la capacidad de mejorar la tolerancia de la piel contra agentes tensioactivos aniónicos irritantes.[2]
Sultaínas
Las Sultaínas son betaínas que poseen un grupo sulfonato en vez de un grupo carboxilato. Igual que en el caso anterior, se clasifican muchas veces como tensioactivos anfóteros, pero realmente no lo son, ya que nunca pueden exhibir una forma aniónica pura.
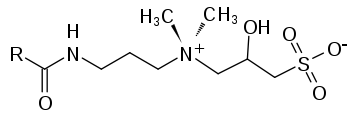 , con R = alquilo
, con R = alquilo
Son sulfobetaínas. En la naturaleza, un compuesto anfótero bastante conocido es la taurina, un aminosulfonato (el 2-aminoetanosulfónico). En champús se utiliza a menudo la cocoamidopropil hidroxisultaína como potenciador de la espuma.
Acil etilenodiaminas
Estos tensioactivos muestran propiedades anfóteras y la forma zwitteriónica aparece alrededor del pH neutro; además, la solubilidad en agua es mínima en el punto isoeléctrico.
Estos tensioactivos se sintetizan por reacción de una alquilimidazolina con ácido cloroacético (para dar anfoglicinatos o anfoacetatos) o con ácido acrílico (para dar anfopropionatos). La imidazolina de partida se puede obtener por condensación de un ácido graso con aminoetiletanolamina (H2N-CH2-CH2-NH-CH2-CH2OH) que posteriormente cicla formando el anillo de imidazolina. Cuando se carboxila la alquilimidazolina con alguno de los reactivos anteriormente citados, el anillo de imidazolina se rompe por hidrólisis. El agua también produce dicha hidrólisis:
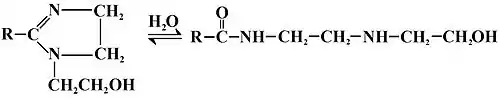
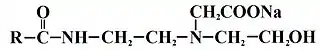
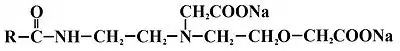
Esta clase de tensioactivos anfóteros son similares a los de betaínas. Se utilizan en productos de cuidado personal, champús para bebés, suavizantes, limpiadores industriales y de automóviles. Son compatibles con otros tensioactivos y toleran el agua dura y electrolitos.[2]
N-Alquil aminoácidos
Son derivados químicos de aminoácidos. El grupo amino (en este caso el de un aminoácido) es susceptible de ser alquilado con ciertos reactivos alquilantes. En la práctica se hace reaccionar una amina con ácido cloroacético o acrílico.
Referencias
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 503−504.
- Oldenhove de Guertechin, Louis. Handbook of Detergents, Part A: Properties (Serie: Surfactant Science). Capítulo 2: Surfactants: Classification. CRC Press. ISBN 978-0824714178.