Bélite
La bélite est un minéral industriel important dans la fabrication du ciment Portland. Son constituant principal est le silicate dicalcique, Ca2SiO4, parfois formulé comme 2 CaO · SiO2 (C2S en notation chimiste du ciment ).
Étymologie
Le nom a été donné par Törnebohm en 1897 à un cristal identifié lors d'une étude microscopique du ciment Portland[1]. Belite est un nom d'usage courant dans l'industrie du ciment, mais n'est pas un nom minéral reconnu. Il se produit naturellement comme le minéral larnite, le nom étant dérivé de Larne, en Irlande du Nord, la ville la plus proche de Scawt Hill où il a été découvert[2].
Composition et structure
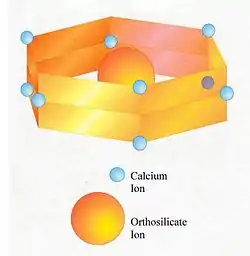
La bélite est présent dans le ciment Portland qui diffère par sa composition du silicate dicalcique pur. C'est une solution solide qui contient des quantités mineures d'autres oxydes en plus de CaO et SiO2 . La composition type dub élite est[3] :
| Oxyde | Masse % |
|---|---|
| CaO | 63,5 |
| SiO2 | 31,5 |
| Al2O3 | 2.1 |
| Fe2O3 | 0,9 |
| MgO | 0,5 |
| SO3 | 0,1 |
| Na2O | 0,1 |
| K2O | 0,9 |
| TiO2 | 0,2 |
| P2O5 | 0,2 |
Sur cette base, la formule peut être exprimée sous la forme Ca1,94 Mg0,02 Na0,01 K0,03 Fe0,02 Al0,07 Si0,90 P0,01 O3,93 . En pratique, la composition varie avec la composition massique du clinker, sous réserve de certaines limites. La substitution des ions calcium ou des ions orthosilicate nécessite que les charges électriques soient maintenues en équilibre. Par exemple, un nombre limité d' orthosilicate ( SiO44− ) les ions peuvent être remplacés par du sulfate ( SO42−) ions, à condition que pour chaque ion sulfate, deux aluminate ( AlO45−) les ions sont également substitués.
Polymorphes
Le silicate dicalcique est stable et se prépare facilement à partir de CaO réactif et de SiO2 à 300 °C. La forme basse température est la γ-bélite, ou chaux olivine . Cette forme ne s'hydrate pas et est évitée dans la fabrication du ciment.
Lorsque la température augmente, elle passe par plusieurs états polymorphes :
| Température °C | Nom | Cristal |
|---|---|---|
| >1425 | ɑ | Hexagonal |
| 1160-1425 | α'H | Orthohombrique |
| 680-1160 | α'L | Orthohombrique |
| 500-680 | β | monoclinique |
| <500 | γ | orthorhombique |
Hydratation
La bélite est le minéral du ciment Portland responsable du développement de la résistance "tardive". L'autre silicate, l'alite, apporte une résistance "précoce", en raison de sa plus grande réactivité. La bélite réagit avec l'eau (grossièrement) pour former des hydrates de silicate de calcium (CSH) et de la portlandite (Ca(OH)2) selon la réaction :
Cette réaction rapide est "chimiquement analogue" à la lente hydratation naturelle de la forstérite (l'extrémité magnésienne de l' olivine ) conduisant à la formation de serpentine et de brucite dans la nature, bien que la cinétique d'hydratation de la bélite artificielle mal cristallisée soit beaucoup plus rapide que la altération lente de la Mgolivine bien cristallisée dans des conditions naturelles.
La phase hydratée, [3 CaO · 2 SiO2 · 3 H2O], est appelée phase « C-S-H ». Il se développe sous la forme d'une masse d'aiguilles imbriquées qui fournissent la résistance du système de ciment hydraté. Une réactivité relativement élevée à la bélite est souhaitable dans la fabrication du ciment Portland, et la formation de la forme γ non réactive doit être rigoureusement évitée. Ceci est réalisé par un refroidissement rapide, formant des cristaux petits, déformés et très défectueux. Les défauts fournissent des sites pour l'attaque initiale de l'eau. L'absence de refroidissement rapide du clinker conduit à l'inversion de la bélite en forme γ. La forme γ a une structure et une densité sensiblement différentes, de sorte que l'inversion conduit à la dégradation du cristal et de sa matrice environnante, et peut également déclencher la décomposition de l' alite voisine. Ceci s'observe macroscopiquement sous forme de « saupoudrage » : les nodules de clinker tombent en une fine poussière .
Détection

Les minéraux du clinker de ciment Portland peuvent être observés et quantifiés par microscopie pétrographique . Les nodules de clinker sont coupés et broyés en une surface plane et polie. Les minéraux exposés sont rendus visibles et identifiables en gravant la surface. La surface peut alors être observée en lumière réfléchie par microscopie optique . Dans l'exemple, un nodule de clinker a été poli et attaqué avec de la vapeur de fluorure d'hydrogène . L'alite apparaît en marron, la bélite en bleu et les phases fondues en blanc. La microscopie électronique peut également être utilisée, auquel cas les minéraux peuvent être identifiés par analyse à la microsonde . La méthode privilégiée pour quantifier avec précision les minéraux est la diffraction des rayons X sur le clinker en poudre, en utilisant la technique d'analyse de Rietveld . La bélite est beaucoup plus difficile à broyer dans un broyeur à ciment que l'alite.
Voir également
- Réaction d'hydratation de la forstérite (olivine) en serpentinisation
- CCN, notation chimiste du ciment
Les références
- Jean-Pierre Bournazel, Yves Malier, Micheline Moranville Regourd, 1998, Concrete, from Material to Structure RILEM Publications, (ISBN 2-912143-04-7).
- William Alexander Deer, R. A Howie et J Zussman, Disilicates and ring silicates, , 248–249 p. (ISBN 9781897799895), « Larnite »
- Taylor H.F.W. (1990), Cement Chemistry, Academic Press, 1990, (ISBN 0-12-683900-X), p. 10-11.
- Portail des minéraux et roches