Pyoverdine
Une pyoverdine est un sidérophore fluorescent et un oligopeptide antibiotique produit notamment par un Pseudomonas aeruginosa et Pseudomonas fluorescens, des bactéries à Gram négatif[3],[4]. On en connaît actuellement une soixantaine de molécules apparentées. Les pyoverdines agissent comme facteurs de virulence des Pseudomonas[5].
| Pyoverdine | |
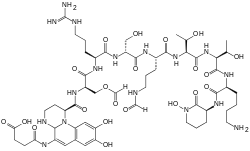 Exemple de structure d'une pyoverdine |
|
| Identification | |
|---|---|
| Synonymes |
pseudobactine |
| No CAS | [1] |
| PubChem | 45479427 (Pyoverdine de type I) |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C56H88N18O22 [Isomères] (Formule d'une pyoverdine de type I) |
| Masse molaire[2] | 1 365,405 3 ± 0,061 2 g/mol C 49,26 %, H 6,5 %, N 18,46 %, O 25,78 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Nature biochimique des pyoverdines
Contrairement à l'entérobactine, les pyoverdines sont des peptides non ribosomiques contenant un dérivé de la dihydroxyquinoléine. La structure du peptide diffère selon les espèces et une quarantaine de structures différentes ont été décrites, tandis que le chromophore acide (1S)-5-amino-2,3-dihydro-8,9-dihydroxy-1H-pyrimido[1,2-a]quinoléine-1-carboxylique demeure inchangé hormis l'azobactine d'Azotobacter vinelandii (en) qui possède un cycle urée supplémentaire[6].
Exemples
| Espèces | Souches | Chaîne peptidique de la pyoverdine * |
|---|---|---|
| P. aeruginosa | ATCC15692 | Q-DSer-Arg-DSer-FoOHOrn-c(Lys-FoOHOrn-Thr-Thr) |
| P. aeruginosa | ATCC27853 | Q-DSer-FoOHDOrn-Orn-Gly-aDThr-Ser-cOHOrn |
| P. aeruginosa | Pa6 | Q-DSer-Dab-FoOHOrn-Gln-DGln-FoOHDOrn-Gly |
| P. chlororaphis | ATCC9446 | Q-DSer-Lys-Gly-FoOHOrn-c(Lys-FoOHDOrn-Ser) |
| P. fluorescens bv.I | ATCC13525 | Q-DSer-Lys-Gly-FoOHOrn-c(Lys-FoOHDOrn-Ser) |
| P. fluorescens bv.I | 9AW | Q-DSer-Lys-OHHis-aDThr-Ser-cOHOrn |
| P. fluorescens bv.III | ATCC17400 | Q-DAla-DLys-Gly-Gly-OHAsp-DGln/Dab-Ser-DAla-cOHOrn |
| P. fluorescens bv.V | 51W | Q-DAla-DLys-Gly-Gly-OHDAsp-DGln-DSer-Ala-Gly-aDThr-cOHOrn |
| P. fluorescens bv.V | 1W | Q-DSer-Lys-Gly-FoOHOrn-c(Lys-FoOHDOrn-Ser) |
| P. fluorescens bv.V | 10CW | Q-DSer-Lys-Gly-FoOHOrn-c(Lys-FoOHDOrn-Ser) |
| P. fluorescens bv.VI | PL7 | Q-DSer-AcOHDOrn-Ala-Gly-aDThr-Ala-cOHOrn |
| P. fluorescens bv.VI | PL8 | Q-DLys-AcOHDOrn-Ala-Gly-aDThr-Ser-cOHOrn |
| P. fluorescens | 1.3 | Q-DAla-DLys-Gly-Gly-OHAsp-DGln/Dab-Gly-Ser-cOHOrn |
| P. fluorescens | 18.1 | Q-DSer-Lys-Gly-FoOHOrn-Ser-DSer-Gly-c(Lys-FoOHDOrn-Ser) |
| P. fluorescens | CCM 2798 | Q-Ser-Dab-Gly-Ser-OHDAsp-Ala-Gly-DAla-Gly-cOHOrn |
| P. fluorescens | CFBP 2392 | Q-DLys-AcOHDOrn-Gly-aDThr-Thr-Gln-Gly-DSer-cOHOrn |
| P. fluorescens | CHA0 | Q-Asp-FoOHDOrn-Lys-c(Thr-Ala-Ala-FoOHDOrn-Lys) |
| P. putida bv. B | 9BW | Q-DSer-Lys-OHHis-aDThr-Ser-cOHOrn |
| P. putida | CFBP 2461 | Q-Asp-Lys-OHDAsp-Ser-aDThr-Ala-Thr-DLys-cOHOrn |
| P. tolaasii | NCPPB 2192 | Q-DSer-Lys-Ser-DSer-Thr-Ser-AcOHOrn-Thr-DSer-cOHDOrn |
| * Les acides aminés sont abrégés sur trois lettres. Les abréviations suivantes sont également utilisées : Q = chromophore, DXxx = acide aminé D, aThr = allo-thréonine, aDThr = allo-D-thréonine, c = structure cyclique, cOHOrn = cyclo-hydroxyornithine, Dab = acide diaminobutyrique, Ac = acétyle, Fo = formyle, OH = hydroxyle[6]. | ||
Utilisations
Ces pyoverdines peuvent doper certains processus de phytoremédiation, pour le fer, mais aussi d'autres métaux[7],[8],[9] (les sidérophores sont particulièrement efficaces dans la captation du fer, mais ils montrent aussi une bonne affinité pour 28 métaux divalents dont Cd(II) et Ni(II)[10].
Notes et références
- Pyoverdines from Pseudomonas fluorescens, Sigma-Aldrich
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) S. Wendenbauma, P. Demangea, A. Dellb, J.M. Meyerc et M.A. Abdallaha, « The structure of pyoverdine Pa, the siderophore of Pseudomonas aeruginosa », Tetrahedron Letters, vol. 24, no 44, , p. 4877-4880 (lire en ligne) DOI:10.1016/S0040-4039(00)94031-0
- (en) Isabelle J. Schalk et Laurent Guillon, « Pyoverdine biosynthesis and secretion in Pseudomonas aeruginosa: implications for metal homeostasis », Environmental Microbiology, vol. 15, no 6, , p. 1661-1673 (lire en ligne) DOI:10.1111/1462-2920.12013
- (en) Pol Nadal Jimenez, Gudrun Koch, Jessica A. Thompson, Karina B. Xavier, Robbert H. Cool et Wim J. Quax, « The Multiple Signaling Systems Regulating Virulence in Pseudomonas aeruginosa », Microbiology and Molecular Biology Reviews, vol. 76, no 1, , p. 46-65 (lire en ligne) DOI:10.1128/MMBR.05007-11
- (en) Jean-Marie Meyer, « Pyoverdines: pigments, siderophores and potential taxonomic markers of fluorescent Pseudomonas species », Archives of Microbiology, vol. 174, no 3, , p. 135-142 (lire en ligne) DOI:10.1007/s002030000188
- Ferret, C. (2012). Rôle des Pseudomonas fluorescents dans la biodisponibilté des métaux contaminant les minéraux du sol: application à la phytoremédiation (Thèse de doctorat, Université de Strasbourg)
- FERRET, C. (2012). Role of fluorescent Pseudomonas in the biodisponibility of metals contamining the soil minerals (application to the phytoremediation) (résumé).
- Cornu, J. Y., Elhabiri, M., Ferret, C., Jezequel, K., Leva, Y., Lollier, M., ... & Lebeau, T. (2014). Phytoextraction-Assisted Bioaugmentation of Soils Contaminated by Cu and Cd: Role of the Bacterial Siderophore Pyoverdine. 한국토양비료학회 학술발표회 초록집, 527-527.
- Ferret, C., Cornu, J. Y., Elhabiri, M., Sterckeman, T., Braud, A., Jezequel, K., ... & Geoffroy, V. of pyoverdine supply on cadmium and nickel complexation and phytoavailability in hydroponics (Manuscript Draft, avec réponse aux relecteurs)
Voir aussi
bibliographie
- Ferret, C., Cornu, J. Y., Elhabiri, M., Sterckeman, T., Braud, A., Jezequel, K., ... & Geoffroy, V. of pyoverdine supply on cadmium and nickel complexation and phytoavailability in hydroponics (Manuscript Draft, avec réponse aux relecteurs).
- Portail de la chimie
- Portail de la biochimie