Gamma knife
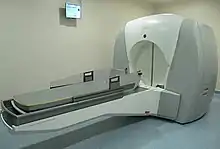
Le Gamma knife (aussi appelé couteau gamma, scalpel gamma[1] ou Leksell Gamma Knife) est un appareil utilisé pour des traitements neurochirurgicaux en radiothérapie stéréotaxique, délivrant de façon très localisée une dose élevée de rayonnements ionisants.
Historique
L'appareil a été inventé sous la direction du neurochirurgien suédois Lars Leksell, en 1967 au Karolinska Institutet de Stockholm après des études débutant dans les années 1940[2],[3] dérivé de la télécobalthérapie.
Dans les années 1950, les professeurs suédois Borje Larsson de l'Institut Gustaf Werner, Université d'Uppsala, et Lars Leksell à l'Institut Karolinska de Stockholm, en Suède, ont effectué des recherches sur la combinaison des faisceaux de protons avec un dispositif de guidage stéréotaxique capables de repérer des cibles dans le cerveau. Cette approche a finalement été abandonnée car complexe et coûteuse. Au lieu de cela, en 1967, les chercheurs ont entamé la construction du premier dispositif nommé « couteau gamma » en utilisant du cobalt 60 comme source d'énergie. Leksell a appelé cette nouvelle technique chirurgicale « radiochirurgie stéréotaxique ». Ce prototype, utilisé depuis 12 ans en Suède, a été spécifiquement conçu pour la neurochirurgie fonctionnelle et le traitement de patients souffrant de douleurs, troubles du mouvement, et même certains troubles du comportement qui ne sont pas sensibles à un traitement psychiatrique classique[4].
Réalisant le potentiel de la radiochirurgie stéréotaxique pour traiter les tumeurs cérébrales, le professeur Leksell et ses collègues ont construit un second Gamma knife en 1975. Il a été installé à l'Institut Karolinska et est devenu partie intégrante du service de neurochirurgie. Les troisième et quatrième unités, construites au début des années 1980, ont été installées à Buenos Aires, en Argentine, et Sheffield, en Angleterre. Les deux unités suivantes sont installées à l'Université de Pittsburgh et l'Université de Virginie.
En octobre 2012, le 500e appareil commercialisé par la société suédoise Elekta fondée par Lars Leksell a été installé au Brésil, et plus de 300 appareils sont opérationnels à cette date dans 38 pays et plus de 700 000 patients ont bénéficié d'une intervention chirurgicale Gamma Knife[5].
Le coût en 2011 est de 4,7 millions d'euros pour un appareil installé à l'hôpital de la Timone à Marseille[6].
Principe de fonctionnement
Les rayonnements sont délivrés par des faisceaux focalisés de rayons gamma émis par 201 sources de cobalt 60 pour les appareils de série produits jusqu'en 2006, par 192 sources pour ceux commercialisés depuis cette date. Les faisceaux se concentrent en un point ciblé à traiter, sur lequel les doses de rayonnement délivrées par les différents faisceaux s'ajoutent.
Ses objectifs sont de limiter à la fois les risques d'hémorragie[7] et de séquelles dans les zones saines que causerait une chirurgie classique invasive, ainsi que l'inoculation de germes pathogènes par les points d'entrée.
Son principe est simple : l'application d'un faisceau ionisant externe vers une zone cible permet la destruction de celle-ci, une étude balistique du faisceau permet de savoir à quelle profondeur le faisceau va déposer la dose la plus élevée (elle dépend de la nature du faisceau, en l'occurrence des rayons gamma, de leur énergie, et de la nature et de l'épaisseur des tissus à traverser). La dose est ensuite ajustée par un temps d'exposition[8].
Mais cela ne suffit pas : la balistique d'un seul faisceau est trop imprécise pour ne pas irradier de manière significative les zones saines qu'il traverse ; en effet si la dose maximale est bien délivrée au point d'intérêt, les zones en amont et aval de celui-ci recevront aussi une dose néfaste.
La parade est donc de multiplier les points d'entrée; plus ceux-ci seront nombreux, plus la dose aux tissus non ciblés sera petite et plus le temps d'exposition sera court.
Explication : le couteau gamma produit 201 faisceaux. En imaginant le point cible comme le centre d'une sphère, on comprend que l'essentiel du volume de la sphère ne sera traversé que par un petit nombre de faisceaux, mais le centre, lui, sera traversé par les 201 faisceaux : il recevra donc une dose de l'ordre de presque 201 fois plus élevée que le reste du volume de la sphère ; il faut néanmoins tenir compte de la largeur des faisceaux, ajustée à la dimension de la zone à détruire, et qui provoque une certaine superposition des faisceaux à proximité immédiate de la cible.
En outre, il faut tenir compte de la non-uniformité du dépôt de dose des faisceaux dans la profondeur des tissus (chaque faisceau dépose le maximum de sa dose au point cible) ; ce n'est donc pas une dose 201 fois supérieure, mais de l'ordre de 1 000 fois supérieure que le centre pourra recevoir par rapport au volume éloigné de la zone cible.
D'autres techniques de radiochirurgie utilisent des faisceaux étroits de rayons X émis par un accélérateur linéaire, ou des faisceaux de particules (protons)[9].
Indications médicales
Les indications médicales du traitement par couteau gamma sont les suivantes : les malformations artério-veineuses cérébrales, les neurinomes du système auditif, les tumeurs bénignes de la base du crâne, les métastases cérébrales, et dans certains aspects de la neurochirurgie fonctionnelle, comme certaines épilepsies pharmaco-résistantes, ou des névralgies faciales[réf. nécessaire].
Le nombre de patients traités a dépassé les 100 000 en 1999, 200 000 en 2002, 300 000 en 2005, 400 000 en 2007 et 500 000 en 2008. À cette dernière date, voici les pourcentages des traitements[10] :
- 44 % pour des tumeurs malignes,
- 35 % pour des tumeurs bénignes,
- 13 % pour des affections vasculaires,
- 8 % pour des désordres fonctionnels,
- 1 % pour des affections oculaires.
Galerie
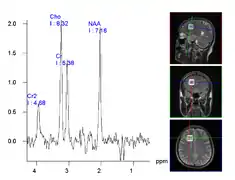 Images en spectroscopie RMN du crane d'un patient traité avec un couteau gamma.
Images en spectroscopie RMN du crane d'un patient traité avec un couteau gamma.
Notes et références
- Les termes « couteau gamma », « appareil Gamma Knife » et « scalpel gamma » sont officiellement reconnus comme valides en français par l'Office québécois de la langue française depuis 1999.
- (en) Leksell L., « The stereotaxic method and radiosurgery of the brain », Acta Chir Scand, vol. 102, no 4, , p. 316-9. (PMID 14914373)
- (en) Gerber DE, Chan TA., « Recent advances in radiation therapy », Am Fam Physician, vol. 78, no 11, , p. 1254-62. (PMID 19069018, lire en ligne)
- (en) « The Gamma Knife: A Technical Overview Development of the Gamma Knife », sur www.medicine.virginia.edu Université de Virginie, (consulté le )
- (en) « World’s 500th Leksell Gamma Knife Radiosurgery System Begins Patient Treatments in Brazil », sur www.elekta.com Elekta, (consulté le )
- « Unité de radiochirurgie Gamma Knife », sur fr.ap-hm.fr hôpital de la Timone, (consulté le )
- Les risques d'hémorragie post-interventionnelles sont limités mais pas éliminés ; une surveillance est donc requise.
- (en) « Leksell Gamma Knife Surgery Technology for Brain Tumors, Lesions and Disorders at Florida Hospital », sur www.gamma-knife-surgery.com (consulté le )
- (en) « Stereotactic Radiosurgery Overview », sur www.irsa.org International RadioSurgery Association (consulté le )
- (en) « Gamma Knife in World », sur www.groupflorence.com Group Florence Nightingale Hospitals, (consulté le )
Liens externes
- (en) The Gamma Knife: A Technical Overview, University of Virginia Health System
- La radio-neurochirurgie stéréotaxique (Leksel Gamma Knife LGK-Novalis), Glioblastome Association Michèle Esnault
- Portail de la médecine
- Portail de la physique
- Portail des neurosciences