Cyanate d'argent
Le cyanate d'argent est le sel de cyanate d' argent . Il peut être fabriqué par la réaction du cyanate de potassium avec du nitrate d'argent en solution aqueuse, à partir de laquelle il précipite sous forme solide.
Alternativement, la réaction
analogue à la réaction utilisée pour la production industrielle de cyanate de sodium, peut être utilisé.
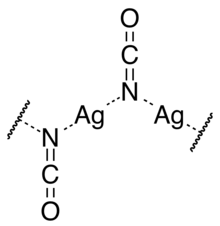
Le cyanate d'argent est une poudre beige à grise. Il cristallise dans le système cristallin monoclinique dans le groupe d'espace P 2 1 / m avec des paramètres a=547.3 pm, b = 637.2 pm, c = 341.6 pm, et β= 91°. Chaque cellule unitaire contient deux ions cyanate et deux ions argent. Les ions argent sont chacun équidistants de deux atomes d'azote formant un groupe N-Ag-N droit. Les atomes d'azote sont chacun coordonnés à deux atomes d'argent, de sorte qu'il existe des chaînes en zigzag d'atomes d'argent et d'azote alternés allant dans la direction de l'axe "b" monoclinique, avec les ions cyanate perpendiculaires à cet axe[1].
Le cyanate d'argent réagit avec l'acide nitrique pour former du nitrate d'argent, du dioxyde de carbone et du nitrate d'ammonium[2] .
- </img>
Voir également
Notes et références
- D. Britton, J. D. Dunitz: The crystal structure of silver cyanate, Acta Crystallogr. (1965). 18, 424-428, DOI:10.1107/S0365110X65000944
- J. Milbauer: Bestimmung und Trennung der Cyanate, Cyanide, Rhodanide und Sulfide in Fresenius' Journal of Analytical Chemistry 42 (1903) 77-95, DOI:10.1007/BF01302741.
- Portail de la chimie