Sorbitol
Le sorbitol ou glucitol est un polyol naturel, au pouvoir sucrant deux fois plus faible que le saccharose. À la différence des oses, sa structure ne renferme aucune fonction cétone ou aldéhyde. Il est principalement utilisé comme édulcorant de masse pour remplacer le saccharose. Il est aussi utilisé comme séquestrant, excipient, humectant ou stabilisant, dans les médicaments, les cosmétiques et les aliments. Il est métabolisé lentement par l'organisme et apporte peu de calories. C'est aussi un laxatif lorsqu'il est consommé à haute dose.
« E420 » redirige ici. Pour les autres significations, voir E420 (homonymie).
| Sorbitol | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (2S,3R,4R,5R)-hexane-1,2,3,4,5,6-hexol | |
| Synonymes |
D-(−)-glucitol |
|
| No CAS | ||
| No ECHA | 100.000.056 | |
| No CE | 200-061-5 | |
| Code ATC | V04 | |
| PubChem | ||
| No E | E420(i), E420(ii) | |
| FEMA | 3029 | |
| Apparence | Poudre blanche[1] | |
| Propriétés chimiques | ||
| Formule | C6H14O6 [Isomères] |
|
| Masse molaire[2] | 182,171 8 ± 0,007 6 g/mol C 39,56 %, H 7,75 %, O 52,7 %, |
|
| pKa | 13,57[3] | |
| Propriétés physiques | ||
| T° fusion | 95 °C (88 à 102 °C[1]) | |
| T° ébullition | 296 °C | |
| Solubilité | Soluble dans l'eau (2 750 g·l−1 à 30 °C)[3], |
|
| Masse volumique | 1,5 g·cm-3[4] | |
| Thermochimie | ||
| Cp | ||
| Cristallographie | ||
| Classe cristalline ou groupe d’espace | P21[6] | |
| Paramètres de maille | a = 4,791 Å b = 9,488 Å |
|
| Volume | 803,57 Å3[6] | |
| Écotoxicologie | ||
| DL50 | 15,9 g·kg-1 (rats, oral) 17,8 g·kg-1 (souris, oral)[3] |
|
| LogP | -2,2[4] | |
| Composés apparentés | ||
| Isomère(s) | Dulcitol, Mannitol, Iditol | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Origine
Le sorbitol tient son nom du sorbier dont les baies contiennent beaucoup de sorbitol. Mais le fruit à plus haute teneur en sorbitol est en fait le pruneau.
Le sorbitol est le produit majeur de la photosynthèse, le principal glucide exporté dans le phloème et un produit pour le stockage temporaire du carbone chez les espèces ligneuses de la famille Rosaceae. Chez les espèces dites à sorbitol, la synthèse de celui-ci est en compétition avec celle du saccharose car ces deux sucres ont un précurseur commun, le glucose-6-phosphate. Les mécanismes qui contrôlent et régulent la partition du C entre ces deux voies sont inconnus. Néanmoins, les effets de l'environnement et les conditions de culture peuvent jouer un rôle important pour modifier les flux métaboliques entre le sorbitol, le saccharose et l'amidon. L'accumulation de sorbitol est considérée comme une réponse adaptative des plantes aux contraintes saline, hydrique et de basse température. La synthèse du sorbitol est confinée aux organes sources. Sa dégradation n'a lieu que dans les organes puits[7].
Le sorbitol est aussi produit naturellement par le corps humain mais il est mal digéré par l'organisme. Un excès de sorbitol dans le sang peut entraîner :
- une cataracte : un dépôt de sorbitol sur le cristallin le rend plus opaque ; cela n'a rien à voir avec la rétinopathie diabétique ;
- une neuropathie (pour les nerfs).
Propriétés
Propriétés chimiques
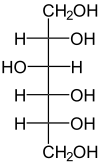
Le sorbitol est un polyol comme le glycérol ou le glycol. Il est composé d'une chaîne carbonée de six atomes de carbone et six groupes alcool (un groupe par carbone). Sa formule chimique est C6H14O6 et il est l'isomère de trois autres polyols : dulcitol, mannitol et iditol.
Propriétés physiques
Le sorbitol est un solide blanc très soluble dans l'eau (2 750 g·l−1 à 30 °C[3]) et faiblement soluble dans l'éthanol[8].
Métabolisme
La dose maximale de sorbitol au-dessus de laquelle il n'est pas toléré par le transit intestinal est de 0,15–0,17 g·kg-1 de masse corporelle pour l'homme et 0,24–0,3 g·kg-1 de masse corporelle pour la femme[9].
Utilisations
En industrie agroalimentaire, cet édulcorant présente de nombreux avantages. Chez l'Homme, le sorbitol est métabolisé de la même façon que le glucose : il apporte la même énergie. Toutefois, son métabolisme étant non insulinodépendant, il n'augmente pas la glycémie. Cette propriété est particulièrement intéressante pour les produits destinés aux diabétiques. Il est non fermentescible par les levures. Possédant une grande capacité de rétention d'eau, le sorbitol est responsable de la consistance moelleuse d'un grand nombre de produits alimentaires. L'eau fixée s'évapore difficilement. Le sorbitol est également utilisé en tant qu'agent de retard de la cristallisation du saccharose dans les produits chocolatés.
Chimie analytique
Le sorbitol est utilisé comme étalon interne dans l'analyse quantitative des sucres par chromatographie gazeuse avec silylation.
Alimentation
C'est un édulcorant[11] (E420[12]) utilisé dans la nourriture de régime mais aussi dans nombre de produits élaborés par l'industrie agroalimentaire dans lesquels il joue le rôle d'anticristallisant et d'émollient. Il est aussi utilisé comme excipient, humectant, stabilisant et séquestrant[13],[14]. Il fournit 2,6-3,4 kilocalories par gramme[9], donc moins que le sucre (>3,5 calories par gramme[9]) et n'augmente que très peu la glycémie. Le sorbitol, comme l'érythritol et le xylitol, possède un goût frais en bouche utile pour les chewing gum, les dentifrices et les produits pour soins de la bouche[15]. L'abus chronique de sucreries édulcorées au sorbitol peut provoquer des troubles gastriques et peut représenter un apport calorique non négligeable (contrairement aux allégations industrielles)[16].
Élevage
Il a été montré que l'apport d'énergie, sous forme de sorbitol, aux bovins avant l'abattage prévient la production de viande à pH élevé[17],[18].
Médecine
Le sorbitol est utilisé comme médicament (sans ordonnance) afin de traiter la constipation, grâce à son effet laxatif.
Microbiologie
Le sorbitol remplace le lactose dans les géloses Mac Conkey pour l'identification de la bactérie Escherichia coli O157:H7 (la maladie du hamburger), la souche E. coli O157:H7 est sorbitol-, elle ne peut métaboliser le sorbitol, alors que les autres E. coli non-pathogènes du système digestif sont sorbitol+, elles peuvent métaboliser le sorbitol.
Cosmétique
Le sorbitol est souvent utilisé par la cosmétique moderne en tant qu'agent humidifiant et épaississant. On le retrouve souvent comme ingrédient dans la plupart des dentifrices. Son goût frais en bouche, conféré par sa qualité de polyol, justifie sa présence dans les solutions d'hygiène bucco-dentaire.
Carburant
Le sorbitol est très connu comme propergol de fusée en association avec le nitrate de potassium (salpêtre) (65 % de nitrate de potassium et 35 % de sorbitol). Grâce à sa basse température de fusion, il se lie très bien avec le nitrate de potassium pour former du propergol solide[19].
L'organisation terroriste État islamique s'est ainsi procuré en 2016 plusieurs tonnes de sorbitol à vocation alimentaire pour le mélanger au nitrate de potassium afin de fabriquer des roquettes[20].
Contre-indications
En cas de grossesse ou d'allaitement, l'ingestion de sorbitol est déconseillée.[réf. nécessaire]
Le sorbitol est contre-indiqué dans l’intolérance héréditaire au fructose (IHF)
Composition
Le sorbitol destiné à l'alimentation est composé d'un minimum de 97 % de glycitols et pas moins de 91 % de D-sorbitol en matière sèche. Les glycitols sont des composés dont la formule développée est CH2OH-(CHOH)n-CH2OH, dans laquelle n représente un nombre entier[1].
Notes et références
- Commission européenne, « Directive 2008/60/CE de la Commission du 17 juin 2008 établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires », Journal officiel de l’Union européenne, no L 158, , p. 17–40 (résumé)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) ChemIDplus, « Sorbitol - RN: 50-70-4 », sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine (consulté le )
- D - SORBITOL, Fiches internationales de sécurité chimique
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 978-0-88415-858-5, LCCN 96036328)
- « Sorbitol », sur www.reciprocalnet.org (consulté le )
- Escobar Gutiérrez A.J. 1995. Photosynthèse, partition du carbone et métabolisme du sorbitol dans les feuilles adultes de pêcher (Prunus persica (L.) Batsch). Thèse de Doctorat de l'Université de Poitiers, France.
- (en) [PDF] JECFA, FAO, « Sorbitol », Jecfa Monogragh, sur www.fao.org, FAO, (consulté le ), p. 2
- (en) Tsuneyuki Oku & Sadako Nakamura, « Digestion, absorption, fermentation, and metabolism of functional sugar substitutes and their available energy. », Pure Appl. Chem., vol. 74, no 7, , p. 1253–1261 (lire en ligne) [PDF]
- [PDF] (en) D Glaser, « Specialization and phyletic trends of sweetness reception in animals », Pure Appl. Chem., vol. 74, no 7, , p. 1153–1158 (lire en ligne)
- Parlement européen et Conseil de l'europe, « Directive 94/35/CE concernant les édulcorants destinés à être employés dans les denrées alimentaires. », Journal Officiel, no L 237, (lire en ligne). [PDF]
- Parlement européen et Conseil de l'europe, « La Directive 95/2/CE concernant les additifs alimentaires autres que les colorants et les édulcorants », Journal officiel de l'Union européenne, no L 61, , p. 1-56 (lire en ligne). [PDF]
- « Noms de catégorie et système international de numérotation des additifs alimentaires », CAC/GL 361989, sur http://www.codexalimentarius.net, Codex Alimentarius, (consulté le ), p. 1-35 [PDF]
- (en) Codex Alimentarius Commission, « Updated up to the 31st Session of the Codex Alimentarius Commission for Sorbitol (420(i)) », GSFA Online, sur http://www.codexalimentarius.net, Codex Alimentarius, (consulté le )
- (en) « Polyols », sur www.cargillpersonalcare.com (consulté le )
- (en) « Chewing gum weight loss warning », BBC News, (consulté le )
- Intérêt d'un apport d'énergie aux bovins avant l'abattage pour la prévention des viandes a pH élevé
- De la pratique de l'abattage des animaux de rente
- (en) Richard Nakka, Richard Nakka's Experimental Rocketry, 1er mai 2007
- Guillaume Dasquié, « Comment du sucre français s'est retrouvé dans les bombes de Daech », Le Journal du dimanche.fr, (lire en ligne, consulté le )
Voir aussi
Articles connexes
- Portail de la chimie
- Alimentation et gastronomie
- Portail de la pharmacie