Isomalt
L'isomalt, ou parfois isomalte, (de formule C12H24O11) est un édulcorant (polyol) employé en alimentation humaine et codifié E953[2] en Europe. Il a un pouvoir sucrant de 0,5 c’est-à-dire qu'il a un goût moitié moins sucré que le sucre de table (saccharose).
| Isomalt | |
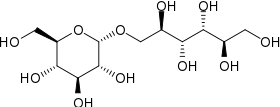
| |
| Identification | |
|---|---|
| Nom UICPA | (2R,3R,4R,5R)-6-[ [(2S,3R,4S,5S,6R)-3,4,5- trihydroxy-6-(hydroxymethyl)-2-tetrahydropyranyl ]oxy]hexane-1,2,3,4,5-pentol |
| Synonymes |
Isomaltitol |
| No CAS | |
| No ECHA | 100.040.096 |
| No CE | 244-122-4 |
| PubChem | |
| No E | E953 |
| SMILES | |
| InChI | |
| Apparence | Solide blanc sans odeur |
| Propriétés chimiques | |
| Formule | C12H24O11 [Isomères] |
| Masse molaire[1] | 344,312 4 ± 0,014 6 g/mol C 41,86 %, H 7,03 %, O 51,11 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Composition
L'isomalt est un mélange de deux composés dans les proportions 50/50, comme le sucre inverti. Pour le sucre inverti, il s'agit des molécules de glucose et de fructose. Pour l'isomalt, il s'agit de deux composés plus complexes, qui sont des dérivés du saccharose par des transformations chimiques multiples ou dérivés de l'isomaltose par hydrogénation. Ces deux composés sont le 1,6-glucopyranosyl-D-sorbitol (abrégé GPS - numéro CAS 534-73-6) et le 1,1-glucopyranosyl-D-mannitol (abrégé GPM - numéro CAS 20942-99-8)[3].
Propriétés
L'isomalt est un dérivé du saccharose, mais ses propriétés sont bien différentes. En voici quelques-unes :
- Il a une plus grande stabilité thermique que le saccharose, c’est-à-dire qu'il se dégrade moins vite sous l'action de la chaleur.
- Il se dissout moins bien dans l'eau : à 25 °C, on peut dissoudre au maximum 28 g d'isomalt dans 100 g d'eau, alors que l'on peut dissoudre à la même température 200 g de saccharose dans la même quantité d'eau.
- Il « remouille » moins que le saccharose (on dit qu'il est moins hygroscopique), ce qui permet aux pièces en sucre de conserver plus longtemps leur brillant et leur tenue.
- Il ménage les dents : les bactéries présentes dans la bouche ne peuvent pas utiliser l'isomalt comme substance nutritive, ce qui empêche la production d'acides, nuisibles pour les dents.
- Il a deux fois moins de calories que le sucre.
- Il a moins de pouvoir sucrant que le saccharose (sucre de table) : il faut exactement deux fois plus d'isomalt pour avoir le même goût sucré que le saccharose, donc cela revient à avoir le même nombre de calories que le sucre de table si on veut le même goût.
- Une consommation excessive d'isomalt peut avoir un effet laxatif.
- Il reste parfaitement transparent même une fois chauffé, ce qui permet de construire des pièces avec une apparence de verre, par exemple en pâtisserie.
Production
L'isomalt est produit industriellement en deux étapes à partir du saccharose (un diholoside comprenant une unité de glucose et une unité de fructose). La première étape est la production de l'isomaltulose (palatinose) par isomérisation du saccharose via l'action d'enzymes sucrose isomérases (alias sucrose-mutases ou isomaltulose-synthases) obtenues à partir de la Protaminobacter rubrum[4]. L'enzyme modifie la liaison osidique (1→2) du saccharose en une liaison (1→6). La deuxième étape est l'hydrogénation catalytique de l'isomaltulose qui conduit à la production d'un mélange de diholosides et d'oses hydrogénés dont les 2 principaux composés sont le glucose α(1→6) sorbitol et le glucose α(1→1) mannitol[3],[5].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Parlement européen et Conseil de l'europe, « Directive 95/31/CE établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires modifiée par les directives 98/66/CE et 2000/51/CE. », Journal officiel de l'Union européenne, (résumé, lire en ligne)
- (en) JECFA, FAO, « Isomalt (Hydrogenated isomaltulose) », Monograph, sur www.fao.org, FAO, (consulté le )
- (en) BAR Lina, D Jonker & G Kozianowski, « Isomaltulose (Palatinose®): a review of biological and toxicological studies. », Food and Chemical Toxicology, vol. 40, no 10, , p. 1375-1381 (ISSN 0278-6915, DOI 10.1016/S0278-6915(02)00105-9, résumé)
- (en) Cargill, « Application for the approval of Isomaltulose. », sur www.foodstandards.gov.uk, www.foodstandards.gov.uk, (consulté le ), p. 1-70 [PDF]
Voir aussi
Articles connexes
Liens externes
Bibliographie
- R Garrett, CM Grisham, B Lubochinsky (2000) Biochimie Éditions Boeck Université. 1292 pages. (ISBN 2-7445-0020-8)
- Portail de la chimie
- Alimentation et gastronomie