Diméthoxyphénol
Le diméthoxyphénol est un composé aromatique de formule C8H10O3. Il constitué d'un cycle de benzène substitué par deux groupes méthoxyle et un groupe hydroxyle.
Du fait des positions relatives possibles des différents groupes, il existe six isomères du diméthoxyphénol. Cependant, l'isomère le plus courant est le 2,6-diméthoxyphénol, avec les deux groupes méthoxyle en position ortho du groupe hydroxyle, connu sous le nom de « syringol ».
Propriétés
| Diméthoxyphénol | ||||||
| Nom | 2,3-Diméthoxyphénol | 2,4-Diméthoxyphénol | 2,5-Diméthoxyphénol | 2,6-Diméthoxyphénol | 3,4-Diméthoxyphénol | 3,5-Diméthoxyphénol |
| Autre nom | Syringol | Taxicatigénine | ||||
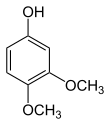
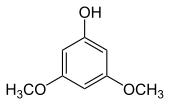
| Structure | 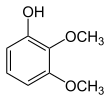 |
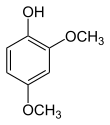 |
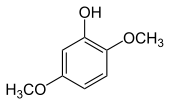 |
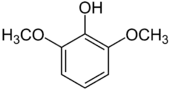 |
 |
 |
| Formule | C8H10O3 | |||||
| Numéro CAS | ||||||
| PubChem | 78828 | 593006 | 5314498 | 7041 | 16251 | 10383 |
| Masse molaire | 154,16 g·mol−1 | |||||
| État | liquide | solide | liquide | solide | solide | solide |
| Apparence | liquide visqueux translucide jaune foncé[1] | poudre jaune[2] | liquide rouge[3] | cristaux blancs à incolores, odeur de bois, médicinale[4] cristaux beige[5] |
cristaux marron clair[6] | cristaux jaune clair[7] |
| Masse volumique | 1,182 g·cm-3 (25 °C)[1] | |||||
| Point de fusion | 53 à 56 °C[5] | 79 à 82 °C[6] | 40 à 43 °C[7] | |||
| Point d'ébullition | 233 à 234 °C[1] | 269,4 °C | 261 °C[5] | 167 °C (14 mmHg)[9] | 172 à 175 °C (23 hPa)[7] 294,1 °C (760 mmHg) | |
| Point d'éclair | 109 °C (coupelle fermée)[1] | 140 °C (coupelle fermée)[5] | 78 °C[11] | |||
| Solubilité | Soluble dans le chloroforme[12] | Légèrement soluble dans l'eau[13], soluble dans les huiles[4] | Soluble dans l'eau[9] | Soluble dans le méthanol, l'éthanol, le benzène, l'eau (légèrement) et le chloroforme. | ||
| Indice de réfraction | 1,540[12] | |||||
| SGH |  [1] |
  [2] |
   [3] |
 [5] |
 [6] |
 [7] |
| Phrase H et P | H315, H319 et H335 [1] |
H304 et H403 [2] |
H304, H332 et H403 [3] |
H302, H315, H319 et H335 [5] |
H315, H319 et H335 [6] |
H315, H319 et H335 [7] |
| P261 et P305+P351+P338 [1] |
P305+P351+P338 et P332+P313 [2] |
P305+P351+P338 et P332+P313 [3] |
P261 et P305+P351+P338 [5] |
P261 et P305+P351+P338 [6] |
P261 et P305+P351+P338 [7] | |
Utilisation
Le 2,3-diméthoxyphénol est utilisé dans l'étude de la désamination nitrosative des bases nucléiques induite par les dérivés réactifs de l'azote (DRA)[12].
Le 2,6-diméthoxyphénol est utilisé comme arôme « fumé » dans divers produits alimentaires : whisky, rhum, thé, épices, fruits de mer, viande, réglisse, café, saveur de noix. Il est considéré comme le composé chimique le plus important concernant les arômes de type « fumé »[13].
Le 3,4-diméthoxyphénol est utilisé dans la préparation de dérivés de 5,6-diméthoxybenzofuranone et de composés anti-Alzheimer multi-cibles. il est aussi utilisé dans les synthèses du 3,4-diméthoxyphényl-β-D-glucopyranoside et du 4-(but-2-ényloxy)-1,2-diméthoxybenzène. C'est enfin un précurseur dans la synthèse de 4H-chromènes[9].
Le 3,5-diméthoxyphénol est un marqueur de l'empoisonnement par l'if commun (Taxus baccata)[11].
Références
- Fiche Sigma-Aldrich du composé 2,3-Dimethoxyphenol, consultée le 18 mai 2019.
- Fiche Novochemy du composé 2,4-dimethoxyphenol, consultée le 18 mai 2019.
- Fiche Novochemy du composé 2,5-dimethoxyphenol, consultée le 18 mai 2019.
- Fiche FAO du 2,6-Dimethoxyphenol
- Fiche Sigma-Aldrich du composé 2,6-Dimethoxyphenol, consultée le 18 mai 2019.
- Fiche Sigma-Aldrich du composé 3,4-Dimethoxyphenol, consultée le 18 mai 2019.
- Fiche Sigma-Aldrich du composé 3,5-Dimethoxyphenol, consultée le 18 mai 2019.
- « Fiche du composé 3,4-Dimethoxyphenol », sur Alfa Aesar (consulté le ).
- « Fiche du composé 3,5-Dimethoxyphenol », sur Alfa Aesar (consulté le ).
- « Fiche du composé 2,3-Dimethoxyphenol », sur Alfa Aesar (consulté le ).
- « Fiche du composé 2,6-Dimethoxyphenol », sur Alfa Aesar (consulté le ).