Acide benzoïque
L'acide benzoïque, de formule chimique C6H5COOH (ou C7H6O2) est un acide carboxylique aromatique dérivé du benzène.
| Acide benzoïque | |
| |
| Identification | |
|---|---|
| Nom UICPA | acide benzoïque |
| Synonymes |
Acide benzènecarboxylique |
| No CAS | |
| No ECHA | 100.000.562 |
| No CE | 200-618-2 |
| No E | E210 |
| FEMA | 2131 |
| SMILES | |
| InChI | |
| Apparence | cristaux blancs ou poudre[1] |
| Propriétés chimiques | |
| Formule | C7H6O2 [Isomères] |
| Masse molaire[2] | 122,121 3 ± 0,006 6 g/mol C 68,85 %, H 4,95 %, O 26,2 %, |
| pKa | 4,2 |
| Propriétés physiques | |
| T° fusion | 122,35 °C[1] |
| T° ébullition | 249,9 °C[1] |
| Solubilité | dans l'eau à 20 °C : 2,9 g l−1[1], soluble dans le chloroforme, l'éthanol et l'acétone |
| Masse volumique | 1,3 g cm−3[1]
|
| T° d'auto-inflammation | 570 °C[1] |
| Point d’éclair | 121 °C (coupelle fermée)[1] |
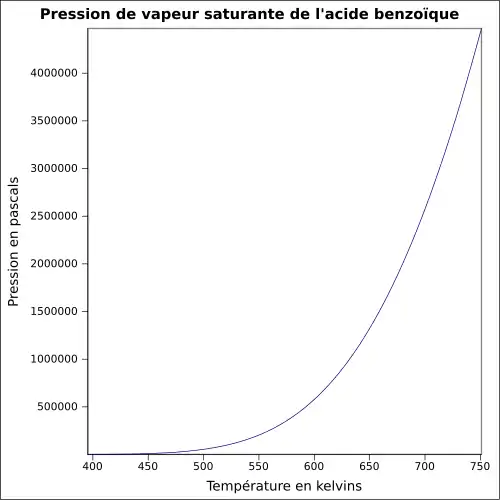
| Pression de vapeur saturante | à 25 °C : 0,1 Pa[1]
|
| Point critique | 45,6 bar, 478,85 °C[4] |
| Thermochimie | |
| S0solide | 165,7 J mol−1 K−1 sous 1 bar[réf. souhaitée] |
| ΔfH0solide | −384,8 kJ/mol[5] |
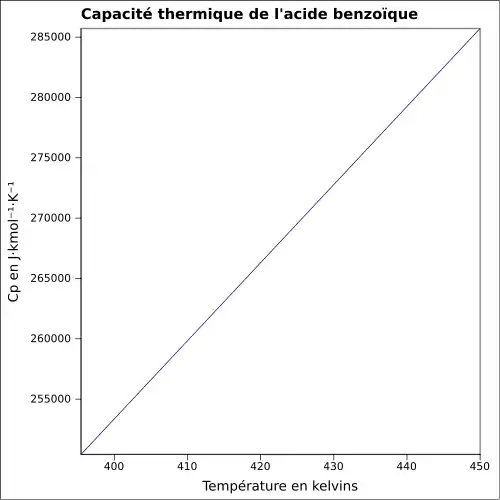
| Cp | 148 J mol−1 K−1 à 300 K 259 J mol−1 K−1 à 413 K (liquide) |
| PCS | 3 226,9 kJ mol−1 (25 °C, solide)[7] |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | P21/c[8] |
| Paramètres de maille | a = 5,500 Å b = 5,128 Å |
| Volume | 613,96 Å3[8] |
| Propriétés optiques | |
| Indice de réfraction | 1,539 7[9] |
| Précautions | |
| SIMDUT[10] | |
 D2B, |
|
| NFPA 704 | |
| Directive 67/548/EEC | |
 Xn |
|
| Écotoxicologie | |
| DL50 | 1 700 mg kg−1 (rats, peroral)[réf. souhaitée] |
| LogP | 1,87[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Description
Il est utilisé comme conservateur alimentaire et est naturellement présent dans certaines plantes. C'est par exemple l'un des principaux constituants de la gomme benjoin, utilisée dans des encens dans les églises de Russie et d'autres communautés orthodoxes. Bien qu'étant un acide faible, l'acide benzoïque n'est que peu soluble dans l'eau du fait de la présence du cycle benzénique apolaire.
On trouve de l'acide benzoïque dans les plantes alimentaires :
- en quantité notable dans le canneberge d'Amérique[11] (Vaccinium macrocarpon) : 48,10 mg/100 ml ;
- dans une moindre mesure dans la poudre de cacao (Theobroma cacao) : 0,06 mg/100 ml.
Parmi les principaux composés qui dérivent de l'acide benzoïque, on peut citer l'acide salicylique et l'acide acétylsalicylique plus connu sous le nom d'aspirine.
En tant qu'additif alimentaire, il est référencé en Europe sous le code E210. Ses sels, appelés des « benzoates », sont référencés sous les numéros :
- E211, benzoate de sodium (Ba) ;
- E212, benzoate de potassium (Ba) ;
- E213, benzoate de calcium (Ba).
Au-dessus de 370 °C, il se décompose en formant du benzène et du dioxyde de carbone. L'acide benzoïque a une odeur forte et est facilement inflammable.
Historique
En 1830, Friedrich Wöhler rencontre Justus von Liebig, qui poursuit des recherches similaires sur les cyanates. Ils extraient, en 1837, l’amygdaline à partir des amandes amères, et découvrent l’acide benzoïque en oxydant l’amygdaline par l’acide nitrique. En 1832, ils publient les résultats de travaux et montrent que les radicaux organiques peuvent se combiner à l’hydrogène électropositif aussi bien qu’à l’oxygène électronégatif. Ils éditent ensemble les Annalen der Chemie und Pharmazie.
En 2021, la NASA annonce la découverte de traces d'acide benzoïque sur la planète Mars [12].
Production
Production industrielle
L'acide benzoïque est produit industriellement par oxydation partielle du toluène par l'oxygène en phase gazeuse en présence de catalyseurs tels que des sels de cuivre[13] ou le pentoxyde de vanadium (V2O5).
Synthèse au laboratoire
L'acide benzoïque est peu cher et disponible auprès de nombreux fournisseurs. Sa synthèse au laboratoire est seulement pratiquée à titre d'exercices pédagogiques.
- L'oxydation du toluène, de l'alcool benzylique ou du benzaldéhyde par le permanganate de potassium produit aussi de l'acide benzoïque. L'oxydation catalytique de l'alcool benzylique[14],[15],[16],[17] avec de l'air ou de l'O2 gazeux comme oxydant est une alternative durable prometteuse à l'oxydation avec du permanganate. Cette réaction peut devenir pertinente sur le plan industriel, en particulier si un catalyseur à base de métal non noble est utilisé[14].
- On peut l'obtenir par l'hydrolyse d'un composé de même niveau d'oxydation que lui (par exemple à partir du benzonitrile ou du benzamide).
- On peut aussi l'obtenir par réaction d'un réactif de Grignard avec le dioxyde de carbone. Le schéma réactionnel ci-dessous montre par exemple l'obtention de l'acide benzoïque à partir du bromobenzène.

Précautions
- Phrases de risque :
- R22 (Nocif en cas d’ingestion)
- R36 (Irritant pour les yeux)
- Conseils de prudence :
- S24 (Éviter le contact avec la peau)
Risques
Selon une étude britannique publiée en 2007, un lien a été établi entre la consommation d'acide benzoïque en association avec des mélanges de colorants synthétiques, et l'hyperactivité infantile, plus précisément le trouble du déficit de l'attention[18],[19].
Alimentation
L'acide benzoïque fait partie des additifs alimentaires et porte le numéro SIN E210[20].
Il est aussi contenu naturellement dans certains aliments (notamment dans les fruits de la plaquebière).
Réglementation
Sur le plan de la réglementation des produits phytopharmaceutiques :
- pour l’Union européenne : cette substance active est inscrite à l’annexe I de la directive 91/414/CEE par la directive 2004/30/CE ;
- pour la France : cette substance active est autorisée dans la composition de préparations bénéficiant d’une autorisation de mise sur le marché.
Voir aussi
- Benzoate de sodium
- Acide benzènedicarboxylique
- Acide benzènetricarboxylique
- Acide 4-tert-butylbenzoïque (PTBBA)
- Acide thiobenzoïque
Liens externes
Références
- ACIDE BENZOIQUE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- http://bilbo.chm.uri.edu/CHM112/tables/thermtable.htm
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 2, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-858-6)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- « Benzoic acid », sur reciprocalnet.org (consulté le )
- (en) J. G. Speight et Norbert Adolph Lange, Lange's Handbook of Chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.289
- « Acide benzoïque » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- d'après Phenol ExplorerPhenol Explorer INRA
- sur Futura science
- Klaus Weissermel et Hans-Jürgen Arpe, Chimie organique industrielle, Éd. De Boeck Université, trad. de la 3e éd., p. 364.
- (en) « Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol », ACS Catal, , p. 1103-1113 (lire en ligne)
- (en) Gergely Nagy, Andrea Beck, György Sáfrán et Zoltán Schay, « Nanodisperse gold catalysts in oxidation of benzyl alcohol: comparison of various supports under different conditions », Reaction Kinetics, Mechanisms and Catalysis, vol. 128, no 1, , p. 71–95 (ISSN 1878-5204, DOI 10.1007/s11144-019-01615-8, lire en ligne, consulté le )
- (en) Ben Qi, Yanbing Wang, Lan-Lan Lou et Ying Yang, « Solvent-free aerobic oxidation of benzyl alcohol over palladium catalysts supported on MnOxprepared using an adsorption method », Reaction Kinetics, Mechanisms and Catalysis, vol. 108, no 2, , p. 519–529 (ISSN 1878-5204, DOI 10.1007/s11144-012-0529-y, lire en ligne, consulté le )
- (en) Liming Sun, Wenwen Zhan, Jiang Shang et Guojian Chen, « Carbon-encapsulated Fe3O4 for catalyzing the aerobic oxidation of benzyl alcohol and benzene », Reaction Kinetics, Mechanisms and Catalysis, vol. 126, no 2, , p. 1055–1065 (ISSN 1878-5204, DOI 10.1007/s11144-018-01529-x, lire en ligne, consulté le )
- Jim Stevenson et al., université de Southampton, dans The Lancet, septembre 2007. Étude relatée dans Le Monde, 7 septembre 2007.
- Documentaire Reporter diffusé sur RTL TVI, 5 février 2010.
- Codex alimentarius, « Noms de catégorie et système international de numérotation des additifs alimentaires », sur codexalimentarius.net, (consulté le )
- Portail de la chimie