Composé carbonylé
Un composé carbonylé est un composé organique comportant une double liaison entre un atome de carbone et un atome d'oxygène, l'atome de carbone étant lié communément à des atomes d'hydrogène ou de carbone. En effet, l'organisme IUPAC (International Union of Pure and Applied Chemistry) précise[1] que les fonctions esters ou les acides carboxyliques et leurs dérivés font également partie des composés carbonylés, bien que leur niveau d'oxydation du carbone soit différent. Dans ce dernier cas on parle de groupe carboxyle.
« Carbonyle » redirige ici. Pour les autres significations, voir Carbonyle de métal.
Sans autre condition, les composés dotés de fonction carbonyle forment la famille des cétones, mais s'y range également celle des aldéhydes chez lesquels le carbone est lié à un atome d'hydrogène et à un atome de carbone et non à deux atomes de carbone. La présence d'un atome d'hydrogène sur un carbone voisin range cette fois le composé dans la famille des composés carbonylés énolisables.
Nomenclature
Si le groupe carbonyle est le principal groupement fonctionnel, donc dans les aldéhydes et les cétones, le nom du composé est celui de l'alcane correspondant avec remplacement du suffixe -e de l'alcane par -al ou par -one (ex.: méthanal et méthanone). Lorsque les deux fonctions sont présentes, le groupe aldéhyde est considéré comme prioritaire par rapport au groupe cétone et impose donc le suffixe -al, s'il est le groupe principal.
Lorsque le groupe carbonyle n'est pas le groupe principal (il est donc considéré comme substituant), il impose le préfixe oxo-, aussi bien dans le cas de cétones que d'aldéhydes.
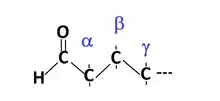
La nomenclature des aldéhydes et des cétones a évolué. Dans le passé, l'atome de carbone accolé directement au groupe carbonyle était qualifié d'alpha, le suivant de bêta et ainsi de suite selon l'alphabet grec. Par la suite, les positions sont désignées par des chiffres, le carbone du groupe carbonyle étant affecté du chiffre 1.
Caractéristiques
Physique
- Les températures de changement d'état sont plus élevées que dans les alcanes équivalents.
- Contrairement à l'eau ou aux alcools, les atomes d'hydrogène sont liés en général à des atomes de carbone, d'électronégativité proche. Ils ne sont donc pas chargés positivement, ce qui entraîne l'absence de formation de liaisons hydrogène. Cela explique des températures de changement d'état plus basses que dans les alcools équivalents (→synthèse des aldéhydes).
Énergie de liaison
L'énergie de liaison C=O est très importante (liaison par conséquent difficile à rompre), en moyenne de l'ordre de 750 kJ/mol, soit plus du double de la liaison C-O (ce qui la différencie de la liaison C=C, dont l'énergie est inférieure au double de l'énergie d'une liaison C-C).
Géométrie
- Longueur : environ 120 pm. Il s'agit d'une liaison courte, donc forte.
- Géométrie VSEPR : la liaison C=O et les deux autres atomes liés au carbone présentent une géométrie de type trigonale plane (angles d'environ 120°).
Polarité
La liaison C=O est fortement polarisée et les molécules qui la comportent (en particulier les aldéhydes et cétones) présentent donc des moments dipolaires importants (accentués par les doublets libres de l'oxygène). Ceux-ci sont en général compris dans l'échelle 1.5 - 4 Debye.
Spectroscopie
- Infra-rouge
La liaison C=O des composés carbonylés présente une bande forte comprise entre 1690 et 1 750 cm−1 (vibration d'élongation de la liaison C=O). Elle peut parfois descendre sous 1 700 cm−1 en cas de phénomènes de conjugaison.
Pour les aldéhydes, deux bandes moyennes de valence de C-H (dans CHO) comprise entre 2 750 et 2 900 cm−1.
RMN du proton : uniquement pour les aldéhydes, = 9.5 - 10
Ce proton est fortement déblindé du fait de la circulation des électrons de la double liaison C=O.
Usages chimiques
Solvants
- Les composés carbonylés sont des composés aprotiques et polaires. Les aldéhydes sont trop réactifs pour être utilisés comme solvants. Par contre, certaines cétones, notamment l'acétone (propan-2-one) et la butan-2-one (ou méthyléthylcétone, MEK) sont d'un emploi courant comme solvant polaire aprotique. Si la fonction carbonyle possède un hydrogène en alpha du carbone, alors il y a possibilité d'un équilibre avec l'énol correspondant ; le solvant est alors légèrement protique du fait de cet hydrogène à caractère acide. Bien que cette réaction soit lente, cette réaction devient problématique en présence de base forte, ces solvants ne seront donc pas employés dans ces conditions et on leur préférera d'autres solvants aprotiques polaires, comme le diméthylsulfoxyde (DMSO), le N,N-diméthylformamide (DMF) ou l'acétonitrile.
- Vu que seul l'atome d'oxygène peut participer aux liaisons hydrogène, la solubilité de ces composés dans l'eau est limitée. Elle l'est d'autant plus que la chaine carbonée (hydrophobe) est longue. Ainsi l'acétone est miscible (soluble en toutes proportions) avec l'eau mais au-delà d'une chaine de six atomes de carbone, la solubilité devient infime.
Composés carbonylés énolisables
Les composés carbonylés énolisables sont des composés carbonylés ayant au moins un atome d'hydrogène sur le carbone en α de la fonction carbonyle. Ainsi peut se produire un équilibre de tautomérie entre le composé carbonylé et l'énol correspondant, c'est-à-dire un alcène avec une fonction alcool en position vinylique.
Équilibre céto-énolique :
Notes et références
- « IUPAC Gold Book - carbonyl compounds », sur goldbook.iupac.org (consulté le )
Voir aussi
- Portail de la chimie