Hémine
L'hémine (hème de chlorure ferrique) est une porphyrine, contenant du fer et du chlore, qui peut être formée à partir d'un groupe hémique, comme l'hème b présent dans l'hémoglobine du sang humain.
| Hémine | |
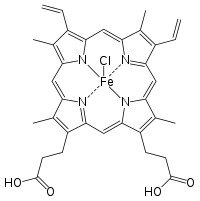
| |
| Identification | |
|---|---|
| Nom UICPA | 18-(2-carboxyéthyl)-8,13-bis(éthényl)-3,7,12,17-tétraméthylporphyrin-21,24-diid-2-yl]propanoate de chloro-ferIII |
| Synonymes |
panhématine, chlorohémine |
| No CAS | |
| No ECHA | 100.036.475 |
| No CE | 240-140-1 |
| Code ATC | |
| PubChem | 455658 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C34H32ClFeN4O4 |
| Masse molaire[1] | 651,94 ± 0,035 g/mol C 62,64 %, H 4,95 %, Cl 5,44 %, Fe 8,57 %, N 8,59 %, O 9,82 %, |
| Précautions | |
| SGH[2] | |
  |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| Hémine | |

| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.036.475 |
| DrugBank | 03404 |
Propriétés chimiques
L'hémine est une molécule de protoporphyrine IX contenant un ion ferrique (Fe3+) avec un ligand chlorure.
Chimiquement, l'hémine diffère de l'hématine composée d'hème apparentée principalement par le fait que l'ion de coordination est un ion chlorure dans l'hémine, tandis qu'il s'agit d'un ion hydroxyde dans l'hématine[3]. L'ion fer dans l'hème est sous forme d'ion ferreux (Fe2+), alors qu'il s'agit de l'ion ferrique (Fe3+) dans l'hémine et l'hématine.
L'hémine est produite de manière endogène dans le corps humain, par exemple lors du renouvellement des globules rouges. Il peut se former de manière inappropriée à la suite d'une hémolyse ou d'une lésion vasculaire. Plusieurs protéines du sang humain se lient à l'hémine, comme l'hémopexine et l'albumine sérique.
Utilisation pharmacologique
Une forme lyophilisée d'hémine est utilisée comme agent pharmacologique dans certains cas pour le traitement des attaques de porphyrie, en particulier dans la porphyrie aiguë intermittente. L'administration d'hémine peut réduire les déficits hémiques chez les patients concernés, supprimant ainsi l'activité de l'acide delta-amino-lévulinique synthase (une enzyme clé dans la synthèse des porphyrines) par rétroaction biochimique, ce qui à son tour réduit la production de porphyrines et de précurseurs toxiques de l'hème. Dans de tels cas pharmacologiques, l'hémine est généralement formulée avec de l'albumine humaine avant d'être administrée par un professionnel de la santé, afin de réduire le risque de phlébite et de stabiliser le composé, qui est potentiellement réactif s'il circule sous forme libre. Ces formes d'hémine sont vendues sous une gamme de noms commerciaux dont les marques Panhematin[4] et Normosang[5].
Synthèse
L'hémine a d'abord été cristallisé dans le sang en 1853, par Ludwik Karol Teichmann. Ce dernier a découvert que les pigments sanguins pouvaient former des cristaux microscopiques. Ainsi, les cristaux d'hémine sont parfois appelés « cristaux de Teichmann ». Hans Fischer a synthétisé l'hémine et a reçu le prix Nobel de chimie en 1930[6] La méthode de Fischer consiste à traiter le sang défribré avec une solution de chlorure de sodium dans de l'acide acétique[7].
Utilisation en médecine
L'hémine peut être produite à partir de l'hémoglobine par le test de Teichmann, lorsque l'hémoglobine est chauffée avec de l'acide acétique froid (saturé de sérum physiologique). Cela peut être utilisé pour détecter des traces de sang.
Autre
L'hémine est considérée comme le « facteur X » nécessaire à la croissance de Haemophilus influenzae[8].
Voir aussi
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- PubChem CID 455658.
- Grenoble DC et Drickamer HG, « The Effect of Pressure on the Oxidation State of Iron, III. Hemin and Hematin », Proceedings of the National Academy of Sciences USA, vol. 61, , p. 1177–1182 (PMID 5249803, PMCID 225235, DOI 10.1073/pnas.61.4.1177, lire en ligne)
- « Panhematin for Acute Porphyria », American Porphyria Foundation
- « Normosang », Electronic Medicines Compendium (eMC)
- « Hans Fischer - Nobel Lecture - On haemin and the relationships between haemin and chlorophyll », Nobel Prize Foundation
- Hans Fischer, « Hemin », Org. Synth., vol. 21, , p. 53 (DOI 10.15227/orgsyn.021.0053)
- Sherris, John C., Ryan, Kenneth J. et Ray, C. L., Sherris medical microbiology: an introduction to infectious diseases, New York, McGraw-Hill, , 395 p. (ISBN 0-8385-8529-9)
Liens externes
- Informations de l'American Porphyria Foundation, y compris les informations de livraison d'urgence
- Hemin chez RxList
- (en) MeSH Hemin
- Portail de la chimie