Isomérie de spin du dihydrogène
L'orthohydrogène est du dihydrogène composé de molécules dans lesquelles les deux protons (un dans chaque atome de la molécule) ont des spins parallèles et de même sens.
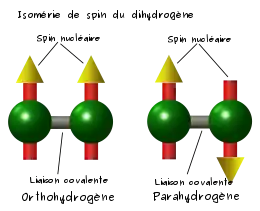
Le parahydrogène est du dihydrogène composé de molécules dans lesquelles les deux protons (un dans chaque atome de la molécule) ont des spins antiparallèles.
Ces deux formes du dihydrogène sont appelées des isomères de spin (nucléaire).
Orthohydrogène et parahydrogène
Les molécules de dihydrogène sont constituées de deux atomes d'hydrogène liés par une liaison covalente. Si on néglige les traces de deutérium ou de tritium qui pourraient être présentes, chaque atome d'hydrogène ne comprend qu'un proton et un électron. Le proton a un moment magnétique associé appelé spin, que l'on peut considérer comme généré par la rotation du proton sur lui-même (même si cette représentation est complètement fausse au sens de la physique quantique). La molécule peut donc contenir deux protons alignés soit dans une même direction (c'est l'orthohydrogène) ou dans des directions opposées (c'est le parahydrogène). Par contre dans une molécule stable de H2, les électrons sont forcément alignés dans des directions opposées pour faire une liaison chimique.
Le spin nucléaire total des deux noyaux de l'orthohydrogène est I = 1, de sorte que c'est un état triplet avec trois valeurs possible de la composante de spin sur un axe défini, à savoir MI = 1, 0 ou −1. Les fonctions d'onde de spin nucléaire qui y correspondent sont α1α2, (α1β2 + β1α2)/(21/2), et β1β2 (où α et β sont les états de spin d'un seul proton de MI = +1/2 et -1/2 respectivement). Le parahydrogène par contre est un état singulet avec nombres quantiques de spin nucléaire I = 0 et MI = 0 et fonction d'onde (α1β2 – β1α2)/(21/2). À température ambiante l'orthohydrogène est trois fois plus abondant, en conséquence de sa dégénérescence de spin nucléaire.
Le proton est un fermion ; la fonction d'onde totale de la molécule doit donc être antisymétrique par rapport à la permutation des deux protons. Cette condition impose une restriction sur les niveaux rotationnels possibles de chaque forme de H2. Le parahydrogène possède une fonction d'onde antisymétrique de spin nucléaire et doit alors posséder une fonction d'onde rotationnelle symétrique. Il est restreint alors aux niveaux rotationnels pairs (nombre quantique rotationnel J = 0, 2, 4, 6, ...). L'orthohydrogène par contre possède une fonction symétrique de spin nucléaire et alors une fonction rotationnelle antisymétrique, ce qui le restreint aux niveaux rotationnels impairs (J = 1, 3, 5, 7, ...). À basse température presque tout l'orthohydrogène est au niveau J = 1.
L'orthohydrogène au niveau J = 1 est instable à basse température et se transforme spontanément en parahydrogène au niveau J = 0 avec le temps, ce qui libère une chaleur indésirable. À température ambiante, l'hydrogène comprend 75 % d'orthohydrogène, proportion que le processus de liquéfaction préserve. Il faut soit utiliser un catalyseur pour accélérer la conversion de l'hydrogène en parahydrogène, soit fournir une réfrigération supplémentaire pour absorber la chaleur qui se dégagera de l'hydrogène liquide au fur et à mesure de sa conversion spontanée.
Source
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Spin isomers of hydrogen » (voir la liste des auteurs).
- Portail de la physique
- Portail de la chimie