Manchon à incandescence
Un manchon à incandescence, ou manchon Auer, est une gaine de tissu combustible imprégnée d'oxydes de terres rares et/ou thorium, dont on entoure la flamme d'un bec de gaz afin d'en accroître l'éclat[1] ; on parle alors de bec Auer.



Les manchons à incandescence ont été utilisés à partir de la dernière décennie du XIXe siècle pour éclairer les rues des villes, principalement en Europe et en Amérique du Nord, ainsi que les phares maritimes. Ils sont toujours utilisés dans les lampes de camping ou de chantier à essence, à pétrole (lampes à pression) ou à gaz (méthane, butane, propane ou mélange de ces gaz).
Par sa forte puissance lumineuse, le manchon incandescent est, aujourd'hui encore, seul à concurrencer l'éclairage électrique lorsque le réseau est inexistant ou défaillant.
Principe de fonctionnement
Le manchon à incandescence contient des oxydes de cérium et thorium, qui, lorsqu'ils sont chauffés, brillent fortement dans le spectre visible, tout en émettant peu de rayonnements infrarouges (en comparaison avec un corps noir). On chauffe ainsi par une flamme de pétrole ou de gaz le manchon pour maximiser l'apport de lumière utile.
Les manchons à incandescence modernes sont fabriqués en saturant un textile, soie artificielle ou viscose, avec des oxydes de cérium et/ou thorium. Le manchon ressemble à un petit filet souple, composé d'une texture de coton, soie ou matière synthétique imbibée de sels, qui doit être brûlé à la première utilisation et laisse alors un fin réseau d'oxydes réfractaires (incombustibles) propres à briller fortement par incandescence sans toutefois se consumer. Le manchon ainsi brûlé devient très fragile : on ne doit alors ni le toucher, ni le secouer trop fortement.
Histoire
Découverte de la lumière à incandescence
Avant le XIXe siècle, la lumière artificielle avait toujours été produite par une flamme. La lumière oxhydrique, inventée vers 1820, fut surtout utilisée pour l'éclairage des scènes de théâtre, mais la trop forte température requise en rendait l'utilisation difficile pour de petites lampes. Vers la fin du XIXe siècle, plusieurs inventeurs ont tenté de développer une alternative efficace en chauffant des matériaux à des températures plus faibles, mais en utilisant des raies spectrales pour simuler une lumière blanche.
De nombreuses tentatives avec de la gaze de platine-iridium trempée dans des nitrates de différents métaux se révélèrent infructueuses du fait du coût élevé des matériaux et d'une faible durabilité.
Le premier manchon à incandescence efficace fut le Clamond basket en 1881, qui porte le nom de son inventeur. Il fut exposé au Crystal Palace en 1883. Cet appareil était fait d'un mélange d'hydrate de magnésium, d'acétate de magnésium et d'eau qui était pressé à travers une plaque perforée, de manière à former un filet, qui était brûlé. L'acétate se consumait et les produits de la combustion formaient une matrice apte à maintenir en forme l'oxyde de magnésium résultant de la décomposition de l'hydrate. Cette structure très fragile était supportée par une grille de platine, et le tout était chauffé au gaz de houille.
Le manchon à incandescence moderne est l'une des nombreuses inventions du chimiste autrichien Carl Auer von Welsbach, qui expérimenta les terres rares vers 1880, après avoir étudié auprès de Robert Bunsen. Son premier procédé utilisait un mélange de 60 % d'oxyde de magnésium, 20 % d'oxyde de lanthane et 20 % d'oxyde d'yttrium, qu'il appela Actinophor, et breveta en 1885.
Les premiers manchons donnaient une lumière verdâtre et n'étaient pas très constants dans leurs résultats[2]. Sa première société, dont l'usine fut établie en 1887 à Atzgersdorf, dans la banlieue de Vienne (Autriche), connut l'échec en 1889. En 1890, Auer découvrit que le thorium était préférable au magnésium et, en 1891, il mit au point un mélange à 99 % de dioxyde de thorium et 1 % de dioxyde de cérium, qui produisait une lumière beaucoup plus blanche et des manchons plus solides. Après son introduction commerciale en 1892, ce nouveau produit se répandit à travers l'Europe. Le manchon à incandescence resta un mode très répandu d'éclairage urbain, qui réussit à se maintenir en concurrence avec l'éclairage électrique jusqu'au milieu du XXe siècle.
Évolution de la fabrication des manchons
Au début, pour produire un manchon à incandescence, du coton était tissé en un filet ressemblant à un petit sac, et imprégné de nitrates solubles de ces métaux. Lors de la première utilisation, le coton brûle et les nitrates sont convertis en nitrites qui fusionnent ensemble pour former une sorte de grille solide. Avec la chaleur, les nitrites se décomposent pour donner les oxydes, dont la température de fusion est très élevée. Ils sont solides mais fragiles.
Chaque manchon à incandescence est vendu sous la forme du filet de coton non brûlé, car la structure en oxyde était trop fragile pour être transportée facilement, et l'acheteur doit effectuer la transformation lui-même, par la simple action d'une allumette avant la première utilisation. Dans les premiers manchons, le coton moisissait rapidement, à cause de la nature corrosive et acide des nitrates de métaux. Ce phénomène fut réduit par la suite par le trempage des manchons dans une solution d'ammoniaque pour neutraliser l'excès acide.
Plus tard, les manchons à incandescence furent fabriqués à partir de nitrocellulose ou de collodion, plutôt que de coton ordinaire, car on pouvait en produire des fils extrêmement fins. Ils étaient convertis en cellulose avant d'être chauffés (car ces matériaux sont très inflammables) en les trempant dans du sulfite d'ammonium.
Il fut découvert que le manchon à incandescence pouvait être vendu préconsumé en le renforçant par immersion dans une solution de collodion : le manchon se trouvait ainsi enrobé d'une fine couche de vernis qui brûlait lorsque le manchon était utilisé pour la première fois. De nos jours, les manchons à incandescence disponibles dans le commerce sont toujours vendus dans leur forme de fabrication d'origine, non préconsumés.
Les manchons à incandescence sont ordinairement pourvus d'un fil d'amiante destiné à les attacher au bec de la lampe, mais du fait de l'action cancérigène de l'amiante, celui-ci est souvent remplacé de nos jours par un fil d'acier, (dans la lampe Northstar de Coleman, par exemple) ou parfois de céramique[3].
Le phénomène physico-chimique de l'incandescence
Selon la loi du rayonnement de Kirchhoff, les flammes à gaz éclairent très peu parce qu'elles ont un degré d'émission en lumière visible à peu près nul. Les lampes à gaz à fonction d'éclairage ont donc d'abord été alimentées par des gaz charbonneux tels que le benzol qui produisent, comme le fait une bougie, une lumière rougeoyante jaunâtre générée par l'incandescence des particules de fumée de carbone (suie) mis en suspension.
On obtient une lumière plus blanche si l'on chauffe de manière permanente certains composés chimiques résistants à l'oxygène. Le chimiste autrichien Carl Auer von Welsbach eut l'idée d'imbiber un réseau de coton avec des solutions de sels de cérium et thorium qu'il brûlait avec précaution de manière à obtenir un résidu de coton combiné avec des oxydes. Il déposa le brevet de ce procédé en Allemagne le sous le nom de « manchon à incandescence Auer » (Auer-Glühstrumpf).
Les manchons étaient alors fabriqués en tissu trempé dans une solution de 99 % de nitrate de thorium et de 1 % de nitrate de cérium, qu'on enflammait ensuite. Par la chaleur, le nitrate de thorium se décomposait en oxyde de thorium et gaz nitreux. Il en subsistait une structure fragile qui, soumise à la flamme du gaz, émettait une lumière blanche. Cette lumière n'a rien à voir avec la faible radioactivité du thorium, il s'agit d'une incandescence tout à fait ordinaire produite par la chaleur de la flamme à gaz.
Carl Auer von Welsbach a tout d'abord procédé à des essais avec l'oxyde de magnésium, puis le dioxyde de zirconium, puis des combinaisons de lanthane, yttrium et praséodyme. Ils ont tous une capacité d'absorption modérée dans la zone visible du spectre et produisent une lumière d'un brun blanchâtre. La percée eut lieu pour lui avec l'oxyde de cérium et le dioxyde de thorium, qui s'avérèrent d'une bien meilleure stabilité. La composition de 1 % de CeO2 pour 99 % de ThO2 fut donc retenue pour la fabrication des manchons, mais elle a été remplacée il y a quelques décennies par un mélange d'oxyde d'yttrium et d'oxyde de cérium, de manière à éviter les manipulations de ThO2, produit légèrement radioactif.
Il existe de nombreux modèles de manchons à incandescence, les plus connus étant probablement ceux à double fixation des lanternes de camping à gaz butane/propane ou ceux à simple fixation des « Petromax » et autres lampes à pression, que l'utilisateur doit lui-même brûler avant de les mettre en service. On a abandonné la fabrication des anciens manchons pour réverbères à gaz verticaux ou suspendus, qui étaient déjà préconsumés en usine et imprégnés d'un vernis de nitrate de cellulose pour une plus grande solidité durant le transport. Cette couche de vernis brûlait très rapidement à la première mise en service. La plupart des manchons sont suspendus, en forme de sachets piriformes, mais il en existe aussi en forme de tube pour certaines lampes à essence ou à gaz (« Coleman ») ou de forme ogivale, destinés aux anciennes lampes à essence ou à alcool (« Tito-Landi »), ou bien coniques, pour les lampes atmosphériques à pétrole américaines (« Aladdin »), encore en fabrication et fournissant une lumière plus généreuse que les simples lampes à pétrole classiques. Dans ce dernier cas, la suspension du manchon ou sa fixation sur le brûleur de la lampe sont souvent facilitées par une ossature faite de pièces formées en oxyde de magnésium.
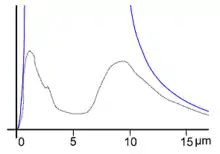
L'émission thermique d'un manchon Auer (ligne pointillée sur le diagramme), est nettement inférieure à celle d'un corps noir (ligne bleue). Le rayonnement se concentre sur les ondes courtes du domaine visible. En conséquence, l'éclairage par manchon à incandescence nécessite une température plus élevée que celui dont il aurait besoin si son rayonnement était continu. Le rouge est ainsi réduit, et la lumière apparaît plus blanche.
Le rendement lumineux des manchons à incandescence est encore accru par les échanges importants d'énergie chimique entre la flamme et le réseau textile garni de cérium : pour preuve, des manchons simplement chauffés dans un four ne deviennent jamais aussi lumineux que lorsqu'ils sont placés au contact direct d'une flamme.
Précautions à prendre concernant le thorium
Le thorium étant radioactif et produisant naturellement un gaz, le radon 220, qui l'est aussi[4], quelques inquiétudes ont été exprimées sur la sûreté des manchons à incandescence. Certaines organisations de santé font du reste des recommandations sur leur usage[5].
Une étude menée en 1981 estime que la dose reçue en utilisant des manchons à incandescence au thorium chaque week-end pendant une année serait de 0,3 à 0,6 millirems, très faible en comparaison avec la dose normale annuelle, de quelques centaines de millirems. Une personne ingérant un manchon à incandescence entier recevrait une dose comparable à 200 millirems[6],[7].
La radioactivité est cependant un enjeu majeur pour les personnes impliquées dans la fabrication des manchons et pour la contamination du sol autour des anciennes usines[8]. Ces problèmes liés à la fabrication industrielle des manchons font que des produits alternatifs, habituellement l'yttrium, parfois le zirconium, sont utilisés dans certains pays, même s'ils sont plus onéreux et un peu moins efficaces.
Une source d'inquiétude potentielle est que les particules de thorium des manchons à incandescence se désagrègent au fil du temps et se retrouvent dans l'air où elles peuvent être inhalées, ou bien ingérées en retombant sur la nourriture, et se fixer dans les poumons ou le foie[9].
Par précaution, et malgré la faible radioactivité des manchons à incandescence, il est donc recommandé de changer les manchons à l'écart de la nourriture et d'éviter de respirer les poussières et les fumées issues de leur première combustion.
Notes et références
- Définitions lexicographiques et étymologiques de « manchon » dans le Trésor de la langue française informatisé, sur le site du Centre national de ressources textuelles et lexicales
- Traité de chimie minérale, p. 867
- Traité de chimie minérale, p. 869
- Produit naturel de la décomposition du thorium. Les produits issus de la décomposition du thorium incluent le radium, l'actinium, et le gaz radon (source : article Radon).
- Radioactivity in Lantern Mantles, Australian radiation Protection and Nuclear Safety Agency
- Aladdin Mantle Info, Survival Unlimited
- Are camp lanterns radioactive?
- A Practitioner's Guide to Patients' Environmental Exposures, New Jersey Department of Health, 1996
- Dangers en cas d'ingestion de thorium
Sources
- A Brief History of the Incandescent Mantle Pressure Lamp
- 1911 Encyclopedia article on lighting
- Gutenberg project - Scientific American October 2, 1886, article on the Clamond Gas Burner
- Auer von Welsbach
- Australian Radiation Protection and Nuclear Safety Agency article "Radioactivity in Lantern Mantles"
- The Straight Dope - Are camp lanterns radioactive?
- Document at New Jersey Consumer and Environmental Health Services containing a description of contamination at former factory site at Camden, New Jersey
Voir aussi
Bibliographie
- Paul Truchot, L'éclairage à incandescence par le gaz et les liquides gazéifiés, 1899
- J. Claypole, The Incandescent Mantle: Hesitant and Complex Beginnings, The Midnight Oil, Issue 23, Spring 1996
- Louis le Cunff, Feux de Mer, 1992, 248 pages, p. 31
- Workshop Receipts, for Manufacturers and Scientific Amateurs
- Éclairage à la chaux (limelight) : Drummond, 1826
- Lumière Drummond. Lumière oxhydrique
- Workshop Receipts, for Manufacturers and Scientific Amateurs
Liens externes
- Lampes à pétrole et histoire de l'éclairage
- Histoire de l'éclairage
- Les lampes à pression : histoire, technique, utilisation
- The International Guild of Lamp Researchers
- Portail de la chimie
- Portail de la physique