Radon
Le radon est l'élément chimique de numéro atomique 86, de symbole Rn. C'est un gaz noble (ou gaz rare) radioactif, incolore, inodore et d'origine le plus souvent naturelle. C'est l'une des substances les plus denses capables de persister sous forme de gaz dans les conditions normales de température et de pression.
Cet article concerne l'élément chimique. Pour les autres significations, voir Radon (homonymie).
Ne doit pas être confondu avec Radium.
Le radon n'existe pas sous forme de corps stable et tous ses isotopes connus sont radioactifs. Son isotope le plus stable est le 222Rn, qui a une demi-vie de 3,8 jours et qui a été utilisé en radiothérapie jusque dans les années 1950[5]. Son intense radioactivité a entravé son étude chimique approfondie, et seuls quelques-uns de ses composés sont bien connus.
L'importance sanitaire du radon tient à sa radioactivité élevée et au fait qu'il est présent partout dans l'atmosphère, il est donc inhalé. Il est souvent le plus gros contributeur à la dose d'un individu pour la radioactivité naturelle, avec cependant de fortes disparités géographiques. Il est ainsi la principale source d'exposition naturelle des populations humaines, animales et de la partie aérienne des plantes aux rayonnements ionisants. En France, il est susceptible d'être inhalé à doses élevées dans les lieux peu aérés (logements) des territoires où il est particulièrement présent (Limousin, Jura, etc.).
Histoire
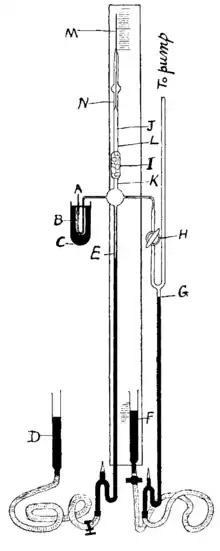
En 1908, William Ramsay et Robert Whytlaw-Gray isolent ce qu'ils appellent le « niton » (nitens en Latin, traduit par brillant, a le symbole Nt) et déterminent sa densité. Le radon a son nom depuis 1923.
Dès 1899, Pierre et Marie Curie observent que le « gaz » émis par le radium reste radioactif pendant près d'un mois[6]. Au cours de cette même année, Robert Bowie Owens (en) et Ernest Rutherford relèvent des résultats variables quand ils tentent de mesurer les radiations d'oxydes de thorium[7].
Rutherford note que les composés de thorium émettent continuellement un gaz radioactif, qui conserve sa radioactivité plusieurs minutes ; il nomme ce gaz « emanation » (du latin emanare, émaner, et emanatio, expiration)[8], et plus tard, émanation de thorium (ThEm).
Le radon a été découvert en 1900 par Friedrich Ernst Dorn qui l'a appelé « émanation de radium ». Ce fut le troisième élément radioactif découvert, après le radium et le polonium.
En 1900, Dorn rend compte d'expériences montrant que des composés de radium émane un gaz radioactif, qu'il baptise « émanation de radium » (RaEm)[9].
En 1901, Rutherford démontre que les émanations de thorium sont radioactives, mais crédite les Curie de la découverte de cet élément[10].
En 1903, des émanations similaires provenant de l'actinium sont observées par André-Louis Debierne[11],[12], et il les baptise « émanation d'actinium » (AcEm).
Des noms furent proposés pour ces trois gaz en 1904 : exradio, exthorio, et exactinio[13] ; puis radon, thoron, et akton ou acton en 1918[14] ; suivis de radéon, thoréon, et actinéon en 1919[15], et finalement radon, thoron, et actinon en 1920[16].
Constatant la similitude du spectre de ces trois gaz avec celui de l'argon, du krypton et du xénon, ainsi que leur inertie chimique, Sir William Ramsay suggéra en 1904 que ces émanations pouvaient correspondre à un nouvel élément de la famille des gaz rares. Rutherford et Soddy avaient émis une supposition similaire dès 1901 sur la base du manque de réactivité chimique de l'émanation du thorium[17].
En 1910, Sir William Ramsay et Robert Whytlaw-Gray parviennent à isoler le radon. Ils déterminent sa densité, et montrent qu'il s'agit du gaz le plus dense connu à l'époque. Ils notent que « l'expression l'émanation du radium est fort incommode », et proposent comme nouveau nom niton (du latin nitens, nitentis, brillant) pour rappeler la propriété qu'a ce gaz de rendre phosphorescentes certaines substances[18]. En 1912, cette proposition fut acceptée par la commission internationale des poids atomiques.
En 1923, le comité international des éléments chimiques et l'Union internationale de chimie pure et appliquée choisirent pour ces trois gaz les noms de radon (Rn), thoron (Tn) et actinon (An). Mais par la suite, quand les isotopes furent simplement numérotés et non nommés, l'élément reçut le nom de l'isotope le plus stable, c'est-à-dire le radon. L'isotope Tn devint 220Rn, et l'isotope An devint 219Rn. Mais jusque dans les années 1960, cet élément était simplement appelé émanation[19].
Caractéristiques physiques et chimiques
Caractéristiques physiques
Gaz chimiquement inerte, le radon est le plus « lourd » (le plus dense) des gaz nobles (en ne prenant pas en compte l'oganesson). Dans les conditions normales de température et de pression, le radon est un gaz monoatomique d'une masse volumique de 9,73 kg/m3[20].
C'est l'un des gaz les plus « lourds » (denses) à température ambiante, pratiquement 8 fois la densité de l'air.
À température et pression standard, le radon est incolore, mais lorsque la température est abaissée en dessous de son point de congélation (202 K ; −71 °C), il devient phosphorescent puis jaune si la température baisse encore et finalement rouge-orangé aux températures de l'air liquide (< −180 °C )[21]. Quand il est dans un état condensé, le radon paraît également lumineux, à cause de l'intensité des radiations qu'il dégage. Il est dit « autofluorescent ».
Caractéristiques radiologiques
Il existe 35 isotopes de radon connus jusqu'à ce jour, mais seuls 4 d'entre eux existent dans la nature, à l'état de traces, qui tous se désintègrent suivant le mode alpha. Seul le radon 222 a une demi-vie suffisante pour représenter un problème de radioprotection dans des cas extrêmes.
- L'isotope le plus fréquent (et à plus longue demi-vie) est le radon 222 qui est le produit (isotope-fils) de la désintégration du radium 226, dans la chaîne de désintégration de l'uranium 238. Il a une demi-vie de 3,823 jours.
- Le radon 220 est le principal produit de désintégration du radium 224, dans la chaîne de désintégration du thorium 232. Il fut pour cette raison appelé « thoron ». Il a une demi-vie de 55,6 secondes.
- Le radon 219 est dérivé de l'actinium, il fut appelé « actinon ». Il provient de la série de l'uranium 235. Il a une demi-vie de 3,96 secondes.
- Le radon 218 est un produit très minoritaire (0,10 %) de la désintégration de l'astate 218 (désintégration β−), lui-même produit de désintégration très minoritaire (0,02 %) du polonium 218. Il appartient donc à la chaîne de désintégration de l'uranium 238, mais ne représente que 0,2 ppm de la radioactivité du radon 222. Il a une demi-vie de 35 millisecondes.
Ayant une faible demi-vie (relativement aux autres radionucléides présents en certaine quantité dans la nature), le radon 222 est un gaz extrêmement radioactif. Son activité massique est de 5,73 × 1015 Bq/g.
Composés chimiques
Le radon est un gaz rare, qui entre difficilement en composition chimique. Des expériences indiquent néanmoins que le fluor peut réagir avec le radon pour former du fluorure de radon. L'existence de clathrates du radon a aussi été rapportée.
Le radon dans l'environnement
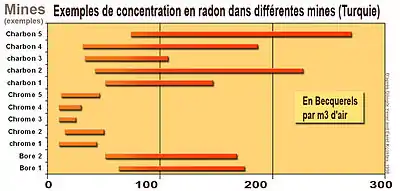
Niveaux mesurés
Les taux de radon observés dans la nature sont si faibles qu'on ne le détecte pas par des analyses chimiques classiques, mais par sa radioactivité.
Une activité de 1 000 Bq par m3 d'air (concentration largement supérieure à ce qui est habituellement observé) traduirait une présence de 0,17 picogramme de radon par mètre cube — soit une concentration molaire de l'ordre d'un millionième de millionième de millionième — alors qu'une concentration relative de l'ordre du millionième est déjà très difficile à détecter. Hors contexte de guerre atomique ou accidentel (Tchernobyl, Fukushima...), toute la radioactivité de l'atmosphère terrestre n'est due qu'à quelques dizaines de grammes de radon[22]. Un air chargé en radon ne change donc pas de composition observable ni de propriétés physico-chimiques (le changement porte sur des « traces de traces de traces »), cependant la présence du radon est détectable à l'aide d'outils appropriés.
Cette faible teneur de l'air en radon est due à sa rapide décomposition radioactive, mais il est en permanence remplacé par un flux de radon libéré par les roches, les mines (d'uranium et de charbon notamment) ou les eaux naturelles qui les traversent.
Formation du flux de radon naturel
Le radon est spontanément présent dans toutes les régions quelle que soit la nature du sol. Sa concentration est plus élevée dans les régions uranifères, notamment granitiques et volcaniques, mais elle n'est pas négligeable même dans les terrains calcaires. La teneur au sol peut dépendre de la circulation des eaux souterraines. En France, selon l'IRSN il « représente le tiers de l'exposition moyenne de la population française aux rayonnements ionisants »[23] ; les régions riches en radon sont la Bretagne, le Massif central, les Vosges et la Corse.
Le radon se forme par désintégration du radium dans la chaîne de désintégration radioactive de l'uranium et du thorium naturellement contenus dans les roches ou le sol (ou déplacés par l'Homme lors de certaines activités industrielles ou minières).
Ces deux métaux sont présents dans la croûte terrestre depuis sa formation, et leurs isotopes les plus communs ont une très longue demi-vie (~704 Ma pour 235U ; ~4,47 Ga pour 238U ; ~14,1 Ga pour 232Th).
L'uranium et le thorium continueront donc à naturellement produire un flux naturel de radon, pour des milliards d'années, à des concentrations voisines de celles que nous connaissons.
Au moment de sa formation par désintégration, chaque atome de radon est expulsé de sa matrice (grain du matériau), avec une énergie cinétique (ou « énergie de recul ») qui lui permet, dans un minéral de densité moyenne de parcourir de 20 à 70 nm[24]. S'il est proche de la surface d'une roche ou dans un grain fin, il peut se déplacer par diffusion et passer dans l'air ou dans l'eau, mais ce processus étant lent, et le radon ayant une assez courte demi-vie, seul le radon formé en surface des phases solides atteindra l'air ou l'eau avant de se désintégrer. L'eau, (chaude et acide notamment) peut aussi solubiliser la roche et se charger de radon[24]. Dans les sols les plus communs, selon l'INERIS, 10 à 50 % du radon s'échappe du grain où il est produit et passe dans les pores et éventuellement l'air ou l'eau interstitielle[24]. Le coefficient d'Oswald (dit coefficient de Bunsen quand il concerne l'eau), est le rapport de l'activité volumique du radon dans l'eau à son activité volumique dans l’air[24] ; ce coefficient α est une fonction décroissante de la température de l’eau T :
- (T exprimée en °C)
Par exemple à 20 °C :
Le flux naturel de radon est normalement piégé dans la roche qui lui donne naissance, et sa demi-vie très courte (de l'ordre de quatre jours) interdit une accumulation au sens propre du terme. Cependant, son caractère gazeux le rend potentiellement mobile. Les activités humaines (mines et combustion du charbon, certaines sécheresses induites par l'homme) peuvent augmenter la libération de radon, et les constructions humaines peuvent l'aspirer et lui permettre de stagner localement, conduisant à des concentrations importantes. Une bonne ventilation est alors nécessaire. Le radon se trouve ainsi en concentration importante dans les mines souterraines et parfois dans les caves (dans certaines zones minières ou granitiques). Il peut aussi être trouvé dans certaines eaux de source et sources chaudes[25].
Le radon dégaze du sol en quantités plus ou moins importantes[26]. On peut mesurer sa radioactivité ou tenter d’en faire une mesure quantitative[27]. Le niveau de radon dans l'air est habituellement plus faible en zone urbaine qu'en zone rurale, en raison de sols plus imperméabilisés.
La concentration du radon dans l'atmosphère est si faible que des eaux naturellement riches en radon le perdent au contact de l'air. De ce fait, les nappes d'eaux souterraines, en contact direct avec les roches où le radon est produit, sont plus chargées en radon que les eaux de surface. De même, dans les sols, la zone saturée en eau a une concentration plus forte que la zone aérée, en contact indirect avec l'atmosphère[28],[29].
Le radon dans la pluie
Les eaux météoriques peuvent parfois être intensément radioactives à cause de niveaux élevés de radon et ses descendants 214Bi et 214Pb, au point de perturber les outils de surveillance radiologique des centrales nucléaires[30].
Les niveaux les plus élevés sont trouvés dans les pluies d'orage. Une hypothèse est que le radon se concentre dans les zones orageuses en raison de sa charge électrique atomique positive. De plus les orages apparaissent en été quand les sols sont plus chauds et/ou desséchés et relarguent le plus de radon[31]. Des estimations de l'âge des gouttes d'eau ont ainsi pu être obtenues en mesurant l'abondance isotopique des descendants du radon à vie courte dans la pluie[32].
Radon et pétrole
Le radon est présent dans les roches pétrolifères, et l'eau de mer ou la boue utilisée comme fluide dans les forages pétroliers peut se charger de précurseurs du radon. Dans l'eau de mer introduite dans les puits comme fluide de mise en pression, le baryum et le strontium sursaturent l'eau en baryum et en solution de sulfate de strontium. Avec la décompression brutale de l'eau de mer remontant dans le tuyau, le baryum et le strontium tendent à précipiter et former des cristaux qui se déposent sur le métal du tuyau. Ils y forment alors des couches de tartre radioactif qui endommagent les tuyaux (le radon peut apparaître dans ce tartre, et y laisser ses produits de désintégration radioactifs). Pour limiter ce risque, les pétroliers cherchent à supprimer les sulfates de l'eau de mer injectée et à en contrôler l'acidité. Des membranes nanofiltrantes suppriment aussi les particules siliceuses et bactériennes, ce qui réduit encore le risque de formation de tartre et de biofilms[33].
De plus, les raffineries pétrolières séparent les produits pétrochimiques grâce à leur point d'ébullition, or le radon a une courbe de pression/température proche de celle du propane et il atteint son point d'ébullition à la même température que le propane, ce qui explique que la zone de l'usine où le propane est traité est souvent l'une des zones les plus radioactives de l'usine. En se désintégrant dans le tuyau de propane fraîchement produit, le radon y forme des radioisotopes solides qui se déposent sur le métal et qui peuvent revêtir la totalité de l'intérieur des tuyauteries de gaz[34].
On trouve donc aussi du radon dans les résidus de l'industrie du pétrole et du gaz naturel.
Le radon souterrain et minier
Sans surprise, on trouve du radon dans les roches profondes. Il peut s'accumuler dans les cavités minières[35] et contaminer l'air et l'eau qui circule dans les galeries en service ou abandonnées[36]. Il est aussi présent dans le pétrole et le gaz naturel extraits des puits creusés dans ces roches.
Le radon percole dans le sol, d'autant plus vite et facilement que le sol est perméable. Il circule au sein de substrats homogènes par diffusion moléculaire et advection/convection en tendant à se répartir de manière uniforme, mais en réalité il diffuse préférentiellement et bien plus rapidement dans les fissures, failles et fractures de la roche, ou avec l'eau qui y circule[24].
À la différence de ses descendants qui sont des aérosols solides s'attachant aux particules fines de l'air[24] et susceptibles de se fixer dans les poumons, il a heureusement peu d'affinité avec la matière organique ou les mucus, ce qui laisse penser que tant qu'il ne s'est pas désintégré, il ne fait que passer dans le sol, avec peu d'impacts mutagènes, et qu'il ne gagne pas la sève des plantes via les racines (par contre il pourrait être absorbé par les feuilles lors de leur respiration, via les stomates) notamment les feuilles proches du sol.
Son comportement dans le sol a fait l'objet d'études dans le cadre de la gestion des déchets radioactifs (qui peuvent générer d'importantes quantités de radon)[37]. Plus encore qu'en surface, la principale source d'exposition au rayonnement dans les mines d'uranium et de charbon est le radon et ses produits de désintégration[38],[39] (le radon est source de 29 % environ de l'exposition totale[40] et d'environ 69 % de la radioactivité naturelle interne dues à des particules inhalées et 59 % de la dose due aux rayonnements d’origine naturelle[24]) à laquelle nous sommes exposés en surface).
Le polonium 218 et le polonium 214 sont en réalité les deux produits les plus cancérigènes générés par le radon, plus que le radon lui-même pour la dose radioactive délivrée aux poumons[41].
Les eaux souterraines, dont thermales
Les eaux souterraines se chargent de radon au contact des roches qui en libèrent, soit en profondeur, soit au contact de roches anciennes présentes en surface (du granite par exemple). Le radon s'échappe de l'eau dès que celle-ci est en contact avec l'air libre, y compris dans certaines stations thermales[42]. Les eaux thermales peuvent en contenir assez pour émettre des centaines à des dizaines de milliers de becquerels par litre[43]. Le radon peut aussi se retrouver concentré dans certains sites de stockage souterrain, et dans les galeries où sont situés certains captages souterrains de sources minérales[44]. Ainsi des taux courants de plusieurs milliers de Bq/m3 d'air sont mesurés dans les salles d'hydrothérapie utilisant des eaux souvent naturellement chargées en radon. Ces taux atteignent même des centaines de milliers de Bq/m3 d'air dans certaines grottes thermales[42].
Les teneurs en radium 226 des eaux minérales varient de quelques millibecquerels à quelques becquerels par litre, avec environ 1 µg d'uranium naturel par litre et souvent moins de 10 µg/l de thorium (peu hydrosoluble en condition normale). Le radon 222 est aussi plus présent que le radium 226 car plus soluble. Il y a jusqu'à 10 000 fois plus de radon 222 que de thorium 226 (exemples à Bad Gastein, Bagnères-de-Luchon, etc.). Une partie du radon peut aussi provenir de l'érosion de roches par les eaux venant de la surface (eaux neptuniennes), expliquant une diminution de la radioactivité de l'eau en période de gel ou de sécheresse et un pic de radioactivité à la fonte des neiges (ex à Bagnères-de-Luchon). L'activité volumique du radon dans les eaux thermales au point d'émergence varie donc beaucoup ; selon la source et parfois selon l'époque de l'année, allant jusqu'à plusieurs dizaines de milliers de Bq/l. Cette activité peut chuter de 80 % entre la source et les bains (par dégazage du radon) quand l'eau passe par un réservoir ou est stockée en piscine, mais elle ne chute pas quand l'eau est directement amenée par tuyaux aux buvettes, étuves, etc.[42].
Au point de prélèvement, dans les provinces carbogazeuses (produisant de l'eau gazeuse chargée en gaz carbonique), le gisement peut produire jusqu'à quatre fois plus de gaz que d'eau (150 m3/h à Royat, contenant du radon et du thoron, « à des teneurs de l'ordre de la dizaine de milliers de becquerels par mètre cube » (Desgranges et collaborateurs, 1978, cités par Améon 2003[42]).
La présence de nombreuses sources thermales dans une région induit souvent une augmentation de la radioactivité moyenne de l'air, avec par exemple à Misasa au Japon (où l'on trouve 70 sources thermales), environ 1,3 GBq de radon sont émis par jour dans l'air à partir de l'eau et du sol.
L'air y est deux fois plus radioactif qu'ailleurs en l'absence de telles sources. Ainsi il a déjà été mesuré en 1962 dans le parc thermal et le jardin de l’hôtel de Luchon une activité volumique du radon de 30 Bq/m3, soit 3 fois plus élevée que la normale (10 Bq/m3 selon UNSCEAR 2000)[42]. L'exposition d'un curiste est généralement de moins de 2 mSv/an, mais peut parfois être « non négligeable du point de vue de la radioprotection ». Les médecins et une partie du personnel (dont le personnel d'entretien la nuit, quand l'aération est moindre) peuvent aussi subir une exposition chronique non négligeable[42].
En Europe, les eaux thermales et potables les plus radioactives sont trouvées en Europe centrale[42], une des plus radioactives étant la source de l’île d'ikaria en Grèce[45]. La directive 96/29/Euratom a inclus le thermalisme comme étant une activité professionnelle durant laquelle les travailleurs sont exposés à des sources naturelles de rayonnement ionisant.
Échelle de concentration
| Bq/m3 | pCi/L | Exemples de concentrations de radon dans l'environnement naturel ou artificiel |
|---|---|---|
| 1 | ~0,03 | La radioactivité due au radon aux abords des grands océans est d'environ 1 Bq/m3, et aux concentrations détectées au-dessus des océans ou en Antarctique le radon émet moins de 0,1 Bq/m3. |
| 10 | 0,27 | La concentration moyenne de l'air extérieur sur les continents est source de 10 à 30 Bq/m3.
Sur la base d'études de surveillance, la radioactivité due au radon de l'air intérieur est estimée être 39 Bq/m3 (avec de fortes variations régionales). |
| 100 | 2.7 | Exposition domestique. La plupart des pays ont adopté 200–400 Bq/m3 comme seuil d'action pour l'air intérieur ou comme niveau de référence. Si les tests montrent des niveaux de radioactivité inférieurs à 4 picocuries par litre d'air pour le radon (160 Bq/m3), aucune action n'est considérée comme nécessaire.
Une exposition cumulée de 230 Bq/m3 au gaz radon durant un an correspond à 1 WLM. |
| 1 000 | 27 | Des concentrations très élevées de radon (> 1 000 Bq/m3) ont été mesurées dans certaines maisons construites au-dessus de mines d'uranium ou sur des sols uranifères ou sur un sol très perméable. Au Canada, à la fin du XXe siècle, à partir de 20 picocuries par litre d'air (800 Bq/m3), il était recommandé de prendre des mesures pour diminuer le taux de radon dans l'air[46], mais on considère maintenant que des actions d'assainissement doivent être entreprises au moins à partir de 200 Bq/m3 d'air intérieur[47]. |
| 10 000 | 270 | Le niveau dit « working level » dans les mines d'uranium correspond à une concentration de 7 000 Bq/m3.
La concentration dans l'air d'une galerie non ventilée du Gastein Healing Gallery approche les 43 kBq/m3 (environ 1,2 nCi/L) avec un maximum de 160 kBq/m3 (environ 4,3 nCi/L)[48]. |
| 100 000 | ~2700 |
Environ 100 000 Bq/m3 (2,7 nCi/L) ont été mesurés dans les parties basses de la maison d'un ingénieur américain, Stanley Watras[49]. |
| 1 000 000 | 27000 | Des émissions de 106 Bq/m3 peuvent être mesurées dans les galeries de mines d'uranium non ventilées. |
Radiotoxicité
Le radon est un émetteur alpha (pour une dose absorbée, les émetteurs alpha font plus de dégâts biologiques que les émetteurs bêta, les rayons gamma ou les rayons X).
À fortes doses, son caractère cancérigène sur les populations exposées de mineurs est statistiquement bien établi, avec ainsi, une surmortalité par cancer pulmonaire qui croît linéairement avec l’exposition cumulée du poumon au radon et à ses descendants[50]. Les études ayant porté sur les mineurs non-fumeurs et travaillant dans des mines sans équipement diesel laissent penser qu'il est un cancérigène pulmonaire humain, même à des taux couramment rencontrés dans l'air intérieur des maisons[51]. La courte durée de demi-vie de ses descendants pourrait expliquer que ces cancers radio-induits semblent cibler les poumons et que les leucémies (de l’adulte, au Royaume-Uni) n’y semblent pas associées[52].
Aux États-Unis, selon l'Agence américaine de protection de l'environnement, il est la seconde cause la plus fréquente de cancer du poumon, après le tabagisme, causant 21 000 morts par cancer du poumon par an aux États-Unis[53].
Enfin, pour l'Organisation mondiale de la santé[54] :
« L’exposition au radon présent dans le sol et les matériaux de construction cause, selon les estimations, entre 3 % et 14 % de l’ensemble des cancers pulmonaires, ce qui en fait la deuxième cause de cancer pulmonaire après la fumée du tabac. »
Histoire
Les premières études sérieuses sur la toxicité du radon se placent dans le contexte des mines d'uranium. Les premières proviennent de la région de Joachimsthal, en Bohême ; d'autres études ont été faites dans la région du sud-est des États-Unis pendant la guerre froide.
Du fait que le radon est un produit de désintégration de l'uranium, les mines souterraines d'uranium peuvent présenter des concentrations élevées de radon. De nombreux mineurs de la zone des Four Corners manifestèrent des cancers du poumon à la suite d'une exposition à des taux élevés de radon pendant les années 1950. L'incidence différentielle des cancers du poumon a été particulièrement élevée chez les mineurs indiens et mormons, parce que ces populations ont normalement des taux de cancer du poumon particulièrement bas. Les normes de sécurité imposant des ventilations performantes et coûteuses n'étaient pas imposées pendant cette période[55].
Le danger du radon dans les habitations a été mis en évidence en 1984, quand Stanley Watras, employé de la centrale nucléaire de Limerick (Pennsylvanie) déclencha les détecteurs de radioactivité en se rendant à son travail, les autorités cherchèrent pendant 2 semaines l'origine de cette contamination. Ils trouvèrent finalement que la source était un taux très élevé de radon (près de 100 000 Bq/m3, soit 2700 pCi/l) dans la cave de son domicile[49], sans relation particulière avec la centrale nucléaire.
Il a été calculé qu'un tel taux d'exposition est aussi risqué que de fumer 135 paquets de cigarettes par jour. À la suite de cette découverte hautement médiatisée, des normes sanitaires furent définies, et la détection du radon (et sa ventilation) devinrent une préoccupation publique[56].
Radiotoxicité biologique
Le radon est chimiquement neutre : l'atome de radon en lui-même ne se fixe pas dans les poumons ni dans l'organisme humain. De ce fait, les doses délivrées par le radon proprement dit sont négligeables. Ce sont les descendants du radon qui sont à l'origine des irradiations, et principalement ses descendants à vie courte. Les effets du radon sur l'organisme peuvent devenir significatifs si la concentration devient trop abondante.
Dans une atmosphère chargée en radon, celui-ci est très rapidement en équilibre séculaire avec ses descendants à vie courte. Par exemple, à la suite de sa désintégration alpha (3,824 jours), le radon 222 va donner du polonium 218 (3,1 min). Celui-ci va rapidement, par une autre désintégration alpha, donner du plomb 214 (26,8 min), qui va donner du bismuth 214 (19,7 min), puis du polonium 214 (164 µs) et enfin du plomb 210 (22,3 années), à vie relativement plus longue.
Les produits de désintégration à vie courte et surtout le plomb 210 se retrouvent sous forme libre (particules nanométriques) ou déposés sur les aérosols (micrométriques), qui pénètrent par les voies respiratoires et se fixent dans le poumon.
Ce plomb est lui-même radioactif, et se désintègre en bismuth 210 (5,01 jours), qui donne du polonium 210 (138 jours), puis du plomb 206 (stable).
Ces descendants radioactifs fixés dans les poumons émettent des particules α d'énergie élevée qui irradient les tissus.
Pour un becquerel de radon, il y a alors 4 désintégrations alpha successives et 5 bêta[57].
Maladie professionnelle
Le seul risque connu pour l'inhalation du radon (et plus encore de ses produits de désintégration) est celui du cancer du poumon. En 1987, le radon a été reconnu par le Centre international de recherche sur le cancer (CIRC) cancérigène pulmonaire pour l'homme, sur la double base d'études expérimentales animales et d'études épidémiologiques chez les mineurs d'uranium. Sa cancérogénicité a été démontrée par de nombreuses études épidémiologiques (études rétrospectives notamment) ayant porté sur les mineurs de fond de mines d'uranium ou de charbon.
Dans le Système international d'unités, l'unité utilisée pour mesurer la concentration d'activité du radon dans l'air est le becquerel par mètre cube (Bq/m3). Le coefficient de dose efficace par unité d’exposition adopté pour le radon est issu de la publication 65 de la CIPR, il est égal à 2,46 × 10−9 Sv par Bq h/m3. Ce taux correspond à un coefficient de conversion de 1 millisievert par an pour 50 Bq/m3[58]. Respirer en permanence un air chargé de radon à 3 000 Bq/m3 (ce qui est une concentration très élevée) conduit donc à une irradiation de 65 mSv/an, ce qui équivaut en termes de risque cancérigène à fumer 20 cigarettes par jour[59].
D'autres unités sont également utilisées en pratique, le working level (WL) et le milli-working level (mWL), qui mesurent le rayonnement émis par les descendants du radon. Par définition, 1 WL est équivalent à 1,3 × 105 MeV en rayonnement alpha par litre d’air. L'exposition des mineurs au radon est alors mesurée en working level months (WLM), c'est-à-dire le produit du nombre de mois de travail (170 h au Canada, 173 h aux États-Unis) par l'activité ambiante quand elle est mesurée en WL[60],[61]. En pratique, le working level équivaut à une activité volumique du radon de 12 000 Bq/m3, et 1 WLM correspond à peu près à l'exposition pendant un an à une atmosphère où l'activité du radon serait de 230 Bq/m3. La conversion entre ces deux unités est difficile, car nécessitant la connaissance précise des facteurs d'incertitude[62].
Le supplément de risque de contracter un cancer du poumon au cours de sa vie serait de 350 cancers par million d'habitants pour un niveau d'exposition de un WLM[63], soit 0,035 % par WLM. Cependant, le niveau d'exposition de la population est mal mesuré, et ce risque est également très dépendant du tabagisme, le radon étant à la fois un inducteur et un facteur multiplicatif du cancer du fumeur, ce qui rend les études épidémiologiques d'interprétation difficile.
Exposition
L'homme et les animaux y sont principalement exposés via l'inhalation d'air en contenant, et plus rarement via l'ingestion d'eau (cas de certaines eaux thermales). Certaines eaux déclarées potables peuvent laisser dégazer du radon[64]. Une étude a conclu que le risque radon devrait être pris en compte dans le choix des sites de creusement de puits[65].
Certains métiers — mineurs, travailleurs des engrais phosphatés[66],[67], du phosphogypse[68] ou du thermalisme — y sont plus exposés.
Concernant l'exposition des mineurs et ses risques
15 études rétrospectives de cohortes de mineurs de fonds exposés au radon, ainsi que les analyses de 22 études épidémiologiques faites en habitat résidentiel en Amérique du Nord, Chine et Europe ont clairement démontré que le radon est un cancérigène certain pour les poumons humains, même à des taux couramment rencontrés dans l'air intérieur des maisons[41]. La courte durée de demi-vie de ses descendants pourrait expliquer que ces cancers radio-induits semblent cibler les poumons et que les leucémies (de l’adulte, au Royaume-Uni) n’y semblent pas associées[52].
Dès les années 1960, au Royaume-Uni notamment, dans le East Midlands, le Kent et le bassin houiller écossais[69], on a mesuré le radon dans certaines mines de charbon. Les valeurs trouvées pour le radon 222 variaient de 0,2 pCi/L (= picocuries de radon par litre d'air), proche de ce qu'on trouve dans l'atmosphère, à plusieurs centaines de fois plus.
En 1964, en se basant sur les modélisations de quantités de radon inhalé et sur l'expérimentation animale, des chercheurs estiment que les normes alors en vigueur dans l'industrie minière de l'uranium (20 rads par an tolérés pour les cellules pulmonaires exposées via une respiration par le nez avec une ventilation pulmonaire moyenne de 15 L/min) ne permettaient pas de limiter les risques. Ils proposaient de réduire cette « norme » de dix fois[38]. Cependant, à la fin du XXe siècle, beaucoup de pays miniers ou d'industries n'avaient pas encore de réglementation sur le radon dans les mines ou ne l'avaient que depuis peu. De plus, la mesure précise de l’exposition réelle au radon et à ses descendants dans la mine, dans le sol à proximité de la mine[70], ou évaluée à partir d’échantillons peut être délicate[71], notamment parce que le radon peut se dégrader rapidement, y compris dans les poumons et l’organisme, en formant des produits de décomposition à vie courte qui rendent difficile l’analyse conjointe de la somme des énergies alpha potentielle du radon et de ses descendants[72], d’autant que la teneur relative des teneurs en ces différents produits varie dans l’espace et le temps.
Enfin, dans une même mine, les teneurs en radon peuvent varier d’un à deux ordres de grandeur, selon le moment et le lieu de la mesure.
Les concentrations en radon dans la mine peuvent être élevées : par exemple, les analyses publiées en 2004[73] faites dans les mines brésiliennes ont mis en évidence des taux de radon dépassant dans toutes le niveau d'action pour les lieux de travail (500 à 1 500 Bq/m3 d’air, recommandés par la Commission Internationale de Protection Radiologique-CIPR 65). La dose efficace moyenne estimée pour les mineurs de fond brésiliens était presque 30 fois plus élevée que la dose moyenne mondiale pour les mineurs de charbon[73].
La modélisation du dégazage de radon et de ses descendants radioactifs, en profondeur comme en surface est encore (en 2011) délicate et en cours de développement et de validation[74]. Le radon (et descendants) peut remonter avec le grisou en surface via les failles du sol (souvent aggravées par les séquelles minières de type effondrement), et il peut s’introduire dans les caves et maisons ou autres bâtiments construits au-dessus d’anciennes mines[75]. D’autres études ont montré (au-dessus d’une ancienne mine d’uranium par exemple), que le radon peut continuer à remonter en surface bien après la fermeture ou l'abandon d'une mine, y compris via les failles de la roche sous-jacente au sol (et avec des variations saisonnières[76]).
Ainsi des taux élevés (410 kBq/m3 en moyenne) de radon ont été détectés dans le tunnel d'une mine d'uranium fermée (ainsi que son système de ventilation) en 1997, située de 15 à 55 m sous le village hongrois de Kővágószőlős). À proximité, la concentration moyenne de radon dans les habitations était de 483 Bq/m3 et bien plus élevée (en moyenne 667 Bq/m3) dans des maisons situées à ± 150 m de la projection en surface du tunnel minier + 50 m, contre en moyenne 291 Bq/m3 dans les maisons plus éloignées (300 m aux alentours). En moyenne, 88,8 kBq/m étaient trouvés dans le sol, et l'exhalaison de radon correspondait à 71,4 Bq/m2 et par seconde (en moyenne). Les taux les plus élevés ont été mesurés en sortie de galerie et au sortir des failles remontant en surface et la concentration de radon élevée générée dans le passage (en moyenne 410 Bq/m3) peuvent influer sur la concentration de radon dans les maisons sur le tunnel minier. L’agriculture a été pratiquée sur le site après fermeture de la mine.
Dans une ancienne région minière où le charbon et les « cendres volantes » (déchets de centrales thermiques au charbon) sont légèrement radioactifs (U et 226Ra), des analyses de radon ont été faites au-dessus de l’ancienne mine et alentours (à toutes les périodes de l'année) ; les taux d'exhalation de radon allaient de 9 × 10−3 à 4 × 10−1 Bq/(m2 s). C'est sur les zones riches en charbon et en cendres de charbon que le dégazage (exhalation) de 222Rn était le plus élevé (avec des taux variant de 1,1 × 10−2 à 4,5 × 10−1 Bq/(m2 s)).
Un test de couverture (par de l’argile et de la terre) d’une partie de la zone située au-dessus de l’ancienne mine de charbon a été fait, après quoi le taux d'exhalation du radon était divisé par 10 en moyenne, mais l’été, les émissions de radon étaient plus importantes, sans doute en raison de la déshydratation du sol.
L’utilisation des cendres volantes comme matériel de terrassement, fond de couche autour des maisons explique un taux élevé de radon dans les zones habitées. (Dans cette zone, à plus de 1 km de la mine, et en centre-ville ou au centre d'une zone de nouvelle urbanisation, on a mesuré des valeurs moyennes (sur un an) d'environ 0,15 Bq/(m2 s) et le radon était encore exhalé autour de la mine d'uranium de Zirovski VRH en Slovénie (maintenant fermée) pour une dose de 0,005 à 0,25 Bq/(m2 s) (à comparer à 0,67 Bq/(m2 s) trouvés dans une maison construite au-dessus d’une ancienne mine d’uranium[77] ou aux 0,67 Bq/(m2 s) de la mine à ciel ouvert australienne de la Sickness country, l’une des plus radioactives d’Australie (0,062 Bq/(m2 s) aux alentours)[78].
En Suède, une étude rétrospective a montré une nette surmortalité par cancer du poumon chez les employés de mines de fer y compris chez les non-fumeurs. Chez un groupe de 1415 mineurs de fer suédois, ponctuellement exposés de 1951 à 1976 à de brèves durées d’exposition à des descendants radioactifs du radon, à des taux conduisant à approcher les limites professionnelles actuellement acceptées, le risque était presque multiplié par 5. Il y a eu 50 morts par cancer du poumon par rapport aux 12,8 attendus (en incluant les risques liés au tabagisme et par comparaison à un échantillon aléatoire de la population suédoise masculine). 18 de ces morts étaient des non-fumeurs, par rapport à 1,8 attendu, et 32 décès ont été observés chez les fumeurs ou des ouvriers récemment sevrés du tabac, pour 11,0 décès attendus. Le tabagisme additionne ses effets à l'exposition aux rayonnements alpha du radon[79].
Une autre étude rétrospective a été faite dans la mine souterraine de charbon de Figueira (Sud-Brésil), en fonction depuis 1942 (sans équipements diesel dans la mine) et où aucune mesure de radon n’avait été faite avant les années 2000 ; Pour 2856 mineurs (1979-2002) dont 2024 mineurs de fond potentiellement exposés au radon. Le risque de cancer pulmonaire est statistiquement bien corrélé à la durée de travail souterrain[80].
Dans des mines de charbon étudiées au Baloutchistan (Pakistan), le taux de radon variait de 121 à 408 Bq/m3, soit une dose calculée pour les mineurs variant de 1,38 à 4,67 mSv/an avec une moyenne de 2,19 ± 0,5 mSv par an, taux jugé acceptable par les autorités sanitaires locales[81].
Le cas particulier des mines (dont de charbon, de schiste bitumineux ou de lignite)
Dans les années 1950, on commence à doser le radon et ses produits de dégradation radioactive dans les mines[82]. Dans les années 1960, après publication en 1959 de recommandations sur l’exposition à la radioactivité par la Commission internationale de protection radiologique[83], on commence à s’inquiéter du taux de radon de certaines mines de charbon[84] et on démontre plus clairement une surmortalité par cancer du poumon des mineurs de fond exploitant le charbon, à l’exposition au radon[85], et on essaye de préciser le rayonnement absorbé (voies externes et internes), dont par inhalation[86],[87].
Les études montrent que la quantité de radon dans les mines et le sol varie considérablement selon le caractère plus ou moins uranifère et radifère du matériau, mais aussi selon qu’il s’agisse d'une mine ouverte en plein ciel ou non, selon que les galeries soient bien ventilées ou non, et selon le contexte géologique et hydrogéologique (failles, mouvements de nappes phréatiques). La température intervient aussi, car elle accentue le dégazage du radon dans l’air, notamment en profondeur là où le charbon est plus chaud ; Par exemple, en portant expérimentalement la température du charbon de 30 °C à 180 °C, le taux de radon trouvé dans le charbon augmente de huit à dix fois. Dans la « fourchette basse » de réchauffement (de 30 °C à 70 °C), ce taux augmente de deux à trois fois (ce qui fait que le taux de radon trouvé dans un charbon peut être utilisé comme indice d'un chauffage du charbon[88], possible en profondeur, mais également en chauffage quand les terrils chauffent au Soleil et/ou ont entamé une combustion interne qui transforme le schiste noir des stériles minières en schiste rouge.
Les conditions météo en particulier les hautes et basses pressions et le vent peuvent également (passagèrement mais considérablement) affecter les taux d’extraction naturelle (exhalation) de radon à partir du sol, des failles drainantes ou de mines actives ou abandonnées[89]. Le radon peut être localement très concentré dans les mines. On en trouve moins que dans les mines d’uranium, mais certains charbons contiennent de petites quantités d’uranium et certaines mines de charbon produisent des quantités parfois importantes de radon.
Au Royaume-Uni (où il n’y a pas de mines d'uranium exploitées), douze mines de charbon et dix autres mines ont été étudiées. Le radon était présent dans les mines de charbon, mais moins que dans trois mines d'hématite (Ouest-Cumberland) et deux mines d'étain, où en plusieurs points des niveaux supérieurs au niveau opérationnel étaient atteints[90] (avec une incidence effectivement accrue de cancers dans les mines d’hématite)[90],[91].
Le lignite relargue aussi du radon et des descendants radioactifs du radon[92] auxquels les mineurs de fond sont plus exposés (dans le cas de mines souterraines). Comme dans les mines de charbon, les taux de radon aéroporté peuvent fortement varier selon les lieux et moments. Par exemple, dans 3 mines de lignite étudiées en Turquie, les concentrations de radon dans les mines variaient de 50 ± 7 à 587 ± 16 Bq/m3 d'air (il faudrait y ajouter les taux de descendants radioactifs du radon), en dessous des seuils d'action en vigueur en Turquie, selon les expositions au radon telles qu'évaluées pour les travailleurs des mines de lignite d'Tunçbilek, Ömerler et Eynez à respectivement 1,23, 2,44 et 1,47 mSv par an[92].
Il en va de même pour les mines de schistes bitumineux (ex. : dans la mine d’Amasra, du « bassin houiller bitumineux de Zonguldak » (Turquie) sur 40 jours, les taux de radon ont varié de 49 Bq/m3 à 40 m de fond à 223 Bq/m3 à -100 m, avec une moyenne de 117 Bq/m3), inférieure au seuil d'intervention de 500–1 500 Bq/m3 recommandés par la Commission internationale de protection radiologique (CIPR) en 1993. La « dose efficace moyenne » pour les travailleurs de cette mine a été estimée à 3,4 µSv par jour[93] et peut être comparée à celle subie dans d’autres mines (mines de bore, où l’air est riche en radon, mines de chrome où le minerai est peu désorbant et où la radioactivité de l’air est « faible », inférieure à celle des minerais[94]) alors que dans les mines de charbon, le radon peut être nettement plus présent, à cause notamment de teneurs plus élevées du charbon en uranium et thorium[94].
Dans d’autres cas, les taux de radon dans l’air intérieur des galeries de mines dépassaient les recommandations du CIPR (ex : plus de 1 000 Bq/m3 d’air dans les mines de Kozlu, de Karadon et d’Üzülmez dans le bassin minier bitumineux de Zonguldak également en Turquie)[95].
Le radon émis par les mines de charbon a des impacts connus sur les mineurs de fond, mais semble pouvoir également et plus largement contribuer à l’augmentation du fond radioactif de l’air autour de certains sites miniers. On a montré par exemple dans le bassin charbonnier des Appalaches une incidence accrue du cancer du poumon dans les zones d’extraction, qui ne semble pas pouvoir être expliquée par d’autres facteurs de risque ou covariables que l’exposition au radon, même si le tabagisme et la pauvreté sont aussi des facteurs contributifs[96].
Dans certaines régions au moins, le fond géochimique et/ou le fond aérochimique[97] naturels peuvent aussi être perturbés par les eaux d’exhaures de pompages miniers[98] ; ces eaux, ont en effet été remontées (par milliards de mètres cubes, depuis plus de 100 ans) et déposées dans des bassins d’évaporation ou évacuées dans les rivières (en modifiant les teneurs en sel de la Baltique). Or, en profondeur, ces eaux sont souvent (en Pologne tout particulièrement) hautement minéralisées (taux de sel atteignant 200 kg/m3, par exemple dans la nappe du carbonifère minier de Haute-Silésie[98]. Elles contiennent souvent une forte concentration de radium 226 (jusqu’à 400 kBq/m3 dans le cas de la Haute-Silésie). Ces eaux radifères contiennent souvent aussi des quantités significatives d'ions baryum[98]. Dans ces cas, en surface, le radium coprécipite facilement avec du baryum sous forme de BaSO4 + RaSO4[98]. La radioactivité spécifique de ces dépôts peut être élevée (se mesurant en MBq/kg parfois). Ces dépôts radioactifs peuvent générer un rayonnement gamma élevé, accompagné d’une certaine élévation des concentrations de radon et de ses descendants dans l'air[98]. Une partie du fond dit « naturel » de radioactivité ambiante aéroportée pourrait en fait provenir des milliers de mines d’uranium, de fer, de charbon… encore actives ou autrefois actives.
Selon les études récentes (2019) mêmes de faibles expositions augmentent le risque de cancer du poumon[99].
Concentration de radon domestique
Impact sanitaire du radon
Le radon est responsable de la plus grande part de l'exposition humaine à la radioactivité : 42 % du total selon l'OMS[101]. Sur cette base, si l'on applique le modèle linéaire sans seuil (dont on sait par ailleurs qu'il ne reflète pas la réalité de l'exposition biologique), les autorités sanitaires[102] estiment que sa radioactivité serait (selon le modèle utilisé) la cause de 2,2 à 12,4 % des décès par cancer du poumon en France, ce qui en ferait la deuxième cause de décès par cancer du poumon, juste derrière le tabac et au même niveau que le tabagisme passif[103],[104],[105].
En fait, depuis les années 1990, les études épidémiologiques de type cas-témoins s’efforçant de relier l’exposition domestique et les cancers du poumon se sont multipliées sans réellement apporter jusqu’à présent de conclusions définitives[106].
Quelques études « à contre-courant » contestent ces estimations et suggèrent au contraire qu'une exposition à des faibles doses de radon pourrait réduire le nombre de cancers constatés[107],[108],[109]. Les corrélations géographiques entre richesse du sol en uranium et cancer du poumon sont constamment inverses[106], un effet possiblement expliqué par la répartition géographique des fumeurs (statistiquement plus citadins, sur des sols moins riches en uranium)[110].
En définitive, les risques de l’exposition résidentielle au radon sont évalués en extrapolant la relation dose-effet obtenue pour les mineurs d’uranium. Le radon présente-t-il vraiment un tel risque pour la population[111] ?
Flux de radon dans les habitations
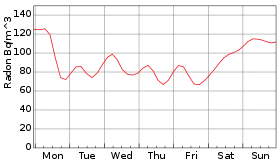
Le flux naturel de radon peut se retrouver plus concentré dans les espaces clos et notamment dans les maisons, dans les caves mal ventilées, à cause de la désintégration du radium, qui vient lui de la désintégration de l'uranium naturellement présent dans les briques et les roches du sol.
Le radon étant à durée de vie courte, il n'a pas le temps en quelques jours de diffuser à travers un matériau continu (sol compact, mur ou dalle sanitaire). Il ne peut pénétrer en quantité significative dans des bâtiments qu'à travers des solutions de continuité le long desquelles le gaz peut migrer rapidement : failles dans le sol, fissures dans les dalles. Une fois sur place, le radon reste dans les lieux quand ils sont mal ventilés : « le radon s'accumule avec les odeurs. » Les moyens pour diminuer les concentrations de radon dans les maisons sont l'aération et la ventilation des maisons, l'utilisation des vides sanitaires, le colmatage des fissures au niveau du sol, etc.
Selon un médecin français, André Aurengo :
« Si vous êtes inquiets du radon, aérez 5 minutes le matin, 5 minutes à midi, et 5 minutes le soir, et vous n’aurez pas de radon. Évidemment, les gens qui sont sur ce marché vous proposeront des solutions incomparablement plus lourdes et coûteuses[112]. »
De ce fait, le taux de radon dans les domiciles ou bâtiments publics est très variable. De plus, ce taux peut varier rapidement d'une pièce à l'autre, ou d'un moment à l'autre, en fonction de la circulation à l'intérieur du bâtiment.
En France, la teneur domestique moyenne est voisine de 65 Bq/m3[104], et 92 % des habitations seraient à moins de 200 Bq/m3. Mais 1,5 % sont situés dans la limite d'intervention, entre 400 et 1 000, et 0,5 % au-dessus de 1 000, c'est-à-dire à des taux comparables à ceux observés dans les mines d'uranium (une fois ventilées). Dans les cas extrêmes, la concentration du flux de radon peut conduire à des valeurs très importantes (comme le montre l'exemple de Stanley Watras, à près de 100 000 Bq/m3).
Dans les régions où la concentration en uranium dans la roche est élevée, il est souvent présent dans les habitations peu ventilées, ou construites sur des sols à fort dégagement de radon (rez-de-chaussée, maisons, caves). Il entraîne alors une exposition interne conséquente à cause de ses descendants à vie courte (dont fait notamment partie le polonium). La Creuse, la Lozère, le Tarn et la Corse-du-Sud ont, dans les bâtiments, des concentrations supérieures à 250 Bq/m3. Les taux les plus faibles sont dans les Landes (28 Bq/m3) en raison de la nature sédimentaire des sols[104].
Normes de concentrations admissibles en radon
En Suisse, dans les pièces d'habitation et de séjour, la valeur limite au-dessus de laquelle il faut assainir est de 1 000 Bq/m3 la valeur recommandée au-dessus de laquelle il est recommandé d'intervenir est de 400 Bq/m3 (pour autant que les investissements soient supportables). La législation de 1994 impose que tout bâtiment dépassant cette limite soit assaini aux frais du propriétaire. Une valeur de référence de 400 Bq/m3 est à respecter pour les bâtiments neufs, transformés ou après une remédiation. La mesure du radon se fait en hiver et au moins pendant un mois.
Aux États-Unis et Luxembourg, la valeur maximale qu'il est recommandé de ne pas dépasser pour les habitations est de 150 Bq/m3.
Dans l'Union européenne, la valeur recommandée est de 400 Bq/m3 pour les bâtiments existants et de 200 Bq/m3 pour les nouveaux bâtiments.
En Italie, la valeur à respecter sur les lieux de travail et les écoles est de 500 Bq/m3.
Au Canada, la valeur recommandée pour les habitations est de 200 Bq/m3.
En France, pour les lieux accueillant du public, la limite d'intervention[113] est de 1 000 Bq/m3 et la valeur recommandée est de 400 Bq/m3. L'obligation de mesure systématique ne concerne en 2008 que 31 départements, mais il est désormais obligatoire de réaliser une surveillance non seulement dans les établissements d'enseignement, les établissements sanitaires et sociaux, les établissements thermaux et les établissements pénitentiaires, mais aussi dans les locaux souterrains où certaines activités professionnelles sont réalisées au moins une heure par jour[114]. Il n'y a pas pour l'instant d'obligation pour l'habitat[104]. Il existe un « plan national 2005-2008 contre le radon » dont l'ASN a publié le premier bilan d'actions le [115], peu après que le Haut Conseil de la santé publique eut recommandé une importante réduction du seuil d'exposition au radon[116].
Applications

- Thérapie. Aux États-Unis et en Europe, on trouve quelques « spas au radon ». Il est possible de s'y asseoir quelques minutes ou heures dans une atmosphère enrichie en radon. Le radon ou ses radiations fortifierait l'organisme selon les partisans de cette méthode qui s'appuie sur les traditions de bains d'eau chaude de Misasa, Tottori au Japon, où l'eau est naturellement riche en radium et expulse du radon. La seule approche scientifique justifiant cette pratique serait celle de l’hormèse, sans qu'aucun mécanisme biologique connu par lequel cet effet pourrait se produire n'ait été scientifiquement démontré (mais inversement, les mécanismes avancés dans l’hypothèse contraire d'un effet linéaire sans seuil des radiations ont été scientifiquement invalidés[117]) ;
- Traçage radioactif. La demi-vie du radon est courte (3,8 jours, pour une énergie de 5,5 MeV). Il est donc utilisé dans les recherches hydrologiques d'interactions entre l'eau du sol, des ruisseaux et des rivières : Tout changement significatif dans la concentration en radon dans un ruisseau ou une rivière est un indice d'apport local d'eau souterraine, ou pour évaluer le degré d'aération de galeries de mines, de caves, de logements, ou l'évaluation de fuites à partir d'un réservoir souterrain. De même, la climatologie l'utilise pour étudier la circulation atmosphérique : suivant la quantité mesurée, on détermine l'origine continentale (riche en radon) ou océanique (pauvre en radon) d’une masse d’air. Le temps de transit de cette masse d’air au-dessus d’un continent va également jouer sur les concentrations de cet élément. Le radon sert donc de traceur des masses d'air continentales ;
- Traitement antitumoral. Une capsule de radon est placée sur le patient, près de la tumeur. Les radiations tuent les cellules cancéreuses. Les cellules environnantes n'étant pas ou peu affectées, en raison de la courte demi-vie du radon ;
- Alerte sismique. Des anomalies d'émission de radon (et de potentiel électrique) sont constatées[118] lors de séismes et d'éruptions volcaniques. Elles pourraient pour certaines précéder (et donc annoncer ?) des éruptions volcaniques, des tremblements de terre ou des mouvements de terrain[119]. L'utilité d'un suivi préventif reste discuté, mais on a constaté (par exemple en Inde[120]) une corrélation entre taux de radon dans les nappes souterraines et activité sismique. Un suivi en temps réel à coût raisonnable est possible[120]. On a montré dans les Alpes françaises que les variations de niveaux (de plus de 50 mètres) de deux lacs artificiels modifiaient les émissions périphériques de radon[121].
Mesure et cartographie du radon
La quantification du radon dans l'air ou dans un organisme est d'un grand intérêt épidémiologique, mais reste délicate car le radon a une courte durée de vie, et sa mesure est difficile en condition humide (dans les utilisations thermales par exemple).
Elle fait l'objet de normes[122].
Des méthodes de mesure ont été adaptées à l'eau[123], dont par dégazage[124].
On commence à disposer de cartes[125], dont en France[126] de risques ou d'émission, souvent fortement interpolées et utilisant des modélisations[127],[128] notamment du potentiel d'émanation (décrit par le facteur d'émanation[129], d'évaluation délicate, car très variable selon les milieux, et éventuellement soumis à des phénomènes complexes de pression atmosphérique, vent, cycles jour/nuit et saisonnier de température en surface, mouvements de nappe et modification de l'hydromorphie du sol, sécheresse et retrait/gonflement des argiles, etc.).
Le « facteur d'émanation » est défini comme le « rapport du nombre d’atomes de radon qui parviennent dans l’espace des pores du matériau par unité de temps et de volume sur le nombre total d’atomes de radon formés par unité de temps et de volume »[24].
Le ministère français de la santé délivre deux types d'agréments aux laboratoires d'analyse du radon :
- l'agrément de niveau 1 (dépistage simple pour déterminer les niveaux d'exposition) ;
- l'agrément de niveau 2 (identification des sources de radon et proposition de mesures correctrices).
En France, à certaines conditions (de ressources notamment), l'ANAH peut subventionner des propriétaires bailleurs et propriétaires occupants (sous conditions pour la réalisation des travaux nécessaires pour traiter les immeubles soumis à la présence de radon[130]. Plusieurs textes réglementaires[131],[132],[133] précisent les conditions dans lesquelles les mesures de radon doivent être faites (de manière à respecter « les normes internationales en vigueur », notamment dans certains lieux de travail[134] ou dans les lieux publics devant être surveillés[135], notamment quand ces lieux sont des bâtiments souterrains, des établissements thermaux, des cavités et ouvrages souterrains où en aout 2015 un arrêté précise que « la période de mesurage est la période comprise entre le 15 septembre d'une année et le 30 avril de l'année suivante. Cette période peut être adaptée dans le cas d'activité professionnelle saisonnière. Cette adaptation devra être justifiée par l'organisme qui réalise la mesure »[134]).
Cartographie
À partir de modélisations, éventuellement recalées par des contrôles in situ, on peut établir des cartes de risque ou d'exposition environnementale, comme cela a été fait ou est en cours en France[126] et éventuellement en précisant le risque pour les personnes plus vulnérables comme les fumeurs comme au Canada[136]
Plusieurs cartes ont été publiées pour la France en 2006[103], par l'IRSN[23] avec de légères nuances, sur la base des données géologiques et parfois de mesures in situ. Elles montrent généralement des moyennes mathématiques de risques d'exposition par région ou département, et ne tiennent pas compte d'éventuels points-chauds locaux d'origine géologique (failles, cavités souterraines naturelles) ou liés à la proximité de cavités minières et d'affaissements miniers[23]. L’IRSN précise que ces cartes « ne fournissent qu’une tendance générale du potentiel radon pour un territoire donné. Ces cartes ne permettent en aucun cas de prédire les concentrations de radon à l’intérieur d’un bâtiment donné et ne peuvent se substituer à la réalisation de mesures »[23]
Une carte européenne (Atlas européen des radiations naturelles) est en préparation depuis 2008, sous l'égide d'un groupe dit « REM » (pour Radioactivity Environmental Monitoring[137]) à l'initiative de la Commission européenne, de l’IES/JRC (Institute for Environment and Sustainability, Joint Research Center), sur la base d'une méthodologie commune et à partir des données géologiques[23].
Dosimètres radon
Le radon pose des difficultés dosimétriques, car à faible durée de vie, en état d'équilibre gazeux complexe, avec des produits de filiation solides de faible période radioactive, et en raison d'une faible pénétration des émissions alpha.
- L'unité d'exposition Sievert mesure l'effet biologique sur un individu, induit par le rayonnement absorbé (pour la totalité du corps exposé de manière interne et/ou externe, on parle de dose efficace).
- Une autre unité d’exposition a été proposée : l’« énergie alpha potentielle cumulée », fondée sur l'exposition à une activité volumique donnée, durant un temps donné et exprimée, en joule-heure par mètre cube (J h/m3). Une équivalence en sievert a été attribuée à cette grandeur, par comparaison avec l'excès de cancers (poumon) induits.
La mesure du radon dans les habitations et locaux s'effectue principalement avec un « dosimètre radon », sur une durée test de quinze jours à plusieurs mois, et, dans les cas où le radon vient du sol (la plupart des cas), préférablement en saison froide, car cela n'est pas significatif de mesurer le radon en été quand les fenêtres sont souvent ouvertes.
Un dosimètre radon consiste en un film plastique, sur lequel, après traitement, chaque impact de particule alpha laisse un trou microscopique. Après étalonnage, le nombre de traces et la durée de la mesure permettent de déduire la concentration de radon dans l'air.
Remédiation du radon
Il existe principalement deux méthodes de remédiation aux problèmes posés par le radon : à l'aide de barrières à l'entrée faisant obstacle au flux naturel (remédiation passive), et à l'aide d'appareils spéciaux extrayant l'atmosphère pour disperser le flux de radon (remédiation active). L'OMS et de nombreux organismes gouvernementaux émettent aujourd'hui des réserves sur l'efficacité de la remédiation passive à long terme et en absolu, même si elle reste plébiscitée dans les pays nordiques.
Les solutions actives sont efficaces mais ont un coût énergétique — électrique et thermique — en désaccord avec les volontés individuelles de réduire la facture énergétique globale du logement, de sorte que des offres d'optimisation énergétique de la remédiation du radon font leur apparition sur le marché.
Notes et références
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche)
- (en) Philip Mayles, Alan Nahum et Jean-Claude Rosenwald, Handbook of Radiotherapy Physics : Theory and Practice, New York, CRC Press, Taylor & Francis Group, , 1470 p. (ISBN 978-0-7503-0860-1 et 0-7503-0860-5), p. 1102 : Brachytherapy developed largely through the use of sealed radium and radon sources. In the 1950s, alternative artificially produced nuclides became available, and gradually radium and radon were replaced with 137Cs, 192Ir, 60Co, 198Au, and 125I sources (Trott 1987; Godden 1988). Although radium and radon are no longer used, many of the techniques that are used currently are based on the clinical experience gained with those sources over more than sixty years. Trott, N.G., Ed., Radionuclides in brachytherapy: Radium and after. Br. J. Radiol. (Suppl. 21), 1987. Godden, T. J., Physical Aspects of Brachytherapy, Medical Physics Handbook 19, Adam Hilger, Bristol and Philadelphia, 1988.
- Curie, P. ; Curie, Mme. Marie, « Sur la radioactivité provoquée par les rayons de Becquerel. », Comptes rendus hebdomadaires des séances de l'Académie des sciences, vol. 129, , p. 714–716.
- (en) E, Rutheford ; Owens, R. B., « Thorium and uranium radiation », Trans. R. Soc. Can., vol. 2, , p. 9–12: « les radiations de l'oxode de thorium n'étaient pas constantes, mais variaient de manière très capricieuse », alors que « tous les composés d'uranium donnent une radiation qui est remarquablement constante ».
- (en) Rutheford, E., « A radioactive substance emitted from thorium compounds », Philosophical Magazine, vol. 40, , p. 1–4.
- Dorn, Friedrich Ernst, « Ueber die von radioaktiven Substanzen ausgesandte Emanation », Abhandlungen der Naturforschenden Gesellschaft zu Halle, Stuttgart, vol. 22, , p. 155.
- (en) Rutheford, E.; Brooks, H.T., « The new gas from radium », Trans. R. Soc. Can., vol. 7, , p. 21–25.
- (de) Giesel, Fritz, « Ueber den Emanationskörper aus Pechblende und über Radium », Chemische Berichte, vol. 36, no 1, , p. 342–347 (DOI 10.1002/cber.19030360177).
- Debierne, André-Louis, « Sur la radioactivité induite provoquée par les sels d'actinium. », Comptes rendus hebdomadaires des seances de l'Academie des sciences, vol. 136, , p. 446 (lire en ligne).
- (en) Ramsay, Sir William ; Collie, J. Normal, « The Spectrum of the Radium Emanation », Proceedings of the Royal Society of London, vol. 73, , p. 470–476 (DOI 10.1098/rspl.1904.0064).
- Schmidt, Curt, « Periodisches System und Genesis der Elemente », Z. Anorg. Ch., vol. 103, , p. 79–118 (DOI 10.1002/zaac.19181030106).
- Perrin, Jean, « Matière et lumière. Essai de synthèse de la mécanique chimique », Annales de Physique, iX, vol. 11, , p. 5–108 (lire en ligne)
- (en) Adams, Elliot Quincy, « The Independent Origin of Actinium », Journal of the American Chemical Society, vol. 42, , p. 2205–2208 (DOI 10.1021/ja01456a010).
- Bernard Fernandez, De l'atome au noyau : Une approche historique de la physique atomique et de la physique nucléaire, Ellipses, , 597 p. (ISBN 978-2-7298-2784-7), partie I, chap. 4 (« L'émanation du thorium »).
- Ramsay, W. ; Gray, R. W., « La densité de l’émanation du radium », Comptes rendus hebdomadaires des séances de l'Académie des sciences, vol. 151, , p. 126–128 (lire en ligne).
- (en) Grosse, A. V., « Some physical and chemical properties of element 118 (Eka-Em) and element 86 (Em) », Journal of Inorganic and Nuclear Chemistry, Elsevier Science Ltd., vol. 27, no 3, , p. 509–519 (DOI 10.1016/0022-1902(65)80255-X).
- « Radon », All Measures, (consulté le ).
- « Radon Facts », chemistry.about.com.
- D'après Laradioactivite.com.
- IRSN (cartographie de risque lié au radon, jusqu'à l'échelle communale et explications sur le radon.
- Ineris & IRSN, Le radon, synthèse des connaissances et résultats des premières investigations en environnement minier, Rapport d'étude 23/12/2008 INERIS-DRS-08-86108-07270A.
- "Facts about Radon". Consulté 2008-09-07.
- E. Stranden, A. K. Kolstad: « Radon exhalation from the ground; method of measurements and preliminary results”, The Science of the Total Envir., 45, p. 165-171, Elsevier, Amsterdam, 1985.
- Megumi, K., Mamuro, T.: « A Method for Measuring Radon and Thoron Exhalation from the Ground », Journal of Geophysical Research, 77, 3052 - 3056, 1972.
- (en) « The Geology of Radon », United States Geological Survey (consulté le ).
- (en) « Radon-222 as a tracer in groundwater-surface water interactions », Lancaster University (consulté le ).
- Yamazawa H., M. Matsuda, J. Moriizumi, T. Iida (2008) Wet Deposition of Radon Decay Products and its Relation with Long-Range Transported Radon ; conference ; The Natural Radiation Environment ; volume = 1034, pages = 149-152 ; doi = 10.1063/1.2991194 ; consulté 2011-08-23 (Résumé).
- M.B. Greenfield, A. Iwata, N. Ito, M. Ishigaki, K. Kubo (2006) « Intense γ radiation from radon progeny accreted in/on rain during and following thunderstorms » dans Bulletin of the American Physical Society ..
- M. B. Greenfield, « Determination of rain age via γ rays from accreted radon progeny », Journal of Applied Physics, vol. 104, no 7, , p. 074912 (ISSN 0021-8979, DOI 10.1063/1.2990773, lire en ligne [archive du ], consulté le ).
- FILMTEC Membranes - SR90 Membrane Sulfate Removal of Offshore Oil Injection Water Answer ID 278 Updated 04/14/2011, consulté 2011-08-31.
- [PDF] "Potential for Elevated Radiation Levels In Propane". National Energy Board. April 1994. Consulté 2009-07-07.
- Z Fokryszka, D Grabowski (2004), Émissions gazeuses à partir des vides miniers dans le bassin ferrifère lorrain ; Revue française de géotechnique- cat.inist.fr.
- L Vaute (1999), « Identification d'éléments indésirables ou toxiques dans les ressources en eau potentielles du bassin ferrifère lorrain »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ) - Rapport BRGM R, 1999 ; brgm.fr.
- La migration du Radon 222 dans un sol. Application aux stockages de résidus issus du traitement des minerais d'Uranium.(21/04/2000) Cécile Ferry, Thèse de doctorat en Sciences de l'université Paris-XI Orsay soutenue le 21 avril 2000. Rapport CEA - No d'ordre: 6127.
- Altshuler, B., Nelson, N., and Kuschner, M. (1964). Estimation of lung tissue dose from the inhalation of radon and daughters. ; Hlth. Phys., 10, 1137-1161. (Résumé).
- Chamberlain, A. C., and Dyson, E. D. (1956). The dose to the trachea and bronchi from the decay products of radon and thoron. Brit. ; J. Radiol., 29, 317-325. (Résumé).
- Site Internet de l'ANDRA, consulté en 2007.
- R.W. Field « Radon: An Overview of Health Effects », Encyclopedia of Environmental Health, pages 745-753, doi:10.1016/B978-0-444-52272-6.00095-7 (Résumé, en anglais).
- R. Améon, Le radon dans les stations thermales, une source d'exposition, Radioprotection 2003, vol.38, no 2, pages 201 à 215, DOI:10.1051/radiopro:2003005.
- IRSN, « Congrès ASFERA » Radon et thermalisme ; R. Améon 11-12 décembre 2001, Paris, France (Résumé).
- DNEMT (Division nationale des eaux minérales et thermales, BRGM, Eau minérale et radioactivité, notes techniques 15 juillet 2000, BRGM, 2000.
- « Therapeutic Hot Mineral Springs & Thermal Spas of Ikaria », sur www.island-ikaria.com (consulté le ).
- Tracy BL, Krewski D, Chen J, Zielinski JM, Brand KP, Meyerhof D (2006) Assessment and management of residential radon health risks: a report from the health Canada radon workshop ; J Toxicol Environ Health A. avril 2006 ; 69(7):735-58. résumé.
- Darby S, Hill D, Doll R. (2001) Radon: a likely carcinogen at all exposures ; Ann Oncol. 2001 Oct; 12(10):1341-51 (résumé).
- (en) Zdrojewicz, Zygmunt et Jadwiga (Jodi) Strzelczyk, « Radon Treatment Controversy, Dose Response », Dose-Response, vol. 4, no 2, , p. 106–18 (PMID 18648641, PMCID 2477672, DOI 10.2203/dose-response.05-025.Zdrojewicz).
- « Berks Home Sits On Top Of Uranium Ore Firm Explains How It Dealt With Highest U.s. Radon Level », sur tribunedigital-mcall (consulté le ).
- D. LAURIER, B. VACQUIER, K. LEURAUD, S. CAER, A. ACKER, M. TIRMARCHE, 2007 : Risques associés au radon : l'apport des études de mineurs. INVS, BEH Thématiques 18-19.
- R.W. Field, « Radon: An Overview of Health Effects », Encyclopedia of Environmental Health, pages 745-753, doi:10.1016/B978-0-444-52272-6.00095-7 ; (Résumé).
- Graham R Law, Eleanor V Kane, Eve Roman, Alex Smith, Ray Cartwright, « Residential radon exposure and adult acute leukaemia » ; The Lancet, Volume 355, Issue 9218, 27 May 2000, Page 1888.
- A Citizen's Guide to Radon. U.S. Environmental Protection Agency. January 2009. Consulté 2008-06-26.
- Voir sur who.int..
- Mould, Richard Francis, A Century of X-rays and Radioactivity in Medicine, CRC Press, (ISBN 0-7503-0224-0).
- Harrison, Kathryn; Hoberg, George, « Setting the Environmental Agenda in Canada and the United States: The Cases of Dioxin and Radon », Canadian Journal of Political Science, vol. 24, no 1, , p. 3–27 (lire en ligne).
- Chaine radioactive de l'uranium 238 ; englobant celle du radon 222..
- Cité d'après Estimation de l’impact sanitaire collectif de la contamination des terrains par la radioactivité présente à Gif sur Yvette, Institut de veille sanitaire, juin 2002.
- D'après .
- (en)Radiation - Quantities and Units of Ionizing Radiation, Canadian Centre for Occupational Health and Safety.
- (en)30 CFR PART 57—SAFETY AND HEALTH STANDARDS—UNDERGROUND METAL AND NONMETAL MINES.
- « Guide sur les mesures du radon dans les maisons »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ), Santé Canada.
- D'après (en) Committee on Health Risks of Exposure to Radon (BEIR VI), National Research Council, Health Effects of Exposure to Radon(BEIR VI), Washington, DC, National Academy Press, (ISBN 0-309-52374-5, présentation en ligne, lire en ligne), (cité par le centre canadien d'hygiène et de sécurité au travail ).
- W.W. NAZAROFF, S.M. DOYLE, A.V. NERO, R.G. SEXTRO, 1987 : Potable water as a source of airborne 222Rn in U.S. dwellings. A review and assessment. Health Physics, 52, p. 281-295.
- A. Lindmark and B. Rosen, Radon in soil gas — Exhalation tests and in situ measurements ; Science of The Total Environment, volume 45, October 1985, pages 397-404 Exposure to Enhanced Natural Radiation and its Regulatory Implications doi:10.1016/0048-9697(85)90243-8 (Résumé).
- H. MAHJOUBI, A.H. CHARFI, S. LABIDI, N. CHAHED, S. MTIMET, 2000 : Estimation des expositions associées à la présence du radon 222 dans les usines de traitement de déchets d'uranium.
- D. PELLEGRINI, 1997 : Étude de l'émanation du radon à partir de résidus de traitement de minerais d'uranium. Mise en évidence de relations entre le facteur d'émanation et les caractéristiques du matériau. Thèse soutenue à l’U.F.R. des sciences et techniques de l'Université de Franche-Comté le 04/12/1999, 200 p., phosphates et leurs environnements en Tunisie. Radioprotection, vol. 35 (2), p. 201-215.
- J. MOISSET, 1980 : Radium removal from phosphogypsum. In Borris D. P., Boody P. W., eds., Phosphogypsum, Proceedings of the International Symposium on Phosphogypsum: utilization and/or disposal of phosphogypsum; potential barriers to utilization: Lake Buena Vista (États-Unis). Publication no 01-001-017, Florida Institute of Phosphate Research: Bartow (États-Unis), reprinted 1987, p. 384-397.
- Duggan, M. J., Howell, D. M., and Soilleux, P. J. (1968). (Radiological Protection Service), « Concentrations of Radon-222 in Coal Mines in England and Scotland » ; Nature 219, 1149 (14 September 1968); doi:10.1038/2191149a0 (Résumé).
- R. Winkler, F. Ruckerbauer, K. Bunzl, « Radon concentration in soil gas: a comparison of the variability resulting from different methods, spatial heterogeneity and seasonal fluctuations », The Science of The Total Environment, volume 272, Issues 1-3, 14 May 2001, pp. 273-282 (Résumé).
- Khalid Jamil et Safdar Ali, « Estimation of radon concentrations in coal mines using a hybrid technique calibration curve » ; Journal of Environmental Radioactivity ; volume 54, Issue 3, 2001, pages 415-422 ; doi:10.1016/S0265-931X(00)00175 (Résumé).
- Jan kowronek, Les descendants à vie courte du radon dans les mines de charbon en Pologne, Radioprotection, volume 26, no 1, janvier-mars 1991, pages 65 – 74 ; DOI :10.1051/radiopro/1991005, on line 8 juin 2009, Radioprotection 1991, vol. 26, no 1, pages 65 à 74 (Résumé).
- L H S Veiga et al High radon exposure in a Brazilian underground coal mine ; 2004 J. Radiol. Prot. 24 295 (Résumé).
- D. Page et D.M. Smith, The Distribution of Radon and its Decay Products in Some UK Coal Mines ; Oxford Journals, Mathematics & Physical SciencesMedicine, Radiation Protection Dosimetry, volume45, Issue1-4 ; pages 163 à 166.
- János Somlai, Zorán Gorjánácz, András Várhegyi, Tibor Kovács, « Radon concentration in houses over a closed Hungarian uranium mine » ; Science of The Total Environment, volume 367, Issues 2-3, 31 August 2006, pages 653-665 (Résumé).
- T.T. Taipale & K. Winqvista, Seasonal variations in soil gas radon concentration ; « Exposure to Enhanced Natural Radiation and its Regulatory Implications” Science of The Total Environment ; volume 45, October 1985, pages 121-126 doi:10.1016/0048-9697(85)90211-6 (Résumé).
- JC Baubron, BRGM, Mesures radon effectuées dans une habitation d'Hyverneresse, Commune de Gioux (Creuse) février 1999, rapport : R 40526.
- Selon Tatz, 1982, cité par Eric Glon, in « Protéger la nature, est-ce protéger la société », in Géographie et cultures, no 69, 2009).
- Edward P. Radford, M.D., and K. G. St. Clair Renard, M.D., Lung Cancer in Swedish Iron Miners Exposed to Low Doses of Radon Daughters ; N Engl J Med 1984; 310:1485-1494 June 7, 1984.
- Lene H. S. Veiga, Eliana C. S. Amaral, Didier Colin and Sérgio Koifman (2006) « A retrospective mortality study of workers exposed to radon in a Brazilian underground coal mine » ; Radiation and Environmental Biophysics ; volume 45, Number 2, 125-134, DOI: 10.1007/s00411-006-0046-3 (Résumé).
- A. Qureshi, D. M. Kakar, M. Akram, N. U. Khattak, M. Tufail, K. Mehmood, K. Jamil and H. A. Khan, « Radon concentrations in coal mines of Baluchistan, Pakistan » ; Journal of Environmental Radioactivity ; Volume 48, Issue 2, April 2000, Pages 203-209 ; doi:10.1016/S0265-931X(99)00065-X (Résumé).
- Kusnetz H.L (1956) « Radon daughters in mine atmospheres ». Amer. industr. Hyg. A4ss. Quart., 17, 85-88.
- Recommendations of the International Commission on Radiological Protection (1959). Publication 2.
- Lucas H.F and Gabrysh A.F (1966) « Radon in coal mines », ANL 7220.
- Goldman, K P (1965) Mortality of coal miners from carcinoma of the lung. Brit. J. industr. Med., 22, 72-77.
- Haque A.K.M.M and Collinson A.J.L (1967) Radiation dose to the respiratory system due to radon and its daughter products. Hlth. Phys., 13, 431-443.
- Jacobi W (1964) « The dose to the human respiratory tract by inhalation of short lived » 2Rn- and “Rn-decay products”. Hlth. Phys., 10, 1163-1175.
- S. Xue, J. Wangb, J. Xiea et J. Wub, « A laboratory study on the temperature dependence of the radon concentration in coal » ; International Journal of Coal Geology ; volume 83, Issue 1, 1 July 2010, pages 82-84 ; doi:10.1016/j.coal.2010.03.003 (Résumé).
- A. Janssens at al. (1983) Transients in the exhalation of radon caused by changes in ventilation and atmospheric pressure, Proce. Of an Int. Sem., Anacapri (Italy), 3-5. Oct., Rad. Prot. Dos., vol. 7, No. 1-4, p. 81-86, Nuc. Tech. Pub., 1987.
- Boyd, J. T., Doll, R., Faulds, J. S., and Leiper, J. P. (1970). Lung cancer in iron-ore (haematite) miners. Brit. J. industr. Med., 26, 97.
- Faulds J.S and Stewart M.J (1956) Carcinoma of the lung in haematite miners. J. Path. Bact., 72, 353-366.
- S. Çile, N. Altınsoy et N. Çelebi, Radon concentrations in three underground lignite mines in Turkey ; Oxford Journals ; Mathematics & Physical SciencesMedicine ; Radiation Protection Dosimetry, volume 138, Issue 1, pages 78-82. (Résumé).
- R. Baldık, H. Aytekin, N. Çelebi, B. Ataksor et M. Taşdelen, Radon concentration measurements in the AMASRA coal mine, Turkey ; Oxford Journals ; Mathematics & Physical Sciences Medicine ; Radiation Protection Dosimetry ; Volume118, Issue1 p. 122-125 (Résumé).
- Güngör Yener and Esref Küçükta, « Concentrations of radon and decay products in various underground mines in western Turkey and total effective dose equivalent » ; Analyst, January 1998, vol. 123 (31–34) (Article intégral en ligne).
- Abdullah Fişne Gündüz Ökten and Nilgün Çelebi, Radon concentration measurements in bituminous coal mines ; Oxford Journals, Mathematics & Physical SciencesMedicine, Radiation Protection Dosimetry, Volume113, Issue2, p. 173-177. (Résumé).
- Michael Hendryx, Kathryn O’Donnell & Kimberly Horn, “Lung cancer mortality is elevated in coal-mining areas of Appalachia” ; Lung Cancer ; volume 62, Issue 1, October 2008, pages 1-7 ; doi:10.1016/j.lungcan.2008.02.004.
- Fond aérochimique : néologisme francophone correspondant au « Radiation background of the natural environment » des anglophones.
- Skubacz K. ; Lebecka J. ; Chalupnik S. ; Wysocka M. « Possible changes in radiation background of the natural environment caused by coal mine activity » ; 1992, vol. 14, no2, p. 149-153 (9 ref.) (Fiche Inist-CNRS).
- Lane R.S, Tomášek L, Zablotska L.B, Rage E, Momoli F & Little J (2019) Low radon exposures and lung cancer risk: joint analysis of the Czech, French, and Beaverlodge cohorts of uranium miners. International archives of occupational and environmental health, 92(5), 747-762. (résumé)
- « The weight of evidence is that the ecological analyses of Cohen can be rejected. »(en) Ionizing Radiation, Part 2 : Some Internally Deposited Radionuclides, vol. 78, World Health Organization, International Agency for Research on Cancer, coll. « IARC Monographs on the Evaluation of Carcinogenic Risks to Humans », (lire en ligne).
- Jean-Marc Jancovici : « À propos de quelques objections fréquentes sur le nucléaire civil ».
- http://www.irsn.fr/FR/expertise/publications-professionnels/Documents/IRSN_EnPratique_Limiter-Radon-Habitation.pdf.
- O. Catelinois, A. Rogel, D. Laurier et al., « Lung Cancer Attributable to Indoor Radon Exposure in France: Impact of the Risk Models and Uncertainty Analysis », Environmental Health Perspectives, National Institute of Environmental Health Science, vol. 114, no 9, , p. 1361–1366 (PMID 16966089, DOI 10.1289/ehp.9070, lire en ligne, consulté le ).
- « Les risques liés à l'exposition domestique au radon », La Revue Prescrire (ISSN 0247-7750), no 281, mars 2007.
- [PDF]« Fiche repère Radon et Cancer, État des connaissances en date du 10 octobre 2011 » [archive du ], Institut National du Cancer, (consulté le ).
- Le radon, aspects historiques et perception du risque, par Roland Masse. Contrôle no 153 : le radon : évaluation et gestion du risque, ASN, juin 2003.
- (en) [PDF] Correllation between mean radon levels and lung cancer rates in US counties : a test of the Linear-No Threshold theory, Bernard L. Cohen (University of Pittsburgh), 1988.
- Bernard L Cohen : Radon exposure and the risk of lung cancer, 2001 J. Radiol. Prot. 21 64-65 .
- (en) [PDF] Topics Under Debate: Does Exposure to Residential Radon Increase the Risk of Lung Cancer? Radiation Protection Dosimetry, vol. 95, no 1, p. 75-81 (2001).
- (en) S Darby, « Radon in homes and risk of lung cancer: collaborative analysis of individual data from 13 European case-control studies », BMJ, vol. 330, no 7485, , p. 223–0 (ISSN 0959-8138, PMID 15613366, PMCID 546066, DOI 10.1136/bmj.38308.477650.63, lire en ligne, consulté le ).
- Le risque du cancer du poumonest-il surestimé ?, André Aurengo, Contrôle no 153 : le radon : évaluation et gestion du risque, ASN, juin 2003.
- Radioactivité et santé, Pr André Aurengo novembre 2003. « http://www.wonuc.org/xfiles/aurengo1.htm »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ).
- Arrêté du 22 juillet 2004 relatif aux modalités de gestion du risque lié au radon dans les lieux ouverts au public .
- http://www.legifrance.gouv.fr/affichTexte.do?cidTexte=JORFTEXT000019414788&dateTexte=.
- Bilan du plan d’actions 2005-2008 pour la gestion du risque lié au radon..
- [PDF]Commission spécialisée Risques liés à l’environnement, « Avis sur les projets de décret et d’arrêtés relatifs à la protection des personnes contre le risque lié au radon dans les bâtiments », Haut Conseil de la santé publique, (consulté le ).
- La relation dose-effet et l’estimation des effets cancérogènes des faibles doses de rayonnements ionisants, rapport conjoint académie des sciences () / académie de médecine (5 octobre 2004), Maurice Tubiana et André Aurengo.
- A. PAWULA, 1997 : « Contribution à l’explication des anomalies du radon 222 dans le milieu naturel. Point de vue d’un géologue », séminaire SUBATECH, École des mines de Nantes, Laboratoire de physique subatomique et des technologies associées.
- Dipak Ghosh, Argha Deb, Rosalima Sengupta (2009) Anomalous radon emission as precursor of earthquake (Review Article) ; Journal of Applied Geophysics, Volume 69, Issue 2, October 2009, Pages 67-81 (résumé).
- M. Singh, M. Kumar, R. K. Jain and R. P. Chatrath, Radon in ground water related to seismic events ; Radiation Measurements Volume 30, Issue 4, August 1999, Pages 465-469 doi:10.1016/S1350-4487(99)00049-9 (Résumé).
- Trique, M; Richon, P; Perrier, F; Avouac, JP; Sabroux, JC., Radon emanation and electric potential variations associated with transient deformation near reservoir lakes. NATURE, 399: (6732) 137-141. (Résumé).
- La mesure du Radon et de ses descendants à vie courte: la normalisation française et internationale. (11/06/2001) Marie-Christine Robé, Véronique Labed Congrès SFRP, Tours, 17-21 juin 2001.
- Norme française NF M 60-761-1 : Énergie nucléaire – Mesure de la radioactivité dans l'environnement – Eau. Partie 1 : Le radon 222 et ses descendants à vie courte dans l’eau : leurs origines et méthodes de mesure. août 2007.
- Norme française NF M 60-761-3 : Énergie nucléaire – Mesure de la radioactivité dans l'environnement – Eau. Partie 3 : Le radon 222 et ses descendants à vie courte dans l’eau : mesures par dégazage. Mai 2008.
- G. Ielsch, D. Thiéblemont, J. Perrin, G. Tymen EOS, Geophysical and geochemical tools for radon mapping at a regional scale.(01/01/1999) ; Transactions, American Geophysical Union, 1999 Fall Meeting, vol. 80, no 46, november 16, 1999/Supplement.
- Géraldine Ielsch, La cartographie radon en France : mise au point d’une méthodologie prédictive d’identification des zones potentiellement à risque.(09/11/1999) Séminaire BRGM Orléans / 9 novembre 1999.
- Quantification of the radon exhalation rate at the surface of the soil : a new predictive tool based on the physical and chemical properties of geological formations and soils.(10/05/2001) Ielsch., G., Ferry, C., Tymen, G. and Robé, M.-C., Third European Symposium on Protection against Radon at home and at work - Liège, 10-11 May 2001.
- G. leisch, C. Ferry, G. Tymen and M.C. Robé, Prediction of areas presenting a high radon exhalation potential: A new methodology based on the properties of geological formations and soils. (01/07/2002) Actes du congrès ECORAD, 3-7 septembre 2001, Aix en Provence, France Radioprotection - Colloques, volume 37, C1-1211/ C1-1216.
- An experimental method for measuring the radon-222 emanation factor in rocks.(15/12/2002) C. Ferry, P. Richon, A. Beneito, J. Cabrera and J. -C. Sabroux Radiation Measurements - volume 35, Issue 6, December 2002, pages 579-583.
- Ministère de l'écologie Radon, consulté 2013-07-07.
- décision n° 2015-DC-0506 de l'Autorité de sûreté nucléaire du 9 avril 2015 relative aux conditions suivant lesquelles il est procédé à la mesure de l'activité du radon prise en application de l'article R. 1333-15 du code de la santé publique.
- arrêté du 5 juin 2009 portant homologation de la décision n° 2009-DC-0135 de l'Autorité de sûreté nucléaire du 9 avril 2015 relative aux conditions suivant lesquelles il est procédé à la mesure de l'activité du radon prise en application de l'article R. 1333-15 du code de la santé publique, abrogé en 2015 et remplacé par un Arrêté du 22 juillet 2015, JORF n°0176 du 1 août 2015 page 13136.
- Arrêté du 22 juillet 2015 portant homologation de la décision n° 2015-DC-0506 de l'Autorité de sûreté nucléaire du 9 avril 2015 relative aux conditions suivant lesquelles il est procédé à la mesure de l'activité du radon prise en application de l'article R. 1333-15 du code de la santé publique, Légifrance, publié au JORF n°0176 le 1 août 2015 page 13136.
- Arrêté du 7 août 2008 relatif à la gestion du risque lié au radon dans les lieux de travail.
- Arrêté du 22 juillet 2004 relatif aux modalités de gestion du risque lié au radon dans les lieux ouverts au public.
- Rauch SA, Henderson SB (2013) A comparison of two methods for ecologic classification of radon exposure in british columbia: residential observations and the radon potential map of Canada ; Can J Public Health. 2013 Mar 6;104(3):e240-5. (résumé).
- RemWeb/.
Voir aussi
Bibliographie
- Bujdosó E (1999) « Radon in environment, A current bibliography » ; Chemistry and Materials Science ; Journal of Radioanalytical and Nuclear Chemistry ; volume 241, Number 2, 439-449, DOI: 10.1007/BF02347484 ; Bibliographic Collection (Springerlink ; résumé)
- Clement C.H, Tirmarche M, Harrison J.D, Laurier D, Paquet F, Blanchardon E & Marsh J.W (2010) Lung cancer risk from radon and progeny and statement on radon. Annals of the ICRP, 40(1), 1-64.
- De Villiers A.J & Windish J.P (1964) Brit. J. Indust. Med., 21, 94
- Frank A.L & Benton E.V. (1977) Radon dosimetry using plastic nuclear track detectors ; Nuclear Track Detection, Volume 1, Issues 3–4, December 1977, Pages 149-179 (résumé)
- Harris S.J (1954), Arch. Indust. Hyg., 10, 54
- Jacoe B.W (1953) Arch. Indust. Hyg., 8, 118
- Lucas H.F & Gabrysh A.F (1966) Radon in Coal Mines, ANL-7060
- Olivier Catelinois (2004), Évaluation des risques associés aux rayonnements ionisants, Cancers du poumon après exposition domestique au radon et cancers de la thyroïde après exposition accidentelle aux iodes radioactifs, Thèse de doctorat en épidémiologie/santé publique ; Université Paris 11.
- Tirmarche M, Harrison J.D. , Laurier D, Paquet F, Blanchardon E & Marsh J.W (2010) Lung Cancer Risk from ICRP Publication 115: Radon and Progeny and Statement on Radon. Ann. ICRP. 40, 1.
Articles connexes
Liens externes
- (en) « Technical data for Radon » (consulté le ), avec en sous-pages les données connues pour chaque isotope
Pour en savoir plus sur la prévention contre les risques associés au radon, voir notamment les liens suivants :
- Le radon – évaluation et gestion du risque (ASN, France)
- Métrologie du radon dans les bâtiments (IRSN, France)
- IRSN : dossier avec notamment l'Atlas Radon, par commune (Institut de Radioprotection et de Sûreté Nucléaire, France)
- Radon-France
- Le radon, comment s'en prémunir (AFCN, Belgique),
- Le radon (BAG, Suisse)
- Tout sur le radon, brochures, exemples, etc. (Office fédéral de la santé publique Berne, Suisse)
- Le radon domiciliaire – Ministère de la Santé et des Services sociaux du Québec
- Le radon, un coupable pernicieux – Association pulmonaire du Québec
- Impact sanitaire du radon domestique : de la connaissance à l’action. Institut de veille sanitaire, Bulletin épidémiologique hebdomadaire / no 18-19.
- [PDF] Roger Cadiergues, La Qualité de l'air : le radon, livret 2010, 18 pages
- WHO handbook on indoor radon.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux Alcalins |
Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métal- loïdes |
Non- métaux |
Halo- gènes |
Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
| Superactinides | |||||||||
- Portail de la chimie
