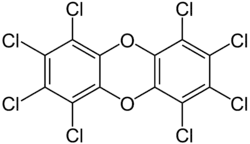
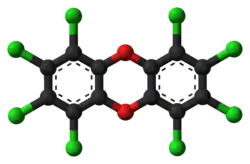
Octachlorodibenzodioxine
L’octachlorodibenzodioxine (abrégé : OCDD) est l’un des congénères des dioxines couramment trouvés dans les fumées et dans certains sols pollués, il appartient au groupe des polychlorodibenzo-p-dioxines (PCDD). Classé toxique[4] et écotoxique[4], c'est aussi un précurseur d'autres organochlorés toxiques.
| Octachlorodibenzodioxine | |||
| |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 1,2,3,4,6,7,8,9-octachlorodibenzo-p-dioxine | ||
| Synonymes |
octachlorodibenzo-p-dioxine |
||
| No CAS | |||
| No ECHA | 100.223.031 | ||
| PubChem | 18636 | ||
| ChEBI | 81566 | ||
| SMILES | |||
| InChI | |||
| Apparence | cristaux incolore ou poudre cristalline blanche[1] | ||
| Propriétés chimiques | |||
| Formule | C12Cl8O2 [Isomères] |
||
| Masse molaire[2] | 459,751 ± 0,026 g/mol C 31,35 %, Cl 61,69 %, O 6,96 %, |
||
| Propriétés physiques | |||
| T° fusion | 330 à 332 °C[1] | ||
| T° ébullition | 510 °C[1] | ||
| Solubilité | eau : 8,70 × 10−13 M[1] sol. en g/l : acide acétique 0,048 ; anisole 1,730 ; chloroforme 0,562 ; ortho-dichlorobenzène 1,832 ; dioxane 0,384 ; diphényl oxyde 0,841 ; pyridine 0,400 ; xylène 3,575[1] |
||
| Pression de vapeur saturante | 8,25 × 10−13 mmHg à 25 °C[1] | ||
| Précautions | |||
| SGH[1] | |||
  |
|||
| Transport[1],[3] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 1 mg/kg (rat, oral)[1] | ||
| LogP | (eau/octanol) 8,2[1] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
Écotoxicité
Elle est encore mal cernée mais cette molécule est étiquetée comme dangereuse pour l'environnement.
Une étude d'indicateurs (multi-substances) basés sur la bioaccumulation de toxines environnementales par des Gammares élevés en cage (crustacé d'eau douce) a montré l’influence de la contamination chimique (dont par cette molécule) sur l’abondance des macroinvertébrés dans les cours d’eau de France[5].
Toxicité
La toxicité de cette molécule a été étudiée et d'abord jugée bien moins toxique que celle de la TCDD (ou 2,3,7,8-tétrachlorodibenzo-p-dioxine, plus connue sour le nom de dioxine de Seveso), mais elle a été réévaluée à Genève en juin 2005 par un panel d'experts de l'OMS et du « Programme international pour la sécurité des substances chimiques »[6].
C’est l’un des congénères dominants de la dioxine dans les émissions de fumées, et fréquemment retrouvé dans les sols pollués. Mais notamment parce que bien moins soluble que par exemple la TCDD, elle ne serait pas facilement bioaccumulée, faisant que sa toxicité effective est moins importante que celle des dioxines les plus problématiques[réf. nécessaire].
(Pour plus de détails, voir Dioxines et composés apparentés aux dioxines).
Facteur d’équivalence toxique (FET)
Le « facteur d’équivalence toxique » (FET) fixé à cette molécule en 1998 par l’OMS était 0,0001 (bien en dehors du 10e centile de la plage des valeurs de REP in vivo et in vitro de la base de donnés de Slone Haws et al. (2006) utilisée par l'OMS pour cette mise à jour. En 2005, les seules PRP in vivo répondant aux conditions strictes de la base de données (Haws et al., 2006) étaient basées sur une étude rapportée par deux articles scientifiques de toxicité subchronique (utilisant chacune différents paramètres) : Wermelinger et al. (1990)[7] et Fattore et al. (2000)[8], cette dernière étude plaidant pour un FET supérieur à 0,0001. Certains experts étaient alors gênés par le fait que les animaux (rat de laboratoire) utilisés dans la publication la plus récente (Fattore et al., 2000) étaient les mêmes que ceux utilisés 10 ans plus tôt dans l'étude de Wermelinger et al. (1990) ; ils étaient aussi gênés par le fait que l'octachlorodibenzo-p-dioxine (OCDD) ajouté à la nourriture des rats était contaminé par d'autres congénères (Dioxin-like) dont le 2,3,4,7,8-PeCDF. Puis sur la base des données du National Toxicology Program (NTP) qui venaient d'être publiées (2005) pour le 2,3,4,7,8-PeCDF[9], il est apparu que la contamination rapportée par le 2,3,4,7,8-PeCDF[10] n’était pas toxicologiquement significative. Elle n'influence pas les résultats des travaux de Fattore et al. publiés en 2000, car elle n'était présente qu'à des doses très inférieures à la dose sans effet observé (DSEO), pour tous les paramètres examinés.
Les seules données in vivo disponibles étaient trop limitées pour convaincre à elles seules le groupe d'experts d'augmenter la valeur du facteur d'équivalence toxiue de ce composé à 0,001 ; mais la combinaison de ces informations avec celles venant de données in vitro fournies par Haws[11] a justifié une augmentation de la valeur du FET, qui a été augmentée en 2005 à 0,0003 (contre 0,0001 initialement)). Le groupe d'experts s'est dit « conscient des conséquences que pourrait avoir l'augmentation de la valeur de cette valeur TEF de l'OMS pour les TOCD, du point de vue de la réglementation et de la gestion des risques », tout en rappelant que si les concentrations d’OCDD sont élevées dans certaines matrices environnementales, la TEQ ne doit pas s'appuyer sur les FET pour les matrices environnementales abiotiques comme le sol.
OCDD et pesticides
Les pesticides chlorés (du groupe des organochlorés) peuvent aussi contenir en tant qu'impuretés des dibenzo-p-dioxines et des dibenzofuranes (PCDD/F) ainsi que leurs précurseurs. "La formation de précurseurs de PCDD/F (OCDD principalement) peut aussi être médiée par la lumière ultraviolette (UV)" artificielle ou provenant du soleil).
Les modifications observées en laboratoire (par Holt et ses collègues en 2012) du rapport de proportion entre congénères après exposition aux UV suggèrent que les sources de molécules issues de pesticides, et ressemblant à des dioxines après exposition au soleil, pourraient ne pas être reconnues sur la base des données établies à partir de l'étude des impuretés de fabrication[12]. Ces modifications fournissent également des informations préliminaires sur les voies de formation possibles et les types de précurseurs impliqués[12].
Notes et références
- PubChem CID 18636.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Octachlorodibenzo-p-dioxin sur biosynth.com
- Fiche PucChem[source insuffisante]
- Alric, B., Geffard, O., Chandesris, A., Ferreol, M., François, A., Perceval, O., … et Chaumot, A. (2019), Multi-substance indicators based on caged Gammarus bioaccumulation reveal the influence of chemical contamination on stream macroinvertebrate abundances across France, Environmental Science & Technology (résumé)
- « {{{1}}} » . source : M. Van den Berg, L.S. Birnbaum, M. Denison, M. De Vito, W. Farland, M. Feeley, H. Fiedler, H. Hakansson, A. Hanberg, L. Haws, M. Rose, S. Safe, D. Schrenk, C. Tohyama, A. Tritscher, J. Tuomisto, M. Tysklind, N. Walker, R.E. Peterson (2006) The 2005 World Health Organization reevaluation of human and mammalian toxic equivalency factors for dioxins and dioxin-like compounds, Toxicol. Sci. 93 223–241.
- Wermelinger, M., Poiger, H. et Schlatter, C. (1990), Results of a 9-month feeding study with OCDD and OCDF in rats. Organohalogen Compd., 1, 221–224.
- Fattore, E., Trossvik, C. et Hakansson, H. (2000), Relative potency values derived from hepatic vitamin A reduction in male and female Sprague-Dawley rats following subchronic dietary exposure to individual polychlorinated dibenzo-p-dioxin and dibenzofuran congeners and a mixture thereof, Toxicol. Appl. Pharmacol., 165, 184–194.
- Walker, N. J., Crockett, P. W., Nyska, A., Brix, A. E., Jokinen, M. P., Sells, D. M., Hailey, J. R., Easterling, M., Haseman, J. K., Yin, M. et al. (2005), Dose-additive carcinogenicity of a defined mixture of “dioxin-like compounds”. Environ. Health Perspect. 113, 43–48.
- La contamination rapportée de l'OCDD était de 2,5 ppm (pg/µg).
- Haws, L. C., Su, S. H., Harris, M., Devito, M. J., Walker, N. J., Farland, W. H., Finley, B. et Birnbaum, L. S. (2006), Development of a refined database of mammalian relative potency estimates for dioxin-like compounds. Toxicol. Sci. 89, 4–30.
- Holt E, Weber R, Stevenson G et Gaus C (2012), Formation of dioxins during exposure of pesticide formulations to sunlight. Chemosphere, 88(3), 364-370.
Annexes
Articles connexes
- Dioxine
- Chloracné
- 2,3,7,8-Tétrachlorodibenzo-p-dioxine (dioxine de Seveso)
- Incinérateur de déchets
- Organochloré
- Perturbateur endocrinien
- Cancérogène
- Mutagène
- Incinération des déchets
- Facteur d'équivalence toxique
- Poisson : élevage en eaux troubles (documentaire)
- Directive IPPC (Prévention et contrôle intégrées de la pollution) (Union Européenne)
- Furane
Liens externes
- Les dioxines et leurs effets sur la santé sur who.int
- Consensus scientifique sur les dioxines sur greenfacts.org
- Guide EMEP des Inventaires sur les Emissions (EMEP/CORINAIR): aide à l’application des méthodologies des inventaires sur l’atmosphère. ; URL du Protocole : http://www.unece.org/env/lrtap/pops_hl.htm URL pour EMEP: http://www.EMEP.int ; URL du Guide: http://reports.eea.eu.int/EMEPCORINAIR3/en
- Procédures de quantification et déclaration harmonisées pour les émissisons de produits toxiques (HARP-HAZ) vers le milieu marin (géré par l’Autorité Norvégienne de Contrôle de la Pollution (SFT), plus particulièrement fait pour les pays d’Europe du Nord ; URL : http://sft.no/english/harphaz/
- bureau de centralisation (http://www.chem.unep.ch/prtr/Default.htm) des registres des Rejets et des Transferts de Polluants (PRTR) (cf. recommandations de l'Agenda 21 (chapitre 19) du CNUED voulant que les gouvernements et organisations internationales appropriés, avec la coopération de l’industrie, œuvrent notamment à « améliorer les bases de données et les systèmes d’information concernant les produits chimiques, tels que les programmes d’inventaires sur les émissions… »
Bibliographie
- Alric, B., Geffard, O., Chandesris, A., Ferreol, M., François, A., Perceval, O., … et Chaumot, A. (2019), Multi-substance indicators based on caged Gammarus bioaccumulation reveal the influence of chemical contamination on stream macroinvertebrate abundances across France, Environmental Science & Technology (résumé).
- Portail de la chimie
- Portail de l'écotoxicologie
