Ostéomyélite
L’ostéomyélite hématogène est une infection osseuse due à un germe qui atteint l'os par voie hématogène. Elle siège préférentiellement au niveau des métaphyses des os longs.
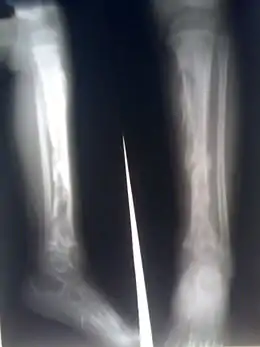
| Médicament | Nafcillin (en), ciprofloxacine, oxacilline, cloxacilline, dicloxacilline (en), méticilline et acexamic acid (d) |
|---|---|
| Spécialité | Rhumatologie et médecine podiatrique (en) |
| CIM-10 | M86 |
|---|---|
| CIM-9 | 730 |
| DiseasesDB | 9367 |
| MedlinePlus | 000437 |
| eMedicine | 967095 |
| MeSH | D010019 |
| Patient UK | Osteomyelitis-pro |
![]() Mise en garde médicale
Mise en garde médicale
Elle doit être distinguée des autres atteintes osseuses par inoculation directe ou par contiguïté.
Physiopathologie
Phase congestive

Lors d'une septicémie ou une bactériémie, le germe atteint l'os par voie sanguine. Au niveau de la métaphyse, le flux sanguin se ralentit ce qui favorise la fixation et le développement des germes.
Abcès sous-périosté
La diffusion de l'infection se fait à travers les canaux de Havers et Volkmann de la corticale interne jusqu'à atteindre le périoste. Ce dernier s'épaissit, se décolle et délimite un abcès sous-périosté.
Stade de nécrose osseuse
Elle survient en l'absence d'un traitement précoce de l'infection et aboutit à une ostéomyélite chronique. L'interruption de la vascularisation osseuse tant centromédullaire que sous-périostée entraîne une nécrose osseuse avec formation d'un os mort avasculaire, libre dans l'abcès, dénommé séquestre osseux.
Une classification physiopathologique est proposée, basée sur les lésions vasculaires engendrées par l'infection, la classification d'Essaddam et Dargouth[1] :
- stade 0 : stade de thrombophlébite intra-osseuse ;
- stade 1 : stade de la suppression de la vascularisation endostée par l'œdème inflammatoire intra-osseux ;
- stade 2 : stade de l'abcès sous-périosté, ou début de la dévascularisation périostée ;
- stade 3 : stade de la dévascularisation périostée. À ce stade l'os a perdu ses deux vascularisations endoste et périostée ;
- stade 4 : stade de la nécrose osseuse.
Cette nouvelle classification permet de définir l'ostéomyélite comme une dévascularisation progressive de l'os d'origine infectieuse. Traitée aux stades 1, 2 et 3, l'ostéomyélite ne passe pas à la chronicité. Traitée au stade 4 elle passe à la chronicité.
Tableau clinique
L'ostéomyélite survient fréquemment au cours de la seconde enfance avec une moyenne d'âge de 6 ans. Elle est exceptionnelle en période néonatale. Elle siège préférentiellement au niveau des métaphyses les plus fertiles, « proche du genou », « loin du coude ». Dans 30 à 40 % des cas, on note la survenue d'un traumatisme mineur dans les jours précédents l'apparition de l'infection. Dans le cas typique, il s'agit d'un garçon (Sex Ratio 3/1) qui se plaint de douleurs métaphysaires circonférentielles à l'extrémité d'un os long. La douleur a un début brutal, pseudo-fracturaire et est accompagné d'une impotence fonctionnelle du membre atteint. La mobilisation douce de l'articulation adjacente est possible. Le syndrome infectieux est marqué avec une fièvre supérieure à 38 °C, une altération de l'état général, des frissons et des sueurs. En phase de début, il n'y a pas ou peu de signes locaux. Plus tardivement, on peut observer un œdème et une inflammation localisée. Habituellement, on ne retrouve pas d'adénopathie. D'autres manifestations doivent faire rechercher une ostéomyélite surtout dans un contexte fébrile :
- un état d'agitation ou de prostration ;
- une pseudoparalysie d'un membre chez le nourrisson ou le nouveau-né ;
- des convulsions ;
- une boiterie.
Devant toute fièvre chez un enfant, il faut palper toutes les métaphyses fertiles et mobiliser toutes les articulations d'autant plus que les douleurs siègent « proche du genou et loin du coude ». Le reste de l'examen clinique recherchera une porte d'entrée soit :
- cutanée ;
- urinaire ;
- ORL et pulmonaire ;
- méningée.
Examens complémentaires
Bilan biologique
- NFS montre une hyperleucocytose à polynucléaires neutrophiles. L'absence d'élévation ne doit pas faire récuser le diagnostic.
- CRP (Protéine C réactive) (N < 10 mg/l) : elle augmente précocement dès la 6e heure. Elle peut être normale dans 20 % des cas.
- Orosomucoïde (N < 1 g/l) est rarement normale.
- VS (N < 20 à la 1re heure) : elle augmente plus tardivement que la CRP de même sa normalisation est beaucoup plus lente.
Bilan à visée bactériologique
Il est à réaliser avant mise en route de l'antibiothérapie. Staphylococcus aureus est le germe responsable dans la majorité des cas. Le streptocoque de groupe A (Streptococcus pyogenes) est le second germe par ordre de fréquence. En dessous de 3 ans, c'est Hæmophilus influenzæ de type G qui est le plus souvent mis en évidence.
Des hémocultures doivent être réalisées, même en l'absence de fièvre mais surtout en cas de pics fébriles de frissons. Elles sont positives dans 40 à 60 % des cas. Une ponction métaphysaire peut être proposée, sous anesthésie générale et contrôle par amplificateur de brillance. Elle permet l'isolement du germe dans 90 à 100 % des cas.
Autres prélèvements
- examen cytobactériologique urinaire (ECBU) ;
- prélèvements ORL ;
- prélèvement d'une lésion cutanée ;
- liquide céphalorachidien (LCR) ;
- électrophorèse de l'hémoglobine à la recherche d'une drépanocytose (sujets noirs ou maghrébins).
Bilan radiographique
Les radiographies standard de face, profil complété par des clichés comparatifs et de 3/4 en cas de doute sur une lésion. Au stade du début, on recherche un flou des parties molles adjacentes à la métaphyse. À la phase d'état, on recherche une apposition de fines lamelles osseuses à la corticale métaphysaire correspondant à la réaction périostée. Plus tardivement apparaissent :
- des lacunes métaphysaires ;
- des irrégularités des corticales ;
- des séquestres osseux (fragment osseux d'aspect dense libre et irrégulier).
L'aspect radiographique de certaines tumeurs malignes, tel que le sarcome d'Ewing, peut simuler une ostéomyélite. Le diagnostic doit être évoqué en cas d'évolution torpide ou atypique et confirmé par une biopsie chirurgicale.
La scintigraphie osseuse au technétium 99 m
Elle montre une hyperfixation mais ne permet pas de faire la différence entre infection, tumeurs ou une autre pathologie inflammatoire. Elle sera demandée en cas de doute diagnostique ou pour rechercher une atteinte multifocale. L'utilisation du Gallium 67 serait plus spécifique de l'infection car l'isotope se fixe sur les leucocytes (mais discutable chez l'enfant du fait de la longue période de l'isotope).
L'échographie
Elle permet le dépistage et la ponction guidée de l'abcès périosté. La découverte de l'abcès sous périosté, rendue précoce par l'échographie, permet de préciser le moment et la voie d'abord du traitement chirurgical. Grâce à ce protocole il y a disparition du passage à la chronicité de la maladie[1].
L'I.R.M.

Elle donne des renseignements précoces avant la radiographie standard mais sa réalisation chez l'enfant nécessite parfois une anesthésie générale. Elle montre un hyposignal en T1 et un hypersignal en T2. Après injection de Gadolinium, on note un réhaussement des tissus inflammatoires. Par contre, au niveau de l'abcès, on n'observe pas de réhaussement ou seulement en périphérie.
Le scanner
Il permet d'étudier surtout l'extension osseuse dans les formes chroniques (aspect hétérogène) et surtout de détecter la présence d'un séquestre, fragment d'os mort qui agit comme un corps étranger et favorise la persistance des fistules : c'est un élément essentiel de l'indication chirurgicale dans les suppurations persistantes. Il permet également d'étudier les localisations vertébrales et sacro-iliaques.
Formes cliniques
Ostéomyélite subaigue
Elle se distingue de l'ostéomyélite aiguë hématogène par son début insidieux, une symptomatologie fruste avec peu de signes locaux. Dans les cas typiques, l'évolution est bénigne. Le bilan biologique est peu perturbé. L'aspect radiographique est une lacune épiphysaire bien circonscrite mais qui parfois atteint la corticale. Le traitement reste controversé. Classiquement, on préconise l'administration d'un antibiotique à visée anti-staphylococcique. Certaines observations rapportées ont évolué vers la guérison sans traitement.
Ostéomyélite chronique
C'est l'évolution d'une ostéomyélite aiguë en l'absence d'un traitement précoce et adapté. Les bactéries en cause sont les mêmes que dans l'ostéomyélite aiguë. En cas de suppuration chronique, on peut observer une surinfection par des germes tels que les Pseudomonas. Brodie et Garre ont décrit des ostéomyélites chroniques d'emblée[réf. nécessaire]. Elles ont été dénommées ostéomyélites chroniques primaires. D'autres formes d'ostéomyélites chroniques d'emblée ont été décrites ; c'est le cas des formes hyperostosantes chroniques.
L'abcès de Brodie
C'est un abcès chronique de l'os décrit par Benjamin Brodie en 1832. Il est défini par son aspect radiologique quelle que soit son agressivité. Il se présente sous forme d'une lacune purement intra-osseuse, de siège métaphysaire ou métaphyso-épiphysaire bordée par une zone de sclérose osseuse.
Évolution et complications
Complications infectieuses
Il existe un risque évolutif d'infection à distance en cas de traitement tardif : staphylococcie pleuro-pulmonaire, péricardite, phlegmon péri-néphrétique, péritonite…
La survenue d'un choc septique est possible avec coagulopathie de consommation, coagulation intravasculaire disséminée, (CIVD) et décès.
Traitée rapidement elle guérit avec des séquelles minimes, l'hyperhémie inflammatoire peut entraîner une poussée de croissance qui se traduira par une inégalité de longueur des membres inférieurs de 1 à 2 cm.
Autres complications
- Une ischémie aiguë d'un membre doit faire rechercher une compression par un abcès sous-périosté ;
- une phlébite peut aussi survenir en cours d'évolution (présence d'une circulation collatérale) ;
- un syndrome de loge peut survenir en phase aiguë ou chronique ;
- l'atteinte du cartilage de croissance est une complication grave entraînant des troubles de la croissance osseuse : raccourcissement, défaut d'axe amènent à des chirurgies correctrices.
Il existe également des complications articulaires à type de raideur.
Ostéomyélite chronique
L'inadaptation du traitement peut conduire à l'ostéomyélite chronique avec des lésions cutanées (fistule, ulcération, perte de substance), musculaires (amyotrophie, fibrose rétractile du quadriceps dans les atteintes fémorales), osseuses avec séquestre (perte d'os par séquestrectomie chirurgicale ou élimination spontanée).
Sur cet os fragile, la survenue de fracture pathologique est possible avec un risque de pseudarthrose.
Abcès de Brodie
C’est un stade évolutif constitué d’une nécrose purulente localisée, enkystée.
Il est défini par son aspect radiologique.
Arthrite
Vite traitée, la guérison est rapide et sans séquelle.
Une atteinte du cartilage articulaire peut entraîner une diminution de la mobilité, sa destruction conduisant à l’arthrodèse.
Une atteinte du cartilage de croissance épiphysaire, du cartilage métaphyso-épiphysaire peut entraîner des troubles de croissance, des destructions articulaires (épiphysiolyse septique).
Personnalités atteintes
La poétesse Sabine Sicaud est morte à quinze ans des conséquences d'une ostéomyélite.
Notes et références
- Essaddam H. Hammou A. « Ostéomyélites » Encycl. ed. Chir. (Elsevier, Paris); Radio-diagnostic-Neuroradiologie–appareil locomoteur 31-218B-10, 1998, 18 p.
Voir aussi
Article connexe
Liens externes
- Elsevier Masson, « Infections ostéoarticulaires de l'enfant », sur EM-Consulte (consulté le )
- Portail de la médecine
- Portail des maladies infectieuses
