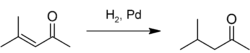Oxyde de mésityle
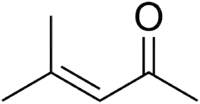
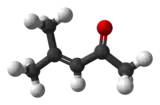
L'oxyde de mésityle est un composé organique de formule semi-développée CH3C(O)CH=C(CH3)2. Cette cétone α,β-insaturée est un composé liquide incolore volatile avec une forte odeur d'urine de chat[5].
| Oxyde de mésityle | |||
| |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 4-méthylpent-3-én-2-one | ||
| Synonymes |
isobutényl méthyl cétone; méthyl isobutényl cétone; isopropylidène acétone; 2-méthyl-2-pentén-4-one |
||
| No CAS | |||
| No ECHA | 100.005.002 | ||
| No CE | 205-502-5 | ||
| No RTECS | SB4200000 | ||
| PubChem | 8858 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore à jaune avec une odeur aromatique[1] | ||
| Propriétés chimiques | |||
| Formule | C6H10O [Isomères] |
||
| Masse molaire[2] | 98,143 ± 0,005 8 g/mol C 73,43 %, H 10,27 %, O 16,3 %, |
||
| Propriétés physiques | |||
| T° fusion | −59 °C[1] | ||
| T° ébullition | 130 °C[1] | ||
| Solubilité | eau : 30 g·l-1 à 20 °C[1] | ||
| Masse volumique | 0,85 g·cm-3[1] | ||
| T° d'auto-inflammation | 340 °C[1] | ||
| Point d’éclair | 24 °C[1] | ||
| Limites d’explosivité dans l’air | 1,4% à 10,1 vol. %[1] | ||
| Pression de vapeur saturante | 10,9 hPa à 20 °C 19,6 hPa à 30 °C 33,5 hPa à 40 °C 54,9 hPa à 50 °C[1] |
||
| Propriétés optiques | |||
| Indice de réfraction | = 1,44397[3] | ||
| Précautions | |||
| SGH[1] | |||
  |
|||
| Transport[1] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 710 mg/kg (souris, oral)[4] 1 000 mg/kg (lapin, oral)[4] 1 120 mg/kg (rat, oral)[4] 354 mg/kg (souris, i.p.)[4] 840 mg/kg (lapin, s.c.)[4] |
||
| CL50 | 10 g/m3/2 h (souris, inhalation)[4] 9 g/m3/4 h (rat, inhalation)[4] |
||
| LogP | 1,370 (octanol/eau)[4] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
Synthèse
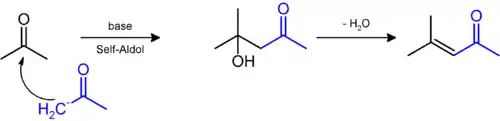
L'oxyde de mésityle est préparé par une crotonisation de l'acétone pour obtenir le 4-hydroxy-4-méthylpentan-2-one (diacétone alcool) qui, facilement déshydraté, fournit le produit[6]
Usage
La majeure partie de l'oxyde de mésityle produit industriellement est transformé en méthylisobutylcétone par hydrogénation :
Il sert également en tant que produit de départ pour la synthèse de terpènes et de parfums, ainsi qu'agent d'extraction de l'uranium et du thorium dans la flottation de minerais.
Notes et références
- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Mesityl oxide » (voir la liste des auteurs) et en allemand « Mesityloxid » (voir la liste des auteurs)..
- Entrée « Mesityl oxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 18/06/2016 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- CRC Handbook of Tables for Organic Compound Identification, 3e Ed., 1984. (ISBN 0-8493-0303-6).
- (en) « Oxyde de mésityle », sur ChemIDplus.
- Merck Index, 11e Ed., p. 5811.
- J. B. Conant, N. Tuttle, Mesityl oxide, Organic Syntheses, 1921, p. 53. DOI:10.15227/orgsyn.001.0053; Coll. Vol. 1, 1941, p. 345 (pdf).
- Portail de la chimie