Prolapsus mitral
Le prolapsus mitral (ou prolapsus de la valve mitrale ou ballonisation de la valve mitrale) est un trouble, habituellement bénin, du fonctionnement de la valve mitrale et pouvant être responsable d'une insuffisance mitrale plus ou moins importante. On le nomme parfois syndrome (ou maladie) de Barlow du nom du professeur de cardiologie sud-africain J.B. Barlow, qui l'a décrit. Il ne faut pas le confondre avec l'autre maladie de Barlow, qui correspond au scorbut, et qui est due à un déficit en vitamine C.
Pour les autres types de prolapsus, voir Prolapsus.

| Spécialité | Cardiologie |
|---|
| CIM-9 | 394.0 et 424.0 |
|---|---|
| OMIM | 607829 et 610840 157700, 607829 et 610840 |
| DiseasesDB | 8303 |
| MedlinePlus | 000180 |
| eMedicine | 759004 |
| MeSH | D008945 |
| Patient UK | Mitral-valve-prolapse |
![]() Mise en garde médicale
Mise en garde médicale
Historique
Il a été décrit par le cardiologue John Brereton Barlow dans une publication de 1963[1].
Causes et mécanisme
La valve mitrale est constituée de deux valvules (petite et grande valvules, chacune est composée de trois couches: atrialis, fibrosa, et spongiosa) et contrôle le flux sanguin qui part de l'oreillette gauche (ou atrium gauche) vers le ventricule gauche du cœur. Normalement, le flux s'écoule dans un seul sens, de haut en bas.
Dans le prolapsus mitral, l'une des valvules est augmentée en surface et devient épaisse, en raison de dépôts de protéoglycanes et de Dermatane sulfate, associés avec une désorganisation des fibres de collagène[2]. Le « cordage » qui la relie au pilier, permettant d'assurer la congruence et l'herméticité de la fermeture, peut être allongé. Le tout fait que la valve ne fonctionne pas correctement : lors de la contraction ventriculaire, la partie de la valve atteinte ne s'arrête pas au plan de l'anneau mais bascule dans l'atrium (on dit qu'« elle se prolabe »), permettant parfois à une partie du sang de fuir dans la mauvaise direction (c'est-à-dire de retourner dans l'atrium) signant une insuffisance mitrale.
La fuite est typiquement latéralisée. Ainsi un prolapsus de la petite valve induit une fuite qui se dirige contre la paroi séparant les deux oreillettes (septum interauriculaire) alors qu'une fuite provenant de la grande valve se dirige contre la paroi libre de l'oreillette gauche.
Il existe une prédisposition familiale[3], avec identification de plusieurs locus responsables[4],[5]. Des variants sur les gènes MCD1, SPTBN1, LTBP2, TGFB2, NMB et ALPK3 sont associés à des formes sporadiques de l'atteinte[6].
L'explication des symptômes généraux (fatigue, palpitations…) n'est pas claire et n'est pas corrélée avec l'importance de la fuite.
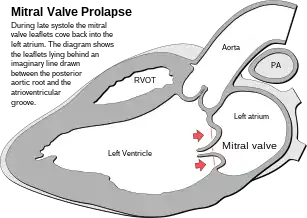
Sémiologie et diagnostic
Dans la majorité des cas, la cause est inconnue. Parfois, on retrouve une origine génétique.
Le prolapsus mitral ne produit très souvent aucun symptôme, et il est découvert lors d'examens cardiaques de routine. Lorsqu'ils existent (souvent chez une jeune femme), les symptômes possibles sont l'irrégularité des battements du cœur, la fatigue, des douleurs thoraciques, de l'anxiété, des palpitations, un essoufflement.
Le prolapsus mitral peut être entendu au stéthoscope en cas de fuite : typiquement le souffle survient après un clic mésosystolique (au milieu de la systole) et est dit « méso-télésystolique ».
L'échocardiographie (ou échographie cardiaque), permet de visualiser l'épaississement d'une des deux valvules et son mouvement de basculement en systole (prolapsus). La fuite mitrale peut être visualisée grâce au Doppler avec une estimation de son importance et de sa direction. L'examen peut être précisé par une échographie transœsophagienne. Néanmoins, le simple basculement d'une valve derrière le plan de l'anneau peut être une variation anatomique normale et ne suffit pas pour que l'on puisse parler de prolapsus[7].
Évolution
L'évolution se fait vers l'aggravation de la fuite mitrale, mais cela peut prendre de nombreuses années[8].
Des complications sont possibles : aggravation brutale de la fuite par rupture de cordage ou endocardite, passage en fibrillation atriale[9]...
Des cas de morts subites ont été décrits par fibrillation ventriculaire, avec une incidence annuelle pouvant aller jusqu'à 2 %[10]. Ils sont probablement en rapport avec une fibrose du muscle papillaire et du myocarde y attenant[11]. Le risque semble plus important en cas d'extrasystolie ventriculaire complexe au holter[10] ou la mise en évidence d'une fibrose localisée à l'IRM cardiaque[11].
Traitement
Des recommandations ont été publiées sur la prise en charge des valvulopathies cardiaques. Celles, américaines, ont été mises à jour en 2020[12].
Dans la majorité des cas, aucun traitement n'est nécessaire. La prise d'antibiotiques avant les opérations dentaires ou chirurgicales peut être prescrite par le médecin, pour éviter une endocardite (c'est-à-dire une inflammation de l'endocarde, qui est la membrane tapissant l'intérieur du cœur).
Si des douleurs thoraciques, de l'anxiété, ou des crises de panique se manifestent, des bêta-bloquants peuvent être prescrits.
Dans certains cas, rares, la fuite de sang (insuffisance mitrale) peut devenir grave : une opération de la valve mitrale (idéalement par réparation ou plastie, à défaut par remplacement par une valve mitrale artificielle) peut être nécessaire.
Les conseils, pour prévenir les troubles associés au prolapsus mitral, sont :
- d'éviter les excitants cardiaques (caféine) ;
- d'éviter les médicaments qui accélèrent le cœur ;
- de pratiquer un exercice physique régulier et modéré.
Épidémiologie
Environ 2 % de la population seraient touchés[13]. On le lie parfois à certaines affections : maladie de Basedow, rhumatisme articulaire aigu, cardiopathie ischémique, communication interauriculaire, syndrome de Marfan, Syndrome d'Ehlers-Danlos...
Notes et références
- (en) JB Barlow et WA Pocock, « The significance of late systolic murmurs and mid-late systolic clicks », Md State Med J, no 12, , p. 76–7. (PMID 13966713).
- (en) Tamura K, Fukuda Y, Ishizaki M, Masuda Y, Yamanaka N, Ferrans VJ, « Abnormalities in elastic fibers and other connective-tissue components of floppy mitral valve » Am Heart J. 1995;129:1149–1158
- (en) Delling FN, Rong J, Larson MG. et al. « Familial clustering of mitral valve prolapse in the community » Circulation 2015;131:263-268
- (en) Disse S, Abergel E, Berrebi A. et al. « Mapping of a first locus for autosomal dominant myxomatous mitral-valve prolapse to chromosome 16p11.2-p12.1 » Am J Hum Genet. 1999;65:1242–1251
- (en) Freed LA, Acierno JS Jr, Dai D. et al. « A locus for autosomal dominant mitral valve prolapse on chromosome 11p15.4 » Am J Hum Genet. 2003;72:1551–1559
- Roselli C, Yu M, Nauffal V et al. Genome-wide association study reveals novel genetic loci: a new polygenic risk score for mitral valve prolapse, European Heart Journal, 2022;43,668–1680
- (en) Levine RA, Stathogiannis E, Newell JB, Harrigan P, Weyman AE, « Reconsideration of echocardiographic standards for mitral valve prolapse: lack of association between leaflet displacement isolated to the apical four chamber view and independent echocardiographic evidence of abnormality » J Am Coll Cardiol. 1988;11:1010–1019
- (en) Avierinos JF, Detaint D, Messika-Zeitoun D, Mohty D, Enriquez-Sarano M, « Risk, determinants, and outcome implications of progression of mitral regurgitation after diagnosis of mitral valve prolapse in a single community » Am J Cardiol. 2008;101:662–667
- Avierinos JF, Gersh BJ, Melton LJ 3rd., Bailey KR, Shub C, Nishimura RA, Tajik AJ, Enriquez-Sarano M, Natural history of asymptomatic mitral valve prolapse in the community, Circulation, 2002;106:1355–1361
- Miller MA, Dukkipati SR, Turagam M, Liao SL, Adams DH, Reddy VY, Arrhythmic mitral valve prolapse: JACC review topic of the week, J Am Coll Cardiol, 2018;72:2904-2914
- Basso C, Perazzolo Marra M, Rizzo S et al. Arrhythmic mitral valve prolapse and sudden cardiac death, Circulation, 2015;132:556-566
- Otto CM, Nishimura RA, Bonow RO et al. 2020 ACC/AHA guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines, Circulation, 2021;143:e72–e227
- (en) Freed LA, Levy D, Levine RA, Larson MG, Evans JC, Fuller DL, Lehman B, Benjamin EJ, « Prevalence and clinical outcome of mitral-valve prolapse » N Engl J Med. 1999;341:1–7
- Portail de la médecine