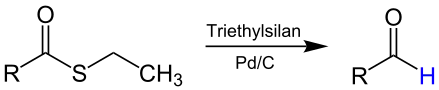
Réduction de Fukuyama
La réduction de Fukuyama est une réaction organique d'oxydoréduction dans laquelle un thioester est réduit en aldéhyde par un hydrure de silyle en présence d'une quantité catalytique de palladium. Cette réaction a été mise au point en 1990 par Tohru Fukuyama[1].
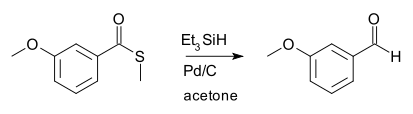
Dans la spécification initiale de la réaction, l'hydrure de silyle était le triéthylsilane (CH2CH3)3SiH et le catalyseur était le palladium sur carbone :
On utilise ces réductions pour la conversion d'acides carboxyliques (comme précurseurs de thioesters) en aldéhydes, procédure considérée comme difficile en raison de la facilité avec laquelle se produit la réduction secondaire en alcool.
Mécanisme
Le mécanisme de réaction de base se présente comme un cycle catalytique :
- Addition oxydante :
- Transmétallation :
- RC(O)–PdII–SR + R3SiH ⟶ RC(O)–PdII–H + R3Si–SR ;
- Élimination réductrice :
- RC(O)–PdII–H ⟶ RC(O)–H + Pd0.
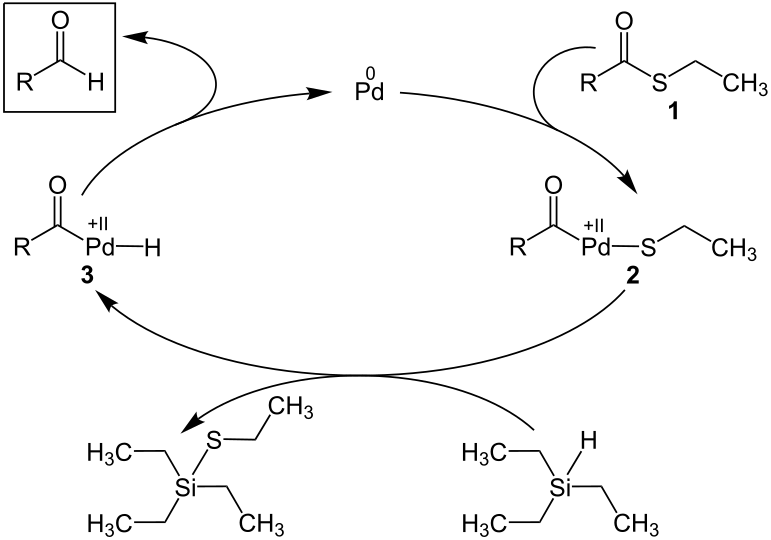 Représentation du cycle catalytique de la réduction de Fukuyama.
Représentation du cycle catalytique de la réduction de Fukuyama.
Applications
Une variation de la réduction de Fukuyama a permis de synthétiser un noyau BODIPY à partir du dérivée SMe-substitué[2] :
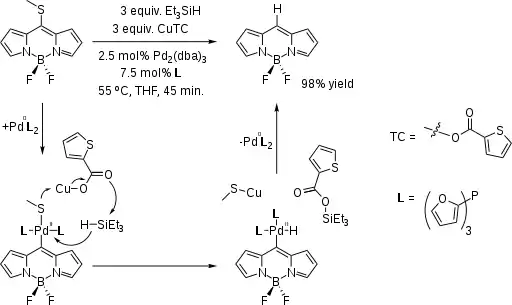
Dans le couplage de Fukuyama, l'hydrure est remplacé par un carbanion nucléophile.
Notes et références
- (en) Tohru Fukuyama, Shao Cheng Lin et Leping Li, « Facile reduction of ethyl thiol esters to aldehydes: application to a total synthesis of (+)-neothramycin A methyl ether », Journal of the American Chemical Society, vol. 112, no 19, , p. 7050-7051 (DOI 10.1021/ja00175a043, lire en ligne)
- (en) Ismael J. Arroyo, Rongrong Hu, Gabriel Merino, Ben Zhong Tang et Eduardo Peña-Cabrera, « The Smallest and One of the Brightest. Efficient Preparation and Optical Description of the Parent Borondipyrromethene System », The Journal of Organic Chemistry, vol. 74, no 15, , p. 5719-5722 (PMID 19572588, DOI 10.1021/jo901014w, lire en ligne)
- Portail de la chimie