Rilpivirine
La rilpivirine (TMC 278) est un médicament antirétroviral. C'est un analogue non-nucléosidique, inhibiteur de la transcriptase inverse (nNRTI) actuellement développé pour le traitement de l'infection par le VIH.
| Rilpivirine | |
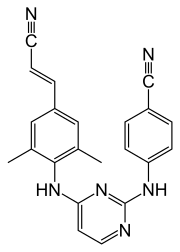
| |
| Identification | |
|---|---|
| Nom UICPA | 4-{[4-({4-[(E)-2-cyanoéthényl]-2,6-diméthylphényl}amino)pyrimidin-2-yl]amino}benzonitrile |
| No CAS | |
| No ECHA | 100.224.394 |
| Code ATC | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C22H18N6 [Isomères] |
| Masse molaire[1] | 366,418 5 ± 0,020 1 g/mol C 72,11 %, H 4,95 %, N 22,94 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
Ce médicament est disponible en France depuis . Rilpivirine seule est vendue sous la marque "Edurant". Quand la rilpivirine est associée au Truvada, le médicament est vendu sous la marque "Eviplera".
Efficacité
L'efficacité antivirale chez les patients naïfs d'antirétroviraux (définie par la proportion de patient ayant une charge virale < 50copies/mL), associée à 2 inhibiteurs mucléosidiques de la RT, est comparable à celle de l'éfavirenz et serait mieux tolérée que cette dernière. Il existe cependant plus d'échecs virologiques dans le bras Rilpivirine (vs. Efavirenz) pour les hautes charges virales initiales (> 100.000 copies/mL) avec apparition de mutations de résistance, dans les essais ECHO et THRIVE[2],[3]
Forme intramusculaire
Sa demi-vie est longue et une forme intramusculaire a été développée, en association avec le cabotégravir, un inhibiteur de l'intégrase. Cette forme, en injection mensuelle, est aussi efficace qu'une trithérapie classique dans le cadre d'un traitement d'entretien[4]. Le délai entre deux injections peut même être prolongé tous les deux mois sans perte d'efficacité[5].
Voir aussi
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Molina J-M, Cahn P, Grinsztejn B, et al, on behalf of the ECHO study group. Rilpivirine versus efavirenz with tenofovir and emtricitabine in treatment-naive adults infected with HIV-1 (ECHO): a phase 3 randomised double-blind active-controlled trial, Lancet, 2011;378:238-246
- Cohen CJ, Andrade-Villanueva J, Clotet B, et al. on behalf of the THRIVE study group. Rilpivirine versus efavirenz with two background nucleoside or nucleotide reverse transcriptase inhibitors in treatment-naive adults infected with HIV-1 (THRIVE): a phase 3, randomised, non-inferiority trial, Lancet, 2011;378:229-237
- Orkin C, Arasteh K, Górgolas Hernández-Mora M et al. Long-acting cabotegravir and rilpivirine after oral induction for HIV-1 infection, N Engl J Med, 2020;382:1124-1135
- Overton ET, Richmond G, Rizzardini G et al. Long-acting cabotegravir and rilpivirine dosed every 2 months in adults with HIV-1 infection (ATLAS-2M), 48-week results: a randomised, multicentre, open-label, phase 3b, non-inferiority study, Lancet, 2020;396,1994-2005
- Portail de la chimie
- Portail de la médecine
- Portail de la virologie
- Portail de la pharmacie