Sclérotinisation
La sclérotinisation, appelée aussi sclérification, est un processus biochimique qui permet de protéger le corps mou d'animaux, principalement les arthropodes (crustacés, insectes). Peu après l'exuviation au cours de laquelle ils quittent leur ancienne cuticule qui se déchire en suivant des lignes de moindre résistance (endroit où la cuticule est moins sclérotinisée), leur nouveau tégument est induré par le tannage de protéines cuticulaires. La sclérotinisation et le brunissement de la cuticule transforme le pâle et mou nouveau tégument en un exosquelette foncé[3] et rigide qui constitue la première barrière contre les pertes en eau, les agressions physiques et chimique du milieu extérieur.


Ce processus est très proche et lié au processus de mélanisation de l'endocuticule qui transforme un tégument blanchâtre en un tégument noir. La biosynthèse des sclérotines, des polymères bruns et des mélanines est en effet assurée par une voie métabolique commune à celle de la dopamine, des catécholamines, de la noradrénaline et de l'adrénaline[4]. Les enzymes de type phénoloxydase (en) (tyrosinases, laccases), décarboxylase, et isomérase interviennent au cours de la sclérotinisation (tannage de protéines tannées par des dérivés quinoniques issus de la tyrosine), du brunissement et de la mélanisation de la cuticule (formation de polymères de tyrosine, respectivement bruns et noirs)[5].
Degré de sclérotinisation
Le degré de sclérotinisation, qui détermine le degré de rigidité, varie en fonction du stade de développement (la cuticule de la larve est flexible avant de se durcir au cours de la nymphose) et des régions du corps, différentes selon les espèces. Les quantités de matière sclérosante incorporées dans les différentes régions exosquelettiques varient de moins de 1 % à plus de 10 % du poids sec cuticulaire. Les quantités de sclérotine incorporées dans les différentes régions de l'exosquelette varient ainsi de moins de 1 % à plus de 10 % du poids sec de la cuticule[6].
Un faible degré de sclérotinisation donne un rôle premier à la chitine qui forme une cuticule résistante mais flexible. Par exemple la cuticule abdominale élastique des insectes hématophages leur permet de se distendre pour s’accommoder au volume des repas de sang[7]. La distension de l'abdomen du criquet pèlerin peut atteindre trois fois sa taille au repos, pour pondre ses œufs profondément dans le sable[8].
Un fort degré de sclérotinisation confère à l'exocuticule une dureté et une résistance importante. Par exemple, les sclérites des scorpions ou les élytres des coléoptères ont des parois fortement sclérifiées. Les pièces buccales de nombreux arthropodes sont des appendices fortement sclérotinisés à caractère masticateur ou préhensile, traduisant une adaptation au régime alimentaire impliquant notamment le broyage de la nourriture[9].
Voie métabolique
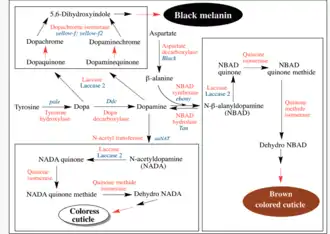
Jusqu'aux années 1950, le durcissement de la cuticule était attribué à une forte chitinisation de celle-ci[11]. Depuis les travaux de Campbell[12] et surtout de Pryor (en) en 1940[13],[14], le nouveau modèle scientifique qui fait consensus fait appel au tannage de protéines cuticulaires, les arthropodines (de), par des quinones tannantes. Le bursicon (en), hormone qui est sécrétée lors de la mue des arthropodes, contrôle le tannage de la cuticule, augmentant la chitinisation de la cuticule alaire (expansion des ailes) et la sclérotinisation de nombreuses parties du corps[15]. Dans ce dernier cas[16], elle provoque, dans l'épiderme, une activation de la tyrosine hydroxylase, qui a pour conséquence d'augmenter la synthèse de la L-DOPA et de la dopamine (composés à structure ortho-diphénolique produits à partir d'un acide aminé aromatique, la tyrosine prélevée par l'épiderme dans l'hémolymphe) puis de la N-acétyldopamine (en) (abrégé en NADA)[17] et de N-beta-alanyldopamine (abrégé en NBAD). L'oxydation de NADA produit des ortho-quinones. Ces dernières subissent différentes isomérisations puis se lient spontanément à des groupes nucléophiles libres[18] de différentes protéines cuticulaires par réticulation. Le tannage de la cuticule est ainsi assuré par ces quinones (tannage quinonique)[19] et des polyphénols qui forment des liaisons covalentes avec les protéines cuticulaires (matrice protéique d'arthropodines associée aux fibrilles de chitine, constituant un complexe glycoprotéique)[20]. Sclérotisées par ces composés tannants, les protéines deviennent des sclérotines imperméables à l'eau, donnant sa dureté à l'exosquelette et le rendant hydrophobe. L'exosquelette est ainsi une protection générique des insectes contre les pertes en eau et contribue à faire d'eux les premiers animaux à être sortis des eaux, alors que la fine cuticule branchiale des crustacés joue un rôle dans l'osmorégulation[21]. Parallèlement, l'oxydation de NBAD produit des quinones impliquées dans la sclérotinisation et le brunissement de la cuticule[22],[23].
Notes et références
- (en) Tony Atkins, Anthony G. Atkins, The Science and Engineering of Cutting. The Mechanics and Processes of Separating, Scratching and Puncturing Biomaterials, Metals and Non-metals, Elsevier Science, , p. 322.
- (en) Malcolm Burrows, Gregory Sutton, « Locusts use a composite of resilin and hard cuticle as an energy store for jumping and kicking », Journal of Experimental Biology, vol. 215, no 19, , p. 3501-3512 (DOI 10.1242/jeb.071993).
- La teinte foncée de la cuticule permet notamment aux insectes poïkilothermes de convertir en chaleur les radiations solaires, chaleur dont ils sont fortement dépendants pour leur activité (fonctionnement des muscles thoraciques alaires pour le vol, recherche de nourriture…).
- (en) Manickam Sugumaran & Hanine Barek, « Critical Analysis of the Melanogenic Pathway in Insects and Higher Animals », Int. J. Mol. Sci., vol. 17, no 10, (DOI 10.3390/ijms17101753).
- (en) S. 0. Andersen, M. G. Peter, P. Roepstorff, « Cuticular Sclerotization in Insects », Comp. Biochem. Physiol, vol. 113B, no 4, , p. 689-705 (DOI 10.1016/0305-0491(95)02089-6).
- (en) Vincent H. Resh, Ring T. Carde, Encyclopedia of Insects, Academic Press, , p. 340.
- plastification induite par une neurohormone qui déclenche une réaction dans les cellules épidermiques responsables d'une diminution des interactions entre les protéines cuticulaires.
- Jeanne Raccaud-Schoeller, Les insectes. Physiologie, développement, Masson, , p. 276.
- (en) Manickam Sugumaran, « Unified Mechanism for Sclerotization of Insect Cuticle », Advances in Insect Physiology, vol. 27, , p. 229-334 (DOI 10.1016/S0065-2806(08)60014-4).
- (en) T.L. Hopkins, K.J. Kramer, « Insect cuticle sclerotization », Annu. Rev. Entomol., vol. 37, , p. 273–302 (DOI 10.1146/annurev.en.37.010192.001421).
- (en) S. C. Pathak, Yadu Nandan Sahai, Recent advances in insect physiology, morphology, and ecology, Today & Tomorrow's Printers and Publishers, , p. 1.
- (en) F. L. Campbell, « The Detection and Estimation of Insect Chitin and the Irrelation of “Chitinization” to Hardness and Pigmentation of the Cuticula of the American Cockroach, Periplaneta Americana », Annals of the Entomological Society of America, vol. 22, no 3, , p. 401–426 (DOI 10.1093/aesa/22.3.401).
- (en) M.G.M. Pryor, « On the hardening of the ootheca of Blatta orientalis », Proceedings of the Royal Society B., vol. 128, no 852, , p. 378–393 (DOI 10.1098/rspb.1940.0017)
- (en) M.G.M. Pryor, « On the hardening of the cuticle of insects », Proceedings of the Royal Society B., vol. 128, no 852, , p. 393–407 (DOI 10.1098/rspb.1940.0018)
- Lauralee Sherwood, Hillar Klandorf, Paul H. Yancey, Physiologie animale, De Boeck supérieur, , p. 280.
- (en) Lawrence I. Gilbert, Insect Endocrinology, Elsevier Science, , p. 98-99.
- (en) Peter Karlson & Constantin E. Sekeris, « N-Acetyl-dopamine as Sclerotizing Agent of the Insect Cuticle », Nature, vol. 195, , p. 183–184 (DOI 10.1038/195183a0).
- résidus d'histidine, de lysine.
- Hypothèse formulée en 1940 par Pryor d'après ses travaux consacrés à la formation de l'oothèque chez la Blatte, et à la formation de la cuticule chez les insectes, ce biologiste inventant le terme de sclérotine en 1945.
- (en) Richard J Suderman, Neal T Dittmer, Michael R Kanost, Karl J Kramer, « Model reactions for insect cuticle sclerotization: cross-linking of recombinant cuticular proteins upon their laccasecatalyzed oxidative conjugation with catechols », Insect Biochemistry and Molecular Biology, vol. 36, no 4, , p. 353-365 (DOI 10.1016/j.ibmb.2006.01.012).
- (en) A.C. Neville, Biology of the Arthropod Cuticle, Springer Science & Business Media, (lire en ligne), p. 126-140
- (en) S.O. Andersen, « Arthropod cuticles: their composition, properties and functions. », Symp. zool. Soc. Lond., no 38, , p. 7-32.
- (en) T.L. Hopkins, T. D. Morgan, Y. Aso, K. J. Kramer, « N-betaalanyldopamine: major role in insect cuticle tanning », Science, no 217, , p. 364-366.