كربونات المغنيسيوم
كربونات المغنيسيوم هو مركب كيميائي له الصيغة MgCO3، ويكون على شكل ملح أبيض اللون لا يذوب في الماء، وله استخدامات عديدة علاجياً وصناعياً وصيدلانياً.
| كربونات المغنيسيوم | |
|---|---|
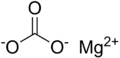 كربونات المغنيسيوم | |
 كربونات المغنيسيوم | |
| أسماء أخرى | |
Magnesite | |
| المعرفات | |
| رقم CAS | 546-93-0 (anhydrous) 13717-00-5 (monohydrate), 5145-48-2 (dihydrate), 14457-83-1 (trihydrate), 61042-72-6 (pentahydrate) |
| بوب كيم (PubChem) | 11029 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | CMgO3 |
| كتلة مولية | 84.31 غ.مول−1 |
| المظهر | white solid استرطاب |
| الرائحة | odorless |
| الكثافة | 2.958 g/cm3 (anhydrous) 2.825 g/cm3 (dihydrate) 1.837 g/cm3 (trihydrate) 1.73 g/cm3 (pentahydrate) |
| نقطة الانصهار | 350 °س، 623 °ك، 662 °ف ( decomposes (anydrous) 165 °م (329 °ف؛ 438 ك) (trihydrate)) |
| الذوبانية في الماء | anhydrous: 0.0106 g/100ml (25 °C) 0.0063 g/100ml (100 °C)[1] pentahydrate: 0.375 g/100ml (20 °C)[بحاجة لمصدر] |
| حاصل الذوبانية، Ksp | 10−7.8[2] |
| الذوبانية | soluble in acid, aqueous ثنائي أكسيد الكربون insoluble in أسيتون، أمونياك |
| معامل الانكسار (nD) | 1.717 (anhydrous) 1.458 (dihydrate) 1.412 (trihydrate) |
| البنية | |
| البنية البلورية | نظام بلوري ثلاثي |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
-1113 kJ/mol[3] |
| إنتروبيا مولية قياسية S |
65.7 J/mol·K[1][3] |
| الحرارة النوعية، C | 75.6 J/mol·K[1] |
| المخاطر | |
| صحيفة بيانات سلامة المادة | ICSC 0969 |
| فهرس المفوضية الأوروبية | Not listed |
| NFPA 704 |
0
1
0
|
| نقطة الوميض | Non-flammable |
| حد التعرض المسموح به U.S | TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp) ْْْْْْْ |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخصائص
مسحوق أبيض ضخم عديم الرائحة، أو كتل خفيفة بيضاء هشة، عديم الانحلال عملياً في الماء، ولا ينحل في الكحول، لكن ينحل في الحموض الممدة مع فوران.
الاستعمالات
- علاجياً: تستعمل كربونات المغنيزيوم كمادة مضادة للحموضة، كما أن لها تأثيراً مسهلاً تناضحياً.
- صناعيا: يدخل في صناعة معاجين الأسنان وأدوات التجميل كالكريمات ويستخدم أيضا كمادة مالئة لتقوية البلاستيك وزيادة صلابته عند التصنيع.[4]
الاستخدام الصيدلاني
يُستعمل كممدد في المضغوطات والمحافظ حيث يُستعمل بشكل رئيسي في مضغوطات الضغط المباشر بتراكيز أعلى من 45% وزن/وزن، كما يُستخدم أيضاً لادمصاص السوائل الداخلة في تركيب المضغوطة كالمطعمات و تُعد كربونات المغنيسيوم غذاءً إضافياً ، أما علاجياً فيُستخدم كمضاد للحموضة.
التأثير على صحة الجسم
-تم تصنيف كربونات المغنيسيوم في فئة المواد غير السامة غير المخرشة لكن كما هو معروف فإن استخدام أملاح المغنيسيوم و منها كربونات المغنيسيوم هو مُضاد استطباب لدى المصابين بقصور كلوي.
-يتفاعل كربونات المغنيسيوم في المعدة مع الحموضة المعديّة مشكلاً ملح كلوريد المغنيزيوم الذوّاب و ثنائي أكسيد الكربون، لذلك لا يُنصح باستخدام كربونات المغنيسيوم كمُضاد للحموضة للأشخاص الذين لا يحتملون حركة غاز ثاني أكسيد الكربون داخل المعدة.
يُمتص جزء من المغنيزيوم و يُطرح عن طريق البول، كما يملك كربونات المغنيزيوم خصائص مليّنة كأملاح المغنيزيوم الأخرى و قد يُحدث إسهالات.
حفظ المادة
يجب أن يحفظ في عبوات محكمة الإغلاق في أماكن جافة و باردة.
اقرأ أيضاً
المراجع
- magnesium carbonate نسخة محفوظة 31 أغسطس 2017 على موقع واي باك مشين.
- Bénézeth, Pascale, et al. "Experimental determination of the solubility product of magnesite at 50 to 200 C." Chemical Geology 286.1 (2011): 21-31.
- Zumdahl, Steven S. (2009)، Chemical Principles 6th Ed.، Houghton Mifflin Company، ص. A22، ISBN 0-618-94690-X.
- استفسارات - بيوتات الكيمياء التعليمية. نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين.
- بوابة الكيمياء
- بوابة صيدلة
- بوابة جمباز
