Células CHO
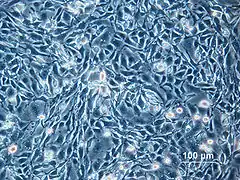
Las células CHO (del inglés Chinese hamster ovary) son células derivadas de ovario de hámster chino (Cricetulus griseus) y cuyo uso está ampliamente extendido en el campo de la biotecnología como cultivos celulares para la expresión y producción de proteínas recombinantes.
Origen
Los hámsteres chinos se usaron por primera vez como animales de laboratorio en 1919, en sustitución de ratones en la investigación de los neumococos. Los esfuerzos del Dr. George Yerganian y otros colegas para domesticar a estos hámsteres a mediados del siglo XX trajo consigo que durante su cría en cautiverio muchos individuos desarrollasen enfermedades degenerativas, debido al estrecho parentesco de los animales que se cruzaban. No obstante, la aparición de tales enfermedades degenerativas aumentó el interés en el estudio de su genética.
Durante este tiempo los investigadores se dieron cuenta de que el bajo número de cromosomas en los hámsteres chinos (2n=22) los convertía en modelos ideales para el estudio de radiaciones citogenéticas y cultivos celulares. En 1957, durante una investigación sobre la utilidad de varias líneas celulares en el campo de la genética de células somáticas, el Dr. Theodore T. Puck, del departamento de medicina de la Universidad de Colorado, aisló un ovario de una hembra de hámster chino y estableció una nueva línea celular.[1][2] Pronto se pudo ver, que estas células eran bastante resistentes y muy aptas para el cultivo in vitro, y su tiempo de generación era muy rápido. Además, la heterogenidad cariotípica de estas poblaciones celulares las convirtió en un candidato ideal para el estudio de anomalías cromosomáticas.
Uso en biotecnología
La primera proteína terapéutica recombinante producida en células mamíferas, el activador tisular del plasminógeno que fue sintetizado usando células CHO, fue aprobado para el uso clínico en 1987. Esto marcó el principio de una nueva era en la producción de proteínas recombinantes y cuyo éxito está basado en el uso de las células CHO para su expresión.
En la actualidad las células CHO son la mejor alternativa a otros sistemas de expresión establecidos como es el caso de líneas celulares derivadas de insectos (Sf9 y Sf21 de Spodoptera frugiperda, Schneider 2 de Drosophila melanogaster, «High Five» de Trichoplusia ni...), bacterias (E. coli, B. subtilis...), levaduras (S. cerevisiae, P. pastoris, H. polymorpha...), entre otros, para la producción de proteínas recombinantes de uso terapéutico con patrones de N-glicosilación similares a los humanos, pues las estructuras de oligosacáridos pueden variar de manera muy significativa en los diferentes sistemas de expresión o incluso carecer de ellas, como es el caso de las bacterias.[3] El patrón de glicosilación en una proteína terapéutica determina su funcionalidad, rechazo o el periodo de vida en el torrente sanguíneo.
También se usan para análisis de toxicidad y de requerimientos nutricionales.
Listado de productos recombinantes
| Nombre comercial | Principio activo | Proteína recombinante | Uso terapéutico | Compañía | Año de autorización por la FDA |
|---|---|---|---|---|---|
| Vectibix | Panitumumab | Anti-EGFR (anticuerpo) | Cáncer metastásico colorrectal | Amgen | 2006 |
| Myozyme | Alglucosidasa alfa | α-glucosidasa | Enfermedad de Pompe | Genzyme | 2006 |
| Aldurazyme | Laronidasa | Laronidasa | Mucopolisacaridosis I | Genzyme | 2006 |
| Orencia | Abatacept | lgG-CTLA fusión | Artritis reumatoide | Bristol-Myers Squibb | 2005 |
| Naglazyme | Galsulfasa | N-acetilgalactosamina-4-sulfatasa | Mucopolisacaridosis VI | BioMarin Pharmaceutical | 2005 |
| Luveris | r-hLH | Hormona luteinizante | Infertilidad | Serono | 2004 |
| Avastin | Bevacizumab | Anti-VEGF (anticuerpo) | Cáncer metastásico colorrectal y cáncer de pulmón | Genentech | 2004 |
| Advate | Octocog alfa | Factor VIII (modificada) | Hemofilia A | Baxter | 2003 |
| Xolair | Omalizumab | Anti-IgE (anticuerpo) | Asma moderado/severo | Genentech | 2003 |
| Raptiva | Efalizumab | Anti-DC11a (anticuerpo) | Psoriasis crónica | Genentech | 2003 |
| Fabrazyme | Agalsidasa beta | α-galactosidasa | Enfermedad de Fabry | Genzyme | 2003 |
| Rebif | Interferón β-1a | Interferón-β | Esclerosis múltiple remitente | Serono | 2002 |
| Humira | Adalimumab | Anti-TNFα (anticuerpo) | Artritis reumatoide | Abbot | 2002 |
| Aranesp | Darbepoetina | Erythropoietin (modificada) | Anemia | Amgen | 2001 |
| Campath | Alemtuzumab | Anti-CD52 (anticuerpo) | Leucemia linfocítica crónica | Genzyme, Bayer | 2001 |
| ReFacto | Moroctocog alfa | Factor VIII (modificada) | Hemofilia A | Wyeth | 2000 |
| Metalyse | Tenecteplasa | Activador tisular del plasminógeno (modificada) | Infarto agudo de miocardio | Genentech | 2000 |
| Herceptin | Trastuzumab | Anti-HER2 (anticuerpo) | Cáncer de pecho metastásico | Genentech | 1998 |
| Enbrel | Etanercept | TNFα receptor fusión | Artritis reumatoide | Amgen, Wyeth | 1998 |
| Benefix | Nonacog alfa | Factor IX | Hemofilia B | Wyeth | 1997 |
| Follistim/Gonal-F | Folitropina alfa | Hormona foliculoestimulante | Infertilidad | Serono/ NV Organon | 1997 |
| Rituxan | Rituximab | Anti-CD20 (anticuerpo) | Linfoma no-Hodgkin | Genentech, Biogen Idec | 1997 |
| Avonex | Interferón β-1a | Interferón-β | Esclerosis múltiple remitente | Biogen Idec | 1996 |
| Cerezyme | Imiglucerasa | β-glucocerebrosidasa | Enfermedad de Gaucher | Genzyme | 1994 |
| Pulmozyme | Dornasa alfa | Deoxyribonucleasa I | Fibrosis quística | Genentech | 1993 |
| Epogen/Pocrit | EPO | Erythropoietina | Anemia | Amgen/Ortho Biotech | 1989 |
| Activase | Alteplasa | Activador tisular del plasminógeno | Infarto agudo de miocardio | Genentech | 1987 |
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Células CHO.
Wikimedia Commons alberga una categoría multimedia sobre Células CHO.- Chinese Hamster Genome Database (en inglés).
- Entrada de Cellosaurus para CHO
- Entrada de Cellosaurus para CHO-K1
Referencias
- H. J. Tjio, T. T. Puck (1958): Genetics of somatic mammalian cells. II. chromosomal constitution of cells in tissue culture. In: J. Exp. Med. 108(2):259-271. PMID 13563760 doi 10.1084/jem.108.2.259
- T. T. Puck, S. J. Cieciura, A. Robinson (1958): Genetics of somatic mammalian cells. III. Long-term cultivation of euploid cells from human and animal subjects. In: J. Exp. Med. 108(6):945-956. PMID 13598821 doi 10.1084/jem.108.6.945
- Betenbaugh, M. J., Tomiya, N., Narang, S., Hsu, J. T., Lee, Y. C., Biosynthesis of human-type N-glycans in heterologous systems.In: Curr Opin Struct Biol 2004, 14, 601-606.Pubmed
- K.P. Jayapal, K.F. Wlaschin, M.G.S. Yap, W-S. Hu (2007): Recombinant protein therapeutics from CHO cells - 20 years and counting. In: Chem. Eng. Prog. 103(7):40-47. PDF