Clorato de sodio
El clorato de sodio (NaClO3) es un compuesto químico que en forma pura se encuentra como polvo cristalino blanco. Es fácilmente soluble en agua y posee la característica de ser higroscópico. Su descomposición, la cual se produce por encima de los 250 °C, libera oxígeno y deja un residuo de cloruro de sodio.
| Clorato de sodio | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Clorato de sodio | ||
| General | ||
| Otros nombres | Clorato sódico, clorato (V) de sodio | |
| Fórmula estructural |
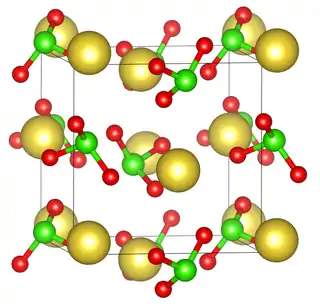
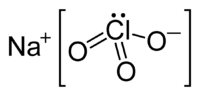 Estructura en Jmol | |
| Fórmula molecular | NaClO3 | |
| Identificadores | ||
| Número CAS | 7775-09-9[1] | |
| Número RTECS | FO0525000 | |
| ChemSpider | 22895 | |
| PubChem | 24487 | |
| UNII | T95DR77GMR | |
| KEGG | C18765 | |
| Propiedades físicas | ||
| Apariencia | polvo cristalino blanco, incoloro | |
| Densidad | 2500 kg/m³; 2,5 g/cm³ | |
| Masa molar | 10 644 g/mol | |
| Punto de fusión | 521,15 K (248 °C) | |
| Punto de descomposición | 573 K (300 °C) | |
| Índice de refracción (nD) | 1.572 | |
| Propiedades químicas | ||
| Solubilidad en agua | 101.0 g/100 ml (20 °C) | |
| Peligrosidad | ||
| NFPA 704 |
0
1
2
OX
| |
| Frases R | R9 R22 R51/53 | |
| Frases S | (S2) S13 S17 S46 S61 | |
| Riesgos | ||
| Ingestión | Dolor abdominal, diarrea, dificultad para respirar, vómito. Enjuagar la boca, atención médica. | |
| Inhalación | Tos, dolor de garganta, azulado de piel, labios, uñas; confusión, convulsiones, mareo, dolor de cabeza, náuseas, inconsciencia. Dar aire fresco, descanso, atención médica. | |
| Piel | Enrojecimiento. Enjuagar con abundante agua, remover ropas contaminadas y enjuagar de nuevo, atención médica. | |
| Ojos | Enrojecimiento, dolor. Enjuagar con abundante agua por varios minutos, atención médica. | |
| LD50 | 1200 mg/kg (ratas, oral)[2] | |
| Compuestos relacionados | ||
| otros aniones |
cloruro de sodio hipoclorito de sodio clorito de sodio perclorato de sodio | |
| otros cationes |
clorato de amonio clorato de litio clorato de potasio clorato de cesio | |
| ácido generador | ácido clórico | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Síntesis
Industrialmente, el clorato de sodio se sintetiza a partir de la electrólisis de una disolución caliente de cloruro de sodio, ocurriendo la siguiente reacción química:
- NaCl + 3H2O → NaClO3 + 3H2
Otra forma de sintetizarse es hacer pasar cloro gaseoso a través de una disolución caliente de hidróxido de sodio, en donde luego se purifica mediante cristalización.
Usos
Su principal uso comercial es el dióxido de cloro (ClO2). Su mayor aplicación es en el blanqueado de pulpa, donde el dióxido de cloro es actualmente el agente blanqueador de ropa predominante.
Herbicidas
El clorato de sodio es usado como un herbicida no selectivo. Se considera fitotóxico para todas las partes verdes de las plantas aunque también causa toxicidad al ser absorbido a través de las raíces.
El clorato de sodio puede utilizarse para controlar diversas especies:
Este herbicida se usa principalmente en tierra no cultivable para el tratamiento del lugar y para la eliminación total de la vegetación en áreas que incluyen bordes de carreteras, mallas o zanjas.
También se utiliza como defoliante y desecante para:
- Algodón
- Arroz
- Cártamo
- Caupí
- Frijoles secos
- Girasoles
- Lino
- Maíz
- Pimientos
- Granos de sorgo
- Granos de soja
Si se usa en combinación con atrazina, se incrementa la persistencia del efecto. Si se usa en combinación con 2,4-D, mejora el rendimiento del material. El clorato de sodio tiene un efecto esterilizante del suelo. La mezcla con otros herbicidas en disolución acuosa es posible siempre que no sean susceptibles a la oxidación.
Generación química de oxígeno
Los sistemas de oxígeno de emergencia, por ejemplo en vuelos comerciales, proveen oxígeno a los pasajeros para protegerlos de caídas de presión en la cabina mediante la descomposición catalítica del clorato de sodio a alta temperatura. Habitualmente, el catalizador contiene polvo de hierro. El peróxido de bario (BaO2) se usa para absorber el cloro, que es un producto menor en esa descomposición.[3]
- 2 NaClO3 → 2 NaCl + 3 O2
El polvo de hierro se mezcla con el clorato de sodio y hace ignición mediante una carga que se activa al jalar la máscara de emergencia. La reacción produce más oxígeno del que se requiere para la combustión. De forma similar, el sistema de soldadura «Solidox» utiliza perdigones de clorato de sodio mezclados con fibras de combustible para generar oxígeno.
Toxicidad en humanos
Debido a su naturaleza oxidante, el clorato de sodio puede ser muy tóxico en caso de ser ingerido. El clorato de sodio, actúa en la hemoglobina llevando a la formación de metahemoglobina, que es seguida por la desnaturalización de la proteína globina y una reticulación de las proteínas de las membranas de los eritrocitos, dañando las enzimas de la misma y aumentando, por tanto su permeabilidad, resultando en una hemólisis severa. La desnaturalización de la hemoglobina excede la capacidad de la ruta metabólica de la Glucosa-6-fosfato deshidrogenasa (G6PD). Además, esta enzima se desnaturaliza directamente con el clorato reduciendo su actividad.
La terapia con ácido ascórbico y azul de metileno se usa con frecuencia en el tratamiento de la metahemoglobinemia. Sin embargo, debido a que el azul de metileno requiere la presencia de NADPH que depende del funcionamiento normal del sistema G6PD, es menos efectivo que en otras condiciones caracterizadas por la oxidación de la hemoglobina.
Provoca hemólisis aguda con fallos multiorgánicos, incluyendo CID e insuficiencia renal. Existe además una toxicidad directa al túbulo proximal renal.[4] El tratamiento consistirá en transfusión de intercambio, diálisis peritoneal o hemodiálisis.[5]
Formas de presentación
El clorato de sodio puede presentarse en forma de polvo, spray o gránulos. Existe riesgo de ignición y explosión en mezclas secas con otras sustancias, especialmente con materiales orgánicos como otros herbicidas o el azúcar, además de azufre, fósforo, metales en polvo y ácidos fuertes. No debe ser almacenado en viviendas para evitar mezclas accidentales con alguna de las sustancias mencionadas anteriormente.[6]
Las formulaciones en el mercado contienen un retardador de fuego cuyo efecto es pequeño si se enciende deliberadamente. La mayoría de los herbicidas de clorato disponibles comercialmente contienen aproximadamente 53% de clorato de sodio y un depresor de fuego, como el metaborato de sodio o el fosfato de amonio.
Nombres comerciales
El ingrediente activo clorato de sodio se encuentra en una variedad de herbicidas comerciales: Atlacide, Defol, De-Fol-Ate, Drop-Leaf, Fall, Harvest-Aid, Kusatol, Leafex y Tumbleaf. El compuesto puede ser usado en combinación con otros herbicidas tales como la atrazina, 2,4-D, bromacil, diuron y metaborato de sodio.
El clorato de sodio fue un herbicida ampliamente usado en Estados Unidos hasta 2009, cuando se retiró su autorización. El clorato de sodio tiene uso en otras aplicaciones, como por ejemplo en la producción de biocidas de dióxido de cloro y para blanqueado de pulpa y papel.
Referencias culturales e históricas
El historiador James Watson de la Universidad Massey en Nueva Zelanda escribió un artículo muy difundido, The Significance of Mr. Richard Buckley's Exploding Trousers (El significado de los pantalones explosivos del Sr. Richard Buckley),[7][8] sobre accidentes con clorato de sodio cuando se usaba como herbicida para controlar la Senecio jacobaea en la década de 1930.[9] Esto ganó después un Premio Ig Nobel de Historia de la Agricultura en el 2005[10] y fue la base para el episodio "Pantalones explosivos" de la cuarta temporada del programa MythBusters en mayo de 2006.
En Estados Unidos, desde septiembre del 2009, se prohibió la venta al por mayor del herbicida clorato de sodio, aunque se permitió utilizar y almacenar el producto hasta el 10 de mayo del 2010.
Referencias
- Número CAS
- Merck MSDS (PDF, inglés)
- Yunchang Zhang, Girish Kshirsagar, and James C. Cannon (1993). «Functions of Barium Peroxide in Sodium Chlorate Chemical Oxygen». Ind. Eng. Chem. Res. 32 (5): 966-969. doi:10.1021/ie00017a028.
- Oliver J.; MacDowell M., Tracy A (1951). «The pathogenesis of acute renal failure associated with traumatic and toxic injury. Renal ischemia, nephrotoxic damage and the ischemuric episode.». J Clin Invest 30 (12): 1307-439. PMC 441312. PMID 14897900. doi:10.1172/JCI102550.
- Goldfrank's Toxicologic Emergencies, McGraw-Hill Professional; 8th edition (March 28, 2006), ISBN 978-0-07-143763-9
- Beveridge, Alexander (1998). Forensic Investigation of Explosions. Taylor & Francis Ltd. ISBN 0-7484-0565-8.
- "The Significance of Mr. Richard Buckley's Exploding Trousers: Reflections on an Aspect of Technological Change in New Zealand Dairy Farming between the World Wars" Archivado el 23 de octubre de 2013 en Wayback Machine., Agricultural History magazine
- "Histories: Farmer Buckley's exploding trousers", New Scientist
- "Trousers Explode, Evening Post, 21 de abril de 1933.
- James Watson for "The Significance of Mr. Richard Buckley’s Exploding Trousers.", improbable.com
Lectura adicional
- "Chlorate de potassium. Chlorate de sodium", Fiche toxicol. n° 217, Paris: Institut national de recherche et de sécurité, 2000. 4pp.
Enlaces externos
- Ficha de seguridad INSHT (PDF)
- Ficha de seguridad CDC (en inglés)
- Ficha de seguridad INCHEM (en inglés)
