Dialilcianamida
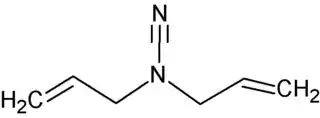
La dialilcianamida, conocida también como di-2-propenilcianamida y N-cianodialilamina,[2][3] es un compuesto orgánico de fórmula molecular C7H10N. Su estructura corresponde a la de la cianamida, si bien el nitrógeno, además estar de estar unido al grupo carbonitrilo (-C≡N), está enlazado a dos grupos alilo. Asimismo, es semejante a la de la dialilamina, pero, a diferencia de ésta, un grupo carbonitrilo está unido al nitrógeno central.
| Dialilcianamida | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| bis(prop-2-enil)cianamida | ||
| General | ||
| Otros nombres |
di-2-propenilcianamida N-cianodialilamina | |
| Fórmula semidesarrollada | CH2=CH-CH2-N(C≡N)-CH2-CH=CH2 | |
| Fórmula molecular | C7H10N | |
| Identificadores | ||
| Número CAS | 538-08-9[1] | |
| ChemSpider | 10392 | |
| PubChem | 10849 | |
| UNII | 0Y2M1X8LXA | |
|
C=CCN(CC=C)C#N
| ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Densidad | 902 kg/m³; 0,902 g/cm³ | |
| Masa molar | 12 217 g/mol | |
| Punto de fusión | 0 °C (273 K) | |
| Punto de ebullición | 222 °C (495 K) | |
| Presión de vapor | 0,1 ± 0,5 mmHg | |
| Índice de refracción (nD) | 1,469 | |
| Propiedades químicas | ||
| Solubilidad en agua | 5 g/L | |
| log P | 1,64 | |
| Familia | Nitrilo, amina | |
| Peligrosidad | ||
| Punto de inflamabilidad | 363,15 K (90 °C) | |
| Compuestos relacionados | ||
| nitrilos | dimetilaminoacetonitrilo | |
| dinitrilos | (dimetilaminometilen)malononitrilo | |
| polinitrilos |
tricianoaminopropeno nitrilotriacetonitrilo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Propiedades físicas y químicas
A temperatura ambiente, la dialicianamida es un líquido incoloro con una densidad inferior a la del agua (0,902 g/cm³). Tiene su punto de fusión a 0 °C, mientras que su punto de ebullición es de 222 °C.[4] En forma de vapor, su densidad es 4,1 veces mayor que la del aire.[3]
Es prácticamente insoluble en agua —apenas 5 g/L— pero es soluble en los disolventes orgánicos habituales como alcohol, éter, acetona y benceno.[3] El valor del logaritmo de su coeficiente de reparto, logP = 1,64, implica una solubilidad mayor en disolventes polares como el agua que en disolventes apolares como el 1-octanol.[5][2] Asimismo, puede descomponerse si es expuesta a la humedad.[6]
Síntesis y usos
La dialilcianamida puede sintetizar a partir de un haluro de alilo y una sal de cianamida, preferiblemente una sal de un metal alcalino como dicianamida de sodio. Esta síntesis, que data de 1928, se lleva a cabo en un disolvente formado por agua y un compuesto orgánico souble en ésta, por ejemplo etanol.[7] También se puede preparar la dialilcianamida a partir de la reacción entre un haluro insaturado con tres átomos de carbono (cloruro de alilo), una cianamida alcalino-térrea y un hidróxido alcalino fuerte. Como catalizador se emplea una sal de cobre como sulfato o sulfito de cobre (II), aunque también pueden usarse sales de cobre (I).[8]
Un método de síntesis más moderno utiliza como precursores cianamida y carbonato de aliletilo, siendo el catalizador paladio(0). Con este procedimiento se alcanza un rendimiento del 86%.[9]
En cuanto a sus usos, la dialilcianamida se emplea en la elaboración de copolímeros que contienen entre un 1% a un 75% de dialilcianamida, además de otro compuesto diferente copolimerizable con ésta y que contiene uno o varios grupos CH2=C. Estos materiales exhiben propiedades que los hacen especialmente adecuados para la industria.[4] Otro uso de la dialilcinamida es en condensadores electrolíticos, en concreto como relleno para condensadores electrolíticos de tántalo para alta tensión y elevada temperatura.[10]
La dialilcianamida también puede utilizarse como agente «secuestrador» o «captador» de dióxido de carbono y sulfuro de hidrógeno en operaciones subterráneas. Ambos compuestos aparecen habitualmente en la producción de petróleo y gas, siendo corrosivos en dicho entorno, lo que en última instancia acaba provocando el agrietamiento u obstrucción de los equipos de producción. La dialilcianamida, introducida por medio de un fluido de tratamiento, reduce la corrosión ocasionada por estos agentes.[11]
Precauciones
La dialilcianamida es una sustancia combustible cuyo punto de inflamabilidad es 90 °C (valor estimado).[2] En contacto con ácidos o bases, o si se calienta, desprende humos de cianuro venenosos.[3] La dialilcianamida es irritante y resulta nociva por ingestión, inhalación o absorción cutánea.[6] Es considerada más tóxica que la cianamida, provocando ataxia y convulsiones a dosis letales.[3]
Véase también
Los siguientes nitrilos son isómeros de la dialilcianamida:
- Heptanodinitrilo
- Tert-butilmalononitrilo
Referencias
- Número CAS
- Diallylcyanamide (ChemSpider)
- Diallylcyanamide (PubChem)
- Diallyl cyanamide copolymer compositions (1951). Drechsel, Erhart K.; Padbury, John J. Patente US2550652 A.
- Diallylcyanamide (EPA)
- Diallylcyanamide (HazMap)
- Diallylcyanamide (1928). Elmer B. Vliet. Patente US1659793 A.
- Preparation of unsaturated cyanamides (1958). Angelo J. Speziale. Patente US 2858338 A.
- Sílvia Cerezo, Jordi Cortés, Marcial Moreno-Mañas, Roser Pleixats, Anna Roglans (1998). «Cyanomethylamines and azidomethylamines: new general methods of the synthesis and transformations». Tetrahedron Letters 54 (49): 14869-14884. Consultado el 6 de abril de 2017.
- Electrolytic capacitor (1961). Cronquist Norman W.; Donald Mohler. Patente US2973465 A
- CYANAMIDE-BASED CARBON DIOXIDE AND/OR HYDROGEN SULFIDE SCAVENGERS AND METHODS OF USE IN SUBTERRANEAN OPERATIONS (2016). Salla, R. et al. Patente 20160237335