Distrofia miotónica de Steinert
La distrofia miotónica (DM), también conocida como distrofia miotónica tipo 1, DM1, es una enfermedad hereditaria autosómica dominante, multisistémica crónica, de progresión lenta y de heredabilidad altamente variable que se puede manifestar en cualquier momento de la vida desde el nacimiento a la vejez; tanto en hombres como en mujeres. Se caracteriza por una reducción de la masa muscular (distrofia muscular), cataratas posteriores subcapsulares iridiscentes (opacidad del cristalino) defectos en la conducción del impulso cardíaco, cambios endocrinos y miotonía (dificultad para relajar un músculo). Es muy curioso que la edad de aparición, que es altamente variable, desciende con las sucesivas generaciones. Así pues la enfermedad muestra una edad de aparición cada vez menor, un fenómeno denominado anticipación. También hay dos clasificaciones de la distrofia miotónica, teniendo cada una de ellas diferentes síntomas asociados.
| Distrofia miotónica de Steinert | ||
|---|---|---|
 Paciente de 40 años de edad con distrofia miotónica presentando cataratas bilaterales y bloqueo cardíaco. | ||
| Especialidad | neurología | |
| Síntomas | Pérdida muscular , debilidad, músculos que se contraen y no pueden relajarse. | |
| Sinónimos | ||
| Distrofia miotónica de tipo 1, Enfermedad de Curschmann-Steinert | ||
Clasificación
La distrofia miotónica es la forma más común de aparición en el adulto de distrofia muscular y la segunda forma más habitual de enfermedad del músculo esquelético tras la Distrofia muscular de Duchenne. Actualmente se conocen dos tipos de distrofia miotónica de comienzo en la edad adulta: La distrofia miotónica tipo 1 (DM1), la conocida propiamente como enfermedad de Steinert, y la distrofia miotónica tipo 2 (DM2), denominada comúnmente como PROMM, o miopatía proximal miotónica. Ambas son identificables mediante análisis de ADN. La distrofia miotónica1 también tiene una forma congénita que puede afectar gravemente a bebés y tiene una forma de aparición en la infancia. Los investigadores sospechan que existen más formas de distrofia miotónica (DM3, DM4, DMX).
Diferencias entre distrofia miotónica 1 y distrofia miotónica 2
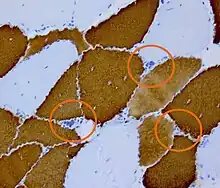
Aunque ambas enfermedades se consideran como afecciones degenerativas de desarrollo lento, la distrofia miotónica tipo 2 es generalmente más leve que la distrofia miotónica tipo 1. La forma congénita grave que afecta a los bebes en la DM1 no se ha encontrado en la DM2 y la literatura médica raramente publica apariciones juveniles de esta forma. La expansión de los trinucleótidos del distrofia miotónica2 es considerablemente más larga en la distrofia miotónica 2 que en distrofia miotónica 1, variando de 75 a más de 11 000 repeticiones. A diferencia de la diatrofia miotónica 1, el tamaño de las expansiones del trinucleótico en el ADN no parecen marcar ninguna diferencia en la edad de aparición o en la severidad de la enfermedad en la distrofia miotónica2. Parece que es menos significativo en el tipo 2 y las revisiones más habituales solo refieren que producen una ligera anticipación en este último caso.
Epidemiología
Es la distrofia muscular más frecuente en el adulto. Su prevalencia se estima en 1/20000 habitantes.[1] En la región canadiense de Saguenay-Lac-Saint-Jean estas cifras se elevan a 1/530 habitantes, siendo todos los afectados descendientes de una misma pareja de emigrados a Canadá en el S. XVII[2]
Etiología

La distrofia miotónica es una enfermedad de transmisión genética donde está involucrado un patrón de dominancia autosómica, significando que hay un gen mutante de uno de los padres que resultará en esta condición. Hay un 50% de probabilidad de recibir distrofia miotónica del progenitor afectado. En la distrofia miotónica tipo 1, el gen afectado es el DMPK (proteína quinasa de distrofia miotónica, que codifica la kinasa miosina), expresada en los músculos esqueléticos. Este gen se localiza en el brazo largo del cromosoma 19. La DM2 es similarmente causada por un defecto del gen ZNF9 en el cromosoma 3 q21.
La DM está incluida dentro de las enfermedades por expansión de trinucleótidos. Ciertas áreas del ADN tienen secuencias repetidas de dos o tres nucleótidos. En DM1, hay una repetición del triplete citosina - timina - guanina (CTG) en el gen DMPK. El número de repeticiones varía grandemente de persona a persona, pero en promedio en un sujeto sano es entre 5 y 37. A veces cuando las secuencias repetitivas de ADN se replican en la división celular, la maquinaria celular agrega una copia extra de la repetición triple a la secuencia. Así hay 37 repeticiones triples en el gen DMPK, la secuencia comienza a ser inestable y los deslizamientos son más probables. La población afectada de DM1 tienen entre 50 y 2000 repeticiones.
El resultado de esto es que el tamaño de repetición de un individuo con DM1 se hará cada vez más grande a medida que envejece. Así se explica el fenómeno de anticipación, así cada niño de un afectado adulto tendrá mayor expansión que su progenitor debido a deslizamientos durante la gametogénesis.
Los individuos con expansiones más grandes tienen enfermedad de inicio más precoz y síntomas más severos en la DM1. La expansión de repeticiones para DM2 es mucho mayor que en DM1, va de 75 a más de 11 000 repeticiones, sin embargo, a diferencia de lo que ocurre en la DM1, el tamaño de la expansión influye muy poco en la edad de aparición y severidad de la enfermedad. La anticipación del mal en generaciones sucesivas es también poco significativa en la DM2.
Cuadro clínico
Las personas afectadas tienen una típica "cara en forma de hacha" producto de atrofia de los músculos temporales, masetero, y faciales.
Los hombres suelen presentar alopecia frontal. Los músculos del cuello y distales de los miembros se afectan de manera temprana. Hay debilidad de los extensores de la muñeca, los dedos y músculos intrínsecos de la mano. Los músculos que permiten la dorsiflexión del tobillo están afectados provocando una caída del pie. Los músculos proximales suelen estar conservados, aunque muchos pacientes tienen afectación del cuádriceps. Hay afectación de músculos del paladar, faríngeos y linguales que pueden provocar disartria, voz nasal y problemas en la deglución. Muchos pacientes tienen debilidad de los músculos respiratorios, provocándoles una insuficiencia respiratoria.
La miotonía puede evidenciarse a partir de los 5 años de edad, pidiéndole al paciente que cierre la mano con fuerza, y luego la relaje, lo cual se produce de manera lenta.
Las manifestaciones cardíacas son comunes, fundamentalmente bloqueos AV de primer grado, entre otros trastornos eléctricos y prolapso mitral. Bloqueos completos pueden ocurrir ocasionando muerte súbita del enfermo.
Diagnóstico
El diagnóstico de la DM1 suele producirse con facultativos con formación especializada en neurología y enfermedades neuromusculares del adulto. Sin la adecuada especialización y recursos médicos experimentados, es común que los pacientes acaben sin diagnóstico o con un diagnóstico erróneo.
Aunque actualmente no existe cura para la DM y el tratamiento se basa en el alivio sintomático, se necesita en todo caso un diagnóstico preciso porque se pueden desarrollar otros problemas con el tiempo. Incluso los pacientes menos afectados pueden ser sometidos a chequeos rutinarios para complicaciones potencialmente fatales (p.ej. problemas con la conducción cardíaca, resistencia a la insulina, cataratas). Además el consejo genético debería estar disponible para todos los pacientes por el alto riesgo de transmisión.
Tratamiento
El tratamiento con quinina y procainamida pueden empeorar la conducción cardíaca, por lo que se recomienda sustituirlos por fenitoína. La colocación de un marcapasos debe ser considerada en enfermos que experimenten síncopes, o anormalidades severas de la conducción. Para la realización de una intervención quirúrgica en el paciente con distrofia miotónica, se da prioridad a las técnicas de anestesia locoregional, siempre que sea posible.[3][4]
Referencias
- «Prevalencia de la enfermedad de steinert en La Presse Médicale, Vol 36 - N° 6-C2 - Junio 2007». Archivado desde el original el 13 de abril de 2008. Consultado el 20 de enero de 2008.
- Mathieu J, De Braekeleer M, Prevost C. Genealogical reconstruction of myotonic dystrophy in the Saguenay-Lac-Saint-Jean area (Quebec, Canada). Neurology 1990;40:839-84
- Distrofia miotónica de Steinert (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- «Manejo anestésico de la Distrofia miotónica de Steinert». Archivado desde el original el 22 de abril de 2012. Consultado el 17 de marzo de 2012.
- «Distrofia miotónica de Steinert y Curschmann» (1960). Amalio R.Telenti, Anales de la Academia Médico-Quirúrgica Asturiana, II, p. 14