Compuesto organometálico
Un compuesto organometalico es un compuesto en el que los átomos de carbono de un ligando orgánico forman enlaces covalentes con un átomo metálico. Los compuestos basados en cadenas y anillos de átomos de carbono se llaman orgánicos, y este es el fundamento del nombre organometálicos. La característica de estos compuestos es la presencia de enlaces entre átomos de metal y de carbono (que pueden ser sencillos, dobles o triples) y por tanto no se consideran organometálicos aquellos compuestos en que un metal se une a una molécula o fragmento por un átomo distinto del carbono, como ocurre en algunos compuestos de coordinación. Este grupo incluye un elevado número de compuestos y algunos químicos lo consideran un grupo distinto al de los compuestos orgánicos e inorgánicos.

Formalmente, los compuestos organometálicos son aquellos que poseen, de forma directa, enlaces entre átomos de metal (o metaloides) y átomos de carbono, M+δ–C-δ, de mayor o menor polaridad.[1] Es decir, un compuesto es considerado como organometálico si este contiene al menos un enlace carbono-metal. En este contexto el sufijo “metálico” es interpretado ampliamente para incluir tanto a algunos no metales (como el fósforo) y metaloides tales como B, Si y As así como a metales verdaderos. Esto es debido a que en muchos casos la química de los elementos B, Si, P y As se asemeja a la química de los metales homólogos respectivos. Por lo tanto, el término de compuestos organometálicos es también usado ocasionalmente para incluir dentro a los ya mencionados no metales y semimetales. En todos los casos se trata de elementos menos electronegativos que el carbono.
Cl2.png.webp)
Tipo de enlace y estabilidad de los compuestos organometálicos
Además del enlace metal-carbono, el metal puede estar unido a otros ligandos formando unidades metal-ligando. El tipo de enlace fundamental entre el carbono y el metal es de tipo covalente, pero también existen compuestos con enlace de dos centros y dos electrones. Además, en los compuestos organometálicos con metales de transición es importante considerar la regla de los 18 electrones.
Hasta 1940 no se pudieron sintetizar muchos organometálicos por lo que se suponía que el enlace carbono-metal era poco estable. En realidad, no es una causa termodinámica la causante de la dificultad de su síntesis, sino un problema cinético que hace necesario inhibir las reacciones de descomposición de los compuestos formados.[2] No obstante, la estabilidad termodinámica decrece con el tamaño del metal.
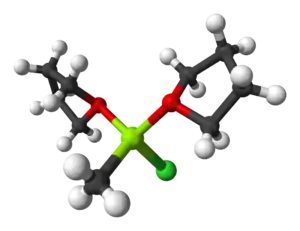
Al aumentar la temperatura, se descomponen muchos de ellos, pero a veces son reacciones lentas por lo que es posible sintetizar estos compuestos.[1] En general son poco estables frente a la oxidación y la hidrólisis pues en ambos casos se obtienen productos de gran estabilidad.
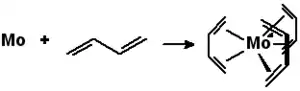
Síntesis de compuestos organometálicos
Son muy variados los métodos de síntesis:
- Reacciones entre un metal y un haluro orgánico
- Reacciones de intercambio metálico, entre un metal y un compuesto organometálico de otro metal.
- Reacciones de un compuesto organometálico con un haluro metálico.
- Reacciones de inserción:
- Inserción de olefinas y acetilenos en enlaces metal-hidrógeno para metales de los grupos 13 y 14.
- Reacciones de inserción para formación de enlaces metal-carbono para metales de otros grupos.
- Reacciones de compuestos diazo.
- Reacciones de decarboxilación de sales metálicas.
- Reacciones de formación de organometálicos de mercurio y talio con compuestos aromáticos.
- Reacciones de formación de organometálicos de mercurio con olefinas y acetilenos.
Tipos de compuestos organometálicos
Se pueden establecer diferentes clasificaciones.
Según el enlace metal-carbono
Si consideramos el carácter del enlace entre el metal (o semimetal) y el carbono tendremos:
- Iónicos (no moleculares): Compuestos organometálicos de sodio, potasio, rubidio, cesio, calcio, estroncio, bario y lantánidos.
- Intermedios: Compuestos organometálicos de litio, berilio, magnesio y aluminio. Tienen déficit de electrones y tendencia a formar puentes alquilo y enlaces multicentrados.
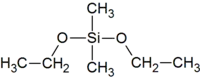
- Covalentes (moleculares): Compuestos organometálicos de boro, silicio y de elementos de los grupos 12 al 16 que estén por debajo del tercer período, como el Zn, Cd, Hg, Ga, In, Tl, Ge, Sn, Pb, As, Sb, Bi, Se, Te y Po.
- Complejos: Compuestos organometálicos de metales de transición de los grupos 3 a 11, en los que abundan los enlaces tipo pi (π).
Según el tipo de ligando
- Ligandos que se unen al metal a través de un solo átomo de carbono.
- Alquilos y ligandos relacionados : el enlace metal-carbono, M-C, es sencillo.
- Alquenilos y acilos: el enlace metal-carbono, M-C, es doble.
- Alquinilos y cianuros: el enlace metal-carbono, M-C, es triple.
- Ligandos que se unen al metal a través de varios átomos de carbono.
El número de átomos de carbono unidos directamente al metal se simboliza con ηn, que se lee n-hapto.
Según el grupo al que pertenece el metal o metaloide
- Compuestos organometálicos del grupo 1:
- Compuestos de organolitio.
- Organilos de otros metales alcalinos: compuestos de organosodio, organopotasio, organorubidio y organocesio.

- Compuestos organometálicos de los grupos 2 y 12:
- Compuestos organometálicos del grupo 2:
- Compuestos de organoberilio.
- Compuestos de organomagnesio.
- Compuestos organometálicos de calcio, estroncio y bario.
- Compuestos organometálicos del grupo 12:
- Compuestos de organozinc.
- Compuestos de organocadmio.
- Compuestos de organomercurio.
- Compuestos organometálicos del grupo 2:
- Compuestos organometálicos del Grupo 13:
- Compuestos de organoboro.
- Compuestos de organoaluminio.
- Compuestos organometálicos de Galio, Indio y Talio:
- Organilos σ de Ga, In y Tl y sus aductos.
- Complejos π de Ga, In y Tl.
- Compuestos organometálicos del Grupo 14:
- Compuestos de organosilicio: organilos, metilclorosilanos y siliconas.
- Compuestos de organogermanio.
- Compuestos de organoestaño.
- Compuestos de organoplomo.
- Compuestos organometálicos del Grupo 15: organilos de Arsénico, Antimonio y Bismuto.

- Compuestos organometálicos de los metales de transición.
- Con ligandos dadores σ.
- Con ligandos dadores σ / aceptores π.
- Con ligandos dadores σ, π /aceptores π.
- Complejos olefínicos: homoalquenos y heteroalquenos.
- Complejos alquinos: homoalquinos y heteroalquinos.
- Complejos alilos y enilos. Complejos dienilos y trienilos. Complejos ciclopentadienilos binarios.
- Complejos bis arenos metálicos.
Aplicaciones de los complejos organometálicos.

Cada día son más abundantes las aplicaciones industriales y de laboratorio de estos complejos. Entre otros usos, se pueden citar:
- Reacciones catalíticas.
- Reacciones de isomerización de olefinas.
- Reacciones de arilación y vinilación (reacción de Heck).
- Metátesis de alquenos.
- Reacciones de oligomerización y polimerización.
- Oxidación de olefinas (Proceso Wacker).
- Hidrogenación de alquenos.
- Reacciones de Fischer-Tropsch.
- Reacción de desplazamiento del gas de agua.
- Proceso Monsanto para la síntesis del ácido acético.
- Hidroformilación de olefinas (Proceso oxo).
- Hidrocianación de olefinas.
- Carbonilación de olefinas (Reacción de Reppe).
- Activación de enlaces C-H en alcanos.
Véase también
Enlaces químicos del carbono con el resto de átomos
| CH | He | |||||||||||||||||
| CLi | CBe | CB | CC | CN | CO | CF | Ne | |||||||||||
| CNa | CMg | CAl | CSi | CP | CS | CCl | CAr | |||||||||||
| CK | CCa | CSc | CTi | CV | CCr | CMn | CFe | CCo | CNi | CCu | CZn | CGa | CGe | CAs | CSe | CBr | CKr | |
| CRb | CSr | CY | CZr | CNb | CMo | CTc | CRu | CRh | CPd | CAg | CCd | CIn | CSn | CSb | CTe | CI | CXe | |
| CCs | CBa | CHf | CTa | CW | CRe | COs | CIr | CPt | CAu | CHg | CTl | CPb | CBi | CPo | CAt | Rn | ||
| Fr | CRa | Rf | Db | CSg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||
| ↓ | ||||||||||||||||||
| CLa | CCe | CPr | CNd | CPm | CSm | CEu | CGd | CTb | CDy | CHo | CEr | CTm | CYb | CLu | ||||
| Ac | CTh | CPa | CU | CNp | CPu | CAm | CCm | CBk | CCf | CEs | Fm | Md | No | Lr | ||||
| Química orgánica básica. | Muchos usos en Química. |
| Investigación académica, pero no un amplio uso. |
Enlace desconocido / no evaluado. |
Referencias
- Curso de iniciación a la Química Organometálica. Gabino A. Carriedo Ule, Daniel Miguel San José, Daniel Miguel San José. Servicio de Publicaciones de la Universidad de Oviedo, 1995. ISBN 8474688736. Pág. 11
- Química organometálica de los metales de transición. Robert H. Crabtree. Editorial de la Universitat Jaume I, 1997. ISBN 8480211342. Pág. 73