Acide oléanolique
L'acide oléanolique ou acide oléanique est un triterpénoïde pentacyclique naturel considéré comme molécule bioactive. Ce composé, qui a été isolé de plus de 1620 espèces végétales, y compris de nombreux aliments et plantes médicinales, existe sous forme d'acide libre ou d'aglycone de saponines triterpénoïdes (en)[3].
| Acide oléanolique | |

| |
| Identification | |
|---|---|
| Nom UICPA | (4aS,6aR,6aS,6bR,8aR,10S,12aR,14bS)-10-hydroxy-2,2,6a,6b,9,9,12a-heptamethyl-1,3,4,5,6,6a,7,8,8a,10,11,12,13,14b-tetradecahydropicene-4a-carboxylic acid |
| Synonymes |
Acide oléanique |
| No CAS | |
| No ECHA | 100.007.347 |
| No CE | 208-081-6 |
| PubChem | 24898021 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche à jaune clair[1] |
| Propriétés chimiques | |
| Formule | C30H48O3 [Isomères] |
| Masse molaire[2] | 456,700 3 ± 0,028 3 g/mol C 78,9 %, H 10,59 %, O 10,51 %, |
| Propriétés physiques | |
| T° ébullition | 300 °C |
| Solubilité | 0,002 g·L-1 |
| Unités du SI et CNTP, sauf indication contraire. | |
Origine naturelle
L'acide oléanolique a d'abord été étudié et isolé de plusieurs plantes, y compris Olea europaea (feuilles, fruit)[4], Rosa woodsii (feuilles), Prosopis Glandulosa (feuilles et brindilles), Phoradendron juniperinum (en) (plante entière), Syzygium claviflorum (feuilles), Hyptis capitata (en) (plante entière), Mirabilis jalapa et Ternstroemia gymnanthera (en) (partie aérienne). D'autres espèces y compris la pomme de java (Syzygium samarangense), les pousses de gui, les fleurs de clou de girofle et les feuilles de romarin[5], Phytolacca americana contiennent ce triterpénoide pentacyclique.
Biosynthèse
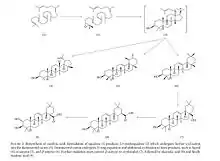
L'acide oléanolique appartient à un grand groupe de produits naturels à structure diverse qui comprend des stérols, des stéroïdes et des saponines triterpénoïdes. Une voie proposée pour la biosynthèse de l'acide oléanolique, part du farnésyl-pyrophosphate dérivé de la voie de mévalonate. À partir du farnésyl-pyrophosphate, le squalène est formé par la squalène synthétase. Le squalène subit une réaction oxydante conduisant au 2,3-Oxydosqualène. Ensuite, le 2,3-Oxydosqualène est cyclisé en beta-amyrine du triterpénoïde du type oléanane pentacyclique par la Bêta-Amyrine synthase. Enfin, la beta-amyrine est oxydée dans une séquence d'oxydation en trois étapes par CYP716A[7] pour donner de l'acide oléanolique à travers l'érythrodiol[8].
Effet biologique
L'acide oléanolique est une substance hépatoprotective[9] et présente des propriétés antitumorales et antivirales[10].
Un analogue triterpénoïde synthétique extrêmement puissant de l'acide oléanolique a été découvert en 2005, c'est-à-dire un puissant inhibiteur des processus inflammatoires cellulaires. Ils fonctionnent par induction par l'IFN-γ de l'oxyde nitrique synthase inductible (iNOS) et de la cyclooxygénase 2 dans les macrophages de souris. Ce sont des inducteurs extrêmement puissants de la réponse de phase 2 (par exemple élévation de la NADH-quinone oxydoréductase et de la hème oxygénase 1), qui est un protecteur majeur des cellules contre la contrainte oxydante et électrophile[11].
Toxicité
L'acide oléanolique est relativement non toxique, et en raison de son manque d'effets secondaires, l'acide oléanolique a été breveté au Japon comme un additif aux boissons santé et aux produits cosmétiques des cheveux. Il est également commercialisé en Chine pour les troubles du foie[12]. Cependant, des doses élevées et une utilisation à long terme peuvent produire des effets indésirables. L'administration de ce composé chez la souris a produit des lésions pathologiques dose-dépendantes au foie, comprenant l'inflammation, l'apoptose hépatocellulaireet la nécrose. Ces lésions étaient évidentes à des doses de l'acide oléanolique égales ou supérieures à 500 μmol / kg. La réaction en chaîne de la polymérase en temps réel a révélé que ce triterpènoide a entraîné une augmentation dose-dépendante des protéines de phase aiguë (MT-1 (en), Ho-1, Nrf2 et NAD(P)H dehydrogenase (quinone 1) (en)), une diminution des gènes de synthèse des acides biliaires (Cyp7a1 et Cyp8b1) et une diminution de l'acide biliaire hépatique. Les transporteurs (Ntcp (en), Bsep (en), Oatp1a1, Oatp1b2 et Ostβ)[13].
Une étude de 2002 chez les rats Wistar a révélé que l'acide oléanolique réduit la qualité du sperme et la motilité, causant l'infertilité. Après avoir retiré l'exposition, les souris ont retrouvé la fertilité et ont imprégné avec succès des souris femelles[14].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Oleanolic acid » (voir la liste des auteurs).
- Oleanolic acid at Sigma-Aldrich
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Human Metabolome Database: Showing metabocard for Oleanolic acid (HMDB02364) », sur www.hmdb.ca (consulté le )
- (en) Sedef N. El et Sibel Karakaya, « Olive tree (Olea europaea) leaves: potential beneficial effects on human health », Nutrition Reviews, vol. 67, no 11, , p. 632–638 (ISSN 0029-6643 et 1753-4887, PMID 19906250, DOI 10.1111/j.1753-4887.2009.00248.x, lire en ligne, consulté le )
- (en) Sebastian Jäger, Holger Trojan, Thomas Kopp et Melanie N. Laszczyk, « Pentacyclic Triterpene Distribution in Various Plants – Rich Sources for a New Group of Multi-Potent Plant Extracts », Molecules, vol. 14, no 6, , p. 2016–2031 (DOI 10.3390/molecules14062016, lire en ligne, consulté le )
- (en) Wei Hsum Yap et Yang Mooi Lim, « Mechanistic Perspectives of Maslinic Acid in Targeting Inflammation », Biochemistry Research International, vol. 2015, , p. 1–9 (ISSN 2090-2247, PMID 26491566, PMCID 4600485, DOI 10.1155/2015/279356, lire en ligne, consulté le )
- (en) Ery O. Fukushima, Hikaru Seki, Kiyoshi Ohyama et Eiichiro Ono, « CYP716A Subfamily Members are Multifunctional Oxidases in Triterpenoid Biosynthesis », Plant and Cell Physiology, vol. 52, no 12, , p. 2050–2061 (ISSN 0032-0781 et 1471-9053, PMID 22039103, DOI 10.1093/pcp/pcr146, lire en ligne, consulté le )
- Jacob Pollier et Alain Goossens, « Oleanolic acid », Phytochemistry, vol. 77, , p. 10–15 (DOI 10.1016/j.phytochem.2011.12.022, lire en ligne, consulté le )
- (en) Changjin Liu, Ying Li, Guowei Zuo et Wenchun Xu, « Oleanolic Acid Diminishes Liquid Fructose-Induced Fatty Liver in Rats: Role of Modulation of Hepatic Sterol Regulatory Element-Binding Protein-1c-Mediated Expression of Genes Responsible for De Novo Fatty Acid Synthesis », Evidence-Based Complementary and Alternative Medicine, vol. 2013, , p. 1–11 (ISSN 1741-427X, PMID 23737835, PMCID 3659486, DOI 10.1155/2013/534084, lire en ligne, consulté le )
- Jie Liu, « Oleanolic acid and ursolic acid: Research perspectives », Journal of Ethnopharmacology, 100th Volume Special Section: Perspectives of Ethnopharmacology, vol. 100, nos 1–2, , p. 92–94 (DOI 10.1016/j.jep.2005.05.024, lire en ligne, consulté le )
- (en) Albena T. Dinkova-Kostova, Karen T. Liby, Katherine K. Stephenson et W. David Holtzclaw, « Extremely potent triterpenoid inducers of the phase 2 response: Correlations of protection against oxidant and inflammatory stress », Proceedings of the National Academy of Sciences of the United States of America, vol. 102, no 12, , p. 4584–4589 (ISSN 0027-8424 et 1091-6490, PMID 15767573, PMCID 555528, DOI 10.1073/pnas.0500815102, lire en ligne, consulté le )
- Jie Liu, « Pharmacology of oleanolic acid and ursolic acid », Journal of Ethnopharmacology, vol. 49, no 2, , p. 57–68 (DOI 10.1016/0378-8741(95)90032-2, lire en ligne, consulté le )
- (en) Yuan-Fu Lu, Xiao-Li Wan, Yasha Xu et Jie Liu, « Repeated Oral Administration of Oleanolic Acid Produces Cholestatic Liver Injury in Mice », Molecules, vol. 18, no 3, , p. 3060–3071 (DOI 10.3390/molecules18033060, lire en ligne, consulté le )
- (en) M. C. Mdhluli et G. van der Horst, « The effect of oleanolic acid on sperm motion characteristics and fertility of male Wistar rats », Laboratory Animals, vol. 36, no 4, , p. 432–437 (DOI 10.1258/002367702320389107, lire en ligne, consulté le )
- Portail de la chimie
- Portail de la biochimie