Aminobenzaldéhyde
L'aminobenzaldéhyde est un composé aromatique de formule C7H7NO. Il est constitué d'un cycle benzénique substitué par un groupe formyle (benzaldéhyde) et un groupe amine. Comme tous les benzènes disubstitués, il existe sous la forme de trois isomères structuraux, les composés ortho, méta et para, selon la position relative des deux substituants sur le cycle.
Propriétés
| Aminobenzaldéhyde | |||
| Nom | 2-aminobenzaldéhyde | 3-aminobenzaldéhyde | 4-aminobenzaldéhyde |
| Autre nom | ortho-aminobenzaldéhyde o-aminobenzaldéhyde 2-formylaniline anthranilaldéhyde |
méta-aminobenzaldéhyde m-aminobenzaldéhyde 3-formylaniline |
para-aminobenzaldéhyde p-aminobenzaldéhyde 4-formylaniline |
| Représentation | 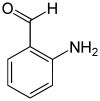 |
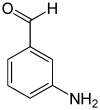 |
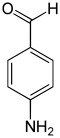 |
| Numéro CAS | |||
| Numéro ECHA | 100.007.687 | 100.015.426 | 100.008.288 |
| PubChem | 68255 | 74366 | 11158 |
| Formule brute | C7H7NO | ||
| Masse molaire | 121,14 g·mol−1 | ||
| État | solide | ||
| Apparence | solide cristallin jaune clair[1] |
||
| Point de fusion | 37 °C[1] | 71 °C[2] | |
| Point d'ébullition | 80 à 85 °C (3 hPa)[1] | ||
| Point d'éclair | 113 °C (coupelle fermée)[1] | ||
| SGH[1],[3] |  |
 Attention | |
| Phrase H et P[1],[3] | H315, H319 et H335 |
H302, H315, H317, H319 et H335 | |
| P280 et P304+P340+P312 P305+P351+P338 et P332+P313 P362, P337+P313 et P403+P233 |
P261, P264, P270 et P271 P272, P280, P301+P312 et P302+P352 P312, P304+P340 et P305+P351+P338 P330, P332+P313 et P333+P313 P362, P363, P337+P313 et P403+P233 P405 et P501 | ||
Synthèse
Le 2-aminobenzaldéhyde est préparé à partir de 2-nitrobenzaldéhyde par réduction par le fer[4] ou le sulfate de fer(II) et de l'acide chlorhydrique[5].
Le 4-aminobenzaldéhyde est préparé à partir de 4-nitrotoluène par réaction avec du sulfure de sodium et du soufre dans une solution aqueuse d'hydroxyde de sodium et d'éthanol[6].
Notes et références
- Fiche Sigma-Aldrich du composé 2-Aminobenzaldehyde, consultée le 6 avril 2020.
- Fiche (en) « Aminobenzaldéhyde », sur ChemIDplus, consulté le
- fiche PubChem
- Chen Zhang, Chandra Kanta De et Daniel Seidel, « o-Aminobenzaldehyde, Redox-Neutral Aminal Formation and Synthesis of Deoxyvasicinone », Org. Synth., vol. 89, , p. 274 (DOI 10.15227/orgsyn.089.0274)
- Lee Irvin Smith et J. W. Opie, « o-Aminobenzaldehyde », Org. Synth., vol. 28, , p. 11 (DOI 10.15227/orgsyn.028.0011)
- E. Campaigne, W. M. Budde, and G. F. Schaefer, p-Aminobenzaldehydes, Org. Synth. 31, coll. « vol. », , 6 p.
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons - Attribution - Partage dans les Mêmes. Des conditions supplémentaires peuvent s'appliquer aux fichiers multimédias.