Nétropsine
La nétropsine, également appelée congocidine et sinanomycine, est un polyamide pourvu d'une activité antibiotique et antivirale. Elle a été isolée pour la première fois à partir de l'actinomycète Streptomyces netropsis[3]. Il s'agit d'un antibiotique de la classe pyrrole-amidine, actif contre les bactéries aussi bien à Gram négatif qu'à Gram positif[4].
| Nétropsine | |||
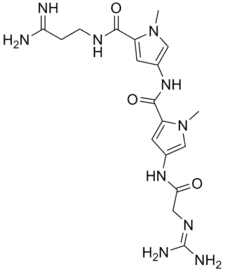 Structure de la nétropsine |
|||
| Identification | |||
|---|---|---|---|
| No CAS | (dichlorhydrate) |
||
| No ECHA | 100.162.288 | ||
| No RTECS | DW2973000 (dichlorhydrate) | ||
| PubChem | 4461 16219788 (dichlorhydrate) |
||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | C18H26N10O3 [Isomères] |
||
| Masse molaire[1] | 430,464 2 ± 0,019 1 g/mol C 50,22 %, H 6,09 %, N 32,54 %, O 11,15 %, |
||
| Précautions | |||
| SGH[2] | |||
 Danger |
|||
| Transport[2] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
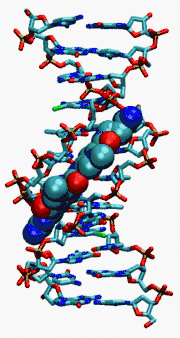
La nétropsine se lie au petit sillon des séquences riches en paires de bases A–T de l'ADN bicaténaire[4] ainsi qu'aux quadruplexes (TGGGGT)4[5], mais pas à l'ADN monocaténaire ni à l'ARN bicaténaire. Des études par cristallographie aux rayons X de nétropsine liée à l'ADN ont permis d'établir que l'oligopeptide établit des liaisons hydrogène avec quatre paires de bases consécutives dans le petit sillon de l'ADN bicaténaire[6],[7].
La liaison de la nétropsine à l'ADN augmente l'inclinaison des bases azotées d'environ 9° par tour de la double hélice, favorisant l'introduction de supertours positifs en présence de topoisomérase I[8].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) A. C. Finlay, F. A. Hochstein, B. A. Sobin et F. X. Murphy, « Netropsin, a New Antibiotic Produced by a Streptomyces », Journal of the American Chemical Society, vol. 73, no 1, , p. 341-343 (DOI 10.1021/ja01145a113, lire en ligne)
- (en) Christoph Zimmer et Ulla Wähnert, « Nonintercalating DNA-binding ligands: Specificity of the interaction and their use as tools in biophysical, biochemical and biological investigations of the genetic material », Progress in Biophysics and Molecular Biology, vol. 47, no 1, , p. 31-112 (PMID 2422697, DOI 10.1016/0079-6107(86)90005-2, lire en ligne)
- (en) Bruno Pagano, Iolanda Fotticchia, Stefano De Tito, Carlo A. Mattia, Luciano Mayol, Ettore Novellino, Antonio Randazzo et Concetta Giancola, « Selective Binding of Distamycin A Derivative to G-Quadruplex Structure [d(TGGGGT)]4 », Journal of Nucleic Acids, vol. 2010, , p. 247137 (PMID 20725616, PMCID 2915651, DOI 10.4061/2010/247137, lire en ligne)
- (en) Mary L. Kopka, Chun Yoon, David Goodsell, Philip Pjura et Richard E. Dickerson, « Binding of an antitumor drug to DNA: Netropsin and C-G-C-G-A-A-T-T-BrC-G-C-G », Journal of Molecular Biology, vol. 183, no 4, , p. 553-563 (PMID 2991536, DOI 10.1016/0022-2836(85)90171-8, lire en ligne)
- (en) M. L. Kopka, C. Yoon, D. Goodsell, P. Pjura et R. E. Dickerson, « The molecular origin of DNA-drug specificity in netropsin and distamycin », Proceedings of the National Academy of Sciences of the United States of America, vol. 82, no 5, , p. 1376-1380 (PMID 2983343, PMCID 397264, DOI 10.1073/pnas.82.5.1376, lire en ligne)
- (en) G. Snounou et A.D.B. Malcolm, « Production of positively supercoiled DNA by netropsin », Journal of Molecular Biology, vol. 167, no 1, , p. 211-216 (PMID 6306251, DOI 10.1016/S0022-2836(83)80043-6, lire en ligne)
- (en) David S. Goodsell, Mary L. Kopka et Richard E. Dickerson, « Refinement of Netropsin Bound to DNA: Bias and Feedback in Electron Density Map Interpretation », Biochemistry, vol. 34, no 15, , p. 4983-4993 (PMID 7711020, DOI 10.1021/bi00015a009, lire en ligne)
- Portail de la chimie
- Portail de la biologie cellulaire et moléculaire