Adrénaline
L’adrénaline est un neurotransmetteur et une hormone appartenant à la famille des catécholamines. Cette molécule porte aussi le nom d’épinéphrine. L’adrénaline est sécrétée en réponse à un état de stress ou en vue d'une activité physique, entraînant une augmentation de la fréquence cardiaque et une augmentation du volume d'éjection systolique du cœur conduisant à une hausse de la pression artérielle, une dilatation des bronches ainsi que des pupilles. Elle permet de préparer l'organisme à un effort intense, par exemple lorsque la faune sauvage doit faire face à un danger. Elle est souvent sécrétée en préparation d'un effort physique.
Pour les articles homonymes, voir Adrénaline (homonymie).
| Adrénaline | |
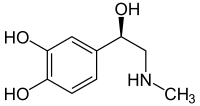
| |
| Structure de la L-adrénaline | |
| Identification | |
|---|---|
| Nom UICPA | (R)-4-(1-hydroxy-2-(méthylamino)éthyl)benzène-1,2-diol |
| Synonymes |
épinéphrine |
| No CAS | R(–) |
| No ECHA | 100.000.090 |
| No CE | 200-098-7 R(–) |
| No RTECS | DO2625000 |
| Code ATC | A01, B02, C01, C01, R01, R03, S01 |
| DrugBank | DB00668 |
| PubChem | 247704 (S) 5816 (R) |
| ChEBI | 28918 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C9H13NO3 [Isomères] |
| Masse molaire[1] | 183,204 4 ± 0,009 2 g/mol C 59 %, H 7,15 %, N 7,65 %, O 26,2 %, |
| pKa | 8.59 à 25 °C[2] |
| Propriétés physiques | |
| T° fusion | 211,5 °C[2] |
| Solubilité | 0,18 g·l-1(211,5 °C,eau)[2] |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | P21[3] |
| Paramètres de maille | a = 7,873 Å b = 6,790 Å |
| Volume | 457,25 Å3[3] |
| Précautions | |
| SGH[4] | |
 Danger |
|
| Transport[4] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Étymologie
Le mot vient du latin : ad renes (« près du rein »). Les Américains utilisent un autre nom, issu du grec, epinephrine (« au-dessus du rein »), la firme Parke Davis ayant déposé la marque « Adrenalin »[5].
Pharmacologie
L'adrénaline est majoritairement sécrétée par le système nerveux central (elle agit alors comme neuromédiateur). Elle est également sécrétée par les glandes surrénales (adrénaline libre). L’adrénaline produit son effet en se fixant sur les récepteurs adrénergiques des cellules cibles.
Les conséquences de l’adrénaline dépendent fortement de la dose et de la répartition des récepteurs alpha et bêta sur les organes. Globalement, les récepteurs alpha sont en plus grand nombre que les récepteurs bêta, mais ces derniers ont une plus forte affinité pour l’adrénaline.
Ainsi, à faible dose (0,1 μg·kg-1·min-1), l’adrénaline est préférentiellement fixée sur les récepteurs bêta. La stimulation des récepteurs bêta-1 entraîne une augmentation de la force et de la fréquence de contraction du cœur (effet inotrope et chronotrope positif), une activation de la lipolyse dans le tissu adipeux (récepteur bêta-3). La fixation de l’adrénaline sur les récepteurs bêta-2 provoque une vasodilatation, une hypotension artérielle, une hyperglycémie, une dilatation des bronches, et une relaxation des muscles de l’intestin (et plus généralement de la totalité du tractus digestif par une mise au repos des muscles lisses de ces organes et par l'arrêt de la sécrétion des glandes), de la vessie et de l’utérus.
À plus forte dose, l’adrénaline stimule à la fois les récepteurs alpha et bêta. Cependant, le cœur mis à part, les récepteurs alpha sont majoritaires sur les organes et leurs effets prédominent : il y a principalement une augmentation de la glycogénolyse dans le foie, une vasoconstriction (dominant la vasodilatation due aux récepteurs bêta-2), une hypertension artérielle. Le cœur ne possède que des récepteurs bêta-1[réf. souhaitée] et répond, quelle que soit la dose d’adrénaline, par une hausse de la force et de la fréquence des contractions.
Au niveau du métabolisme lipidique, l’adrénaline a une action identique à celle du glucagon, elle favorise l’hydrolyse des glycérides en libérant du glycérol et des acides gras.
Consulter l’article régulation de la glycémie pour le rôle de l’adrénaline dans ce phénomène.
Histoire de la découverte
En 1894, Georges Oliver et Edward Schafer montrent l'effet vasoconstricteur d'un extrait de glandes surrénales.[6]
En 1897 , John Abel extrait l’Épinéphrine (=Adrénaline) de glandes surrénales de mouton[6]
En 1901, Thomas Aldrich en détermine la formule chimique[6]
En 1906, Dale émet l'hypothèse de 2 types de récepteur cellulaire à l'adrénaline : la stimulations des uns a un effet "excitant" et inversement celle des autres un effet "relaxant"
En 1948, Alquist confirme l'hypothèse de Dale et nomme ces récepteurs "alpha" et "bêta". Il montre également que la stimulation des récepteurs "alpha" a un effet constricteur sauf au niveau des intestins. La stimulation des récepteurs "bêta" a elle un effet relaxant sauf au niveau du cœur.
Métabolisme
L’adrénaline est sécrétée par les neurones et par les cellules chromaffines de la médullosurrénale, en réponse à une stimulation directe par les neurones du système nerveux orthosympathique. La synthèse de l’adrénaline s’effectue à partir d’une autre catécholamine, la noradrénaline, par méthylation grâce à une enzyme, la phényléthanolamine N-méthyltransférase (voir aussi le métabolisme des catécholamines).
L’adrénaline a une brève durée d’action (de l’ordre de deux minutes) car elle est rapidement dégradée par deux enzymes, la catéchol-oxyméthyltransférase (COMT) et la monoamine oxydase (MAO).
Utilisation médicale
L’adrénaline en injection est le médicament de choix pour le traitement en première ligne :
- des arrêts cardiorespiratoires, essentiellement en cas d’asystolie (défaillance du muscle cardiaque sans troubles du rythme) ;
- des chocs anaphylactiques (d'origine allergique) ; en intramusculaire, par le patient lui-même s'il dispose d'un kit portable. En médecine d’urgence la prise en charge de l'anaphylaxie a fait l’objet de recommandations récentes[7]. « Le médecin régulateur du service d’aide médical urgente doit favoriser l’accès rapide à l’adrénaline et l’utilisation précoce des auto-injecteurs d’adrénaline[7]. » ;
- de certains états de choc graves (en réanimation).
Son maniement reste délicat, car un surdosage peut entraîner tachycardie et troubles du rythme cardiaque susceptibles d'aggraver l'état du patient.
Dans les chocs septiques, elle n'est pas plus efficace qu'une combinaison de dobutamine et de noradrénaline[8] ou que la noradrénaline utilisée seule, avec cependant plus d'effets secondaires avec l'adrénaline[9].
Elle est commercialisée sous différents noms[10] :
- Adrénaline Renaudin (solution injectable) : 0,25 % ; 0,5 % ; 0,1 % ; 1 % ;
- Adrénaline Aguettant (solution injectable) : 0,25 mg·ml-1 ; 0,5 mg·ml-1 ; 1 mg·ml-1 ; 1 mg·ml-1 sans sulfites.
L'adrénaline est parfois injectée à faible dose en intra-articulaire lors d'examens arthrographiques en association avec un produit de contraste, son action permet un ralentissement de l'élimination du produit de contraste (notamment son absorption par les cartilages et la synoviale) et donc d'allonger la durée de l'examen.
Effets secondaires
L'adrénaline cause plus d'arythmie cardiaque qu'une combinaison de noradrénaline et de dobutamine[11] ; elle peut aussi causer de l'hypertension artérielle avec risque d'hémorragie cérébrale.
Contre-indications
Trouble du rythme (ventriculaire), hypertension artérielle, hyperthyroïdie, insuffisance coronarienne, diabète, etc.
Synthèse
L'adrénaline a été synthétisée dès le début du XXe siècle, d'abord par le Polonais Napoleon Cybulski (1895) puis par l'Américain John Jacob Abel (en) (1897), enfin par le Japonais Jokichi Takamine, installé à Baltimore, qui fut le premier à produire des extraits purs. Le premier brevet de production d'adrénaline fut déposé en 1911 aux États-Unis (Parke-Davis & Co. v. H. K. Mulford Co) — ce qui serait la raison pour laquelle le terme d'« épinéphrine » est utilisé aux États-Unis comme terme générique. Voir History of catecholamine research (en) pour plus de détails.
Biosynthèse
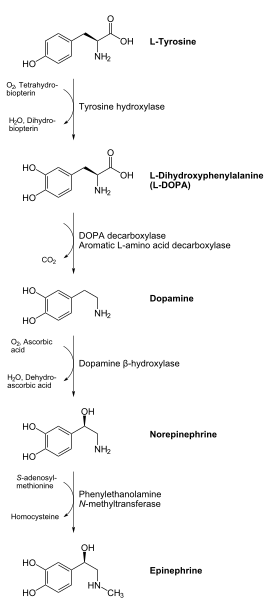
L'adrénaline peut être biosynthétisée à partir de la phénylalanine.
- La phénylalanine est d'abord hydroxylée par l'action de la phénylalanine hydroxylase en tyrosine. La biosynthèse peut d'ailleurs directement débuter à partir de la tyrosine, naturellement présente dans les organismes.
- La tyrosine est elle aussi hydroxylée par l'action de la tyrosine β hydroxylase, donnant la L-DOPA (dihydroxyphénylalanine).
- Cette dernière est décarboxylée par l'action de la DOPA-décarboxylase.
- La dopamine (dihydroxyphényléthylamine) ainsi produite est ensuite hydroxylée par l'action de la dopamine β hydroxylase, produisant la noradrénaline (norépinéphrine).
- Cette dernière, par réaction avec la S-adénosylméthionine catalysée par la PNMT (phényléthylamine-N-méthyltransférase) et méthylée pour donner finalement l'adrénaline.
Synthèse chimique
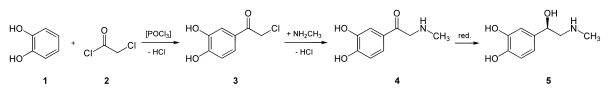
L'adrénaline peut être synthétisée à partir du catéchol (1). Il est acylé par l'action du chlorure de chloroacétyle (2) en présence de trichlorure de phosphoryle (POCl3), donnant la 3,4-dihydroxychloroacétophénone (3). Cette dernière subit une substitution nucléophile par la méthylamine pour donner une cétone, l'adrénalone (4) qui est ensuite réduite en un mélange racémique dont l'un des énantiomères est l'adrénaline (5). Ce mélange peut être séparé par l'utilisation de l'acide tartrique.
Divers
L'adrénaline fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[12].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Adrénaline », sur ChemIDplus, consulté le 4 juin 2009
- « Adrenaline », sur www.reciprocalnet.org (consulté le )
- « A ADRENALIN Trademark Application of Adrenaline, Inc. - Serial Number 85809424 :: Justia Trademarks », sur trademarks.justia.com (consulté le )
- « «Adrénaline» vs. «épinéphrine» : faisons tomber la pression », sur www.esanum.fr (consulté le )
- Meininger C (2017). Traitement des allergies graves: l’adrénaline dans l’urgence. Revue Française d'Allergologie, 57(3), 131-132. résumé
- Annane D, Vignon P, Renault A et al. Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: a randomised trial, Lancet, 2007;370:676-684
- Myburgh JA, Higgins A, Jovanovska A, Lipman J, Ramakrishnan N, Santamaria J, A comparison of epinephrine and norepinephrine in critically ill patients, Intensive Care Med, 2008;34:2226-2234
- « VIDAL : Base de données médicamenteuse pour les prescripteurs libéraux », sur VIDAL (consulté le ).
- Levy B, Perez P, Perny J, Thivilier C, Gerard A, Comparison of norepinephrine-dobutamine to epinephrine for hemodynamics, lactate metabolism, and organ function variables in cardiogenic shock: a prospective, randomized pilot study, Crit Care Med, 2011;39:450-455
- WHO Model List of Essential Medicines, 18th list, avril 2013
Voir aussi
Articles connexes
Liens externes
- Ressources relatives à la santé :
- ChEMBL
- DrugBank
- (en) Australian Register of Therapeutic Goods
- (en) International Union of Pharmacology
- (en) Medical Subject Headings
- (en) National Drug File
- (no + nn + nb) Store medisinske leksikon
- (cs + sk) WikiSkripta
- Adrénaline - Propriétés pharmacologiques. Adrénaline - dans les pharmacopées du monde - Medzai.net
- Portail de la chimie
- Portail de la médecine
- Portail de la pharmacie
- Portail des neurosciences
