Méthylènecyclopropène
Le méthylènecyclopropène ou triafulvène, est un hydrocarbure de formule C4H4, constitué d'une partie cyclopropénique avec une liaison double exocyclique. Cette molécule hautement contrainte et réactive a été synthétisée et caractérisée pour la première fois en 1984 ; elle est d'un intérêt théorique et expérimental considérable[2].
| Méthylènecyclopropène | |
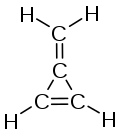
| |
| Structure du méthylènecyclopropène | |
| Identification | |
|---|---|
| Nom UICPA | 3-méthylidènecyclopropène |
| Synonymes |
triafulvène, |
| No CAS | |
| PubChem | 138112 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C4H4 [Isomères] |
| Masse molaire[1] | 52,074 6 ± 0,003 5 g/mol C 92,26 %, H 7,74 %, |
| Moment dipolaire | 1,90 D ± 0,02 D (expérimental)[2] |
| Propriétés physiques | |
| T° fusion | stabilité thermique extrêmement faible[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
Description
Le méthylènecyclopropène est le plus simple des fulvènes (famille de molécules instables, cycliques, conjuguées transversalement[4], avec un nombre impair d'atomes de carbone dans le cycle[3]), se plaçant avant le pentafulvène[5].
Sa structure possède deux liaisons doubles interagissant, et représente le système électronique π conjugué transversalement le plus simple. Le méthylènecyclopropène est un hydrocarbure non alternant (en) fondamental[2]. La valeur de son moment dipolaire (qui est élevée[6] et environ le quadruple de celle du pentafulvène, par exemple[3]) peut être calculée par la méthode de Hückel (HMO).
Son étude a fait appel à l'utilisation d'isomères isotopiques (isotopomères (en)).
Réactivité
La plupart des fulvènes sont typiquement des composés non aromatiques (d'après des données spectroscopiques), possédant plutôt des propriétés propres aux alcènes[3].
Pour le cas des tria- et pentafulvène, la possibilité de formes de résonance dipolaires suggère un caractère aromatique dans la structure cyclique ; de plus, à la différence du pentafulvène, une forme de résonance du triafulvène porte la charge négative sur l'atome de carbone exocyclique[6].
Comme l'heptafulvène (fulvène constitué d'un cycle à sept atomes), le triafulvène polymérise très facilement à −20 °C et est stabilisé par l'introduction de groupes accepteurs d'électrons sur l'atome de carbone exocyclique[3].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) I. Prigogine et Stuart A. Rice, Advances in Chemical Physics : New Methods in Computational Quantum Mechanics, John Wiley & Sons, , 813 p. (ISBN 0-471-14321-9, lire en ligne), p. 263-269
- (en) Markus Neuenschwander, « Synthetic and NMR spectroscopic investigations of fulvenes and fulvalenes » [PDF], Pure Appl. Chem., vol. 58, no 1, p. 55-56, 1986 (consulté le 19 novembre 2015).
- en anglais : Cross conjugated.
- Le pentafulvène est le fulvène proprement dit.
- (en) Francis A. Carey et Richard J. Sundberg, Advanced Organic Chemistry : Part A: Structure and Mechanisms, New York, Springer, , 5e éd., 1321 p. (ISBN 978-0-387-44897-8, lire en ligne), chap. 8, p. 754