Protéine urinaire majeure
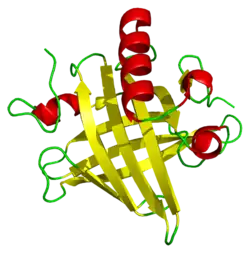
Les protéines urinaires majeures (Major urinary proteins MUPs en anglais), également connues sous le nom d’α2u-globulines sont une sous-famille de protéines que l'on trouve en abondance dans l'urine et d'autres sécrétions de nombreux animaux. Elles fournissent quelques informations permettant l'identification de l'animal producteur, après avoir été repérées par l'organe voméro-nasal de l'animal récepteur. Elles appartiennent à une grande famille de protéines appelées lipocalines. Elles sont codées par un groupe de gènes, situés côte à côte sur un seul tronçon d'ADN, qui varie grandement selon les espèces: d'au moins 21 gènes fonctionnels chez la souris à aucun chez l'homme. Ces protéines ont une forme caractéristique de gant, comprenant une poche de liaison du ligand spécifique qui accueille de petits produits chimiques organiques spécifiques.
Les protéines urinaires ont été découvertes chez l'homme en 1932, au cours d'études par Thomas Addis sur les causes de protéinuries. Les MUPs sont de puissants allergènes chez l'homme et sont les principales responsables d'un certain nombre d'allergies aux animaux comme les chats, les chevaux et les rongeurs. Leur fonction endogène est inconnue, mais elles pourraient intervenir dans la régulation des dépenses énergétiques. Toutefois, ces protéines jouent de multiples rôles dans la communication chimique entre animaux, servant de transporteurs et de stabilisateurs de phéromones chez les rongeurs et les porcs. Elles peuvent aussi agir comme des phéromones protéiques. On a démontré qu'elles provoquaient un comportement agressif chez les souris mâles et qu'une protéine spécifique retrouvée dans l'urine de souris mâle était sexuellement attirante pour les femelles. Elles peuvent également fonctionner comme des signaux entre des espèces différentes: des souris affichent une réaction de peur instinctive à la détection de MUPs provenant de prédateurs comme les chats et les rats.
Découvertes
Les êtres humains en bonne santé n'excrètent dans leurs urines que de très faibles quantités de protéines. C'est pourquoi, depuis 1827, médecins et scientifiques se sont intéressés à la présence anormale de protéines dans les urines (protéinurie) comme indicateur de maladie rénale[2],[3]. Pour mieux comprendre l'origine de la protéinurie, certains scientifiques ont tenté d'étudier le phénomène sur des animaux de laboratoire[4]. Entre 1932 et 1933, un certain nombre de scientifiques, dont Thomas Addis, ont découvert indépendamment les uns des autres que certains rongeurs sains ont des protéines dans leurs urines[5],[6],[7]. Toutefois, il a fallu attendre les années 1960 pour que les principales protéines urinaires de souris et de rats soient décrites en détail[8],[9]. On a constaté que ces protéines sont principalement produites dans le foie des mâles et sécrétées par les reins en quantités chiffrées en milligrammes par jour[8],[9],[10].
Depuis qu'elles ont été découvertes, ces protéines ont été retrouvées exprimées de façon différente dans des glandes exocrines comme notamment les glandes lacrymales, parotides, submaxillaires, sublinguales, préputiales et mammaires[11],[12],[13]. Chez certaines espèces, comme les chats et les porcs, les MUPs ne sont pas trouvées dans les urines mais dans les sécrétions, principalement dans la salive[14],[15]. Parfois, le terme de MUPs urinaires (uMUPs) est utilisé pour distinguer les MUPs retrouvées dans l'urine de celles trouvées dans d'autres tissus[16].
Les gènes MUPs
Entre 1979 et 1981, on a découvert que les MUPs sont codées par une famille de gènes comprenant entre 15 et 35 gènes et pseudogènes chez la souris et par environ 20 gènes chez le rat[17],[18],[19]. En 2008, un nombre plus exact de gènes MUP de toute une série d'espèces ont été découverts en analysant les séquences d'ADN de génomes entiers[1],[20].
Rongeurs
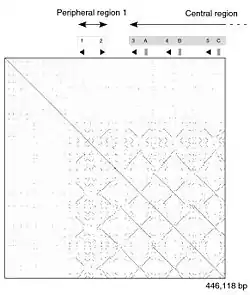
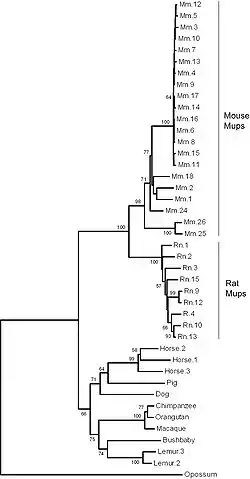
Le génome de référence est celui de la souris qui a au moins 21 gènes distincts MUPs (avec des cadres de lecture ouverts) et 21 autres pseudogènes MUPs (avec des cadres de lecture perturbés par une mutation non-sens ou une duplication incomplète de gènes. Ils sont tous regroupés, situés côte à côte dans 1,92 mégabases d'ADN sur le chromosome 4. Les 21 gènes fonctionnels ont été divisés en deux sous-classes en fonction de leur position et de la similarité des séquences: 6 périphériques de « Classe A Mups » et 15 centraux de « catégorie B Mups »[1],[21]. Le groupe de gènes de la classe B est formé par un certain nombre de duplications de l'un des gènes de catégorie A. Comme tous les gènes de classe B sont presque identiques les uns aux autres, les chercheurs en ont conclu que ces duplications ont eu lieu très récemment dans l'évolution de la souris. En effet, la structure répétitive de ces gènes MUPs centraux signifie qu'ils sont susceptibles d'être instables et peuvent varier en nombre chez les souris dans la nature[21]. Les gènes de classe A sont plus différents entre eux et sont donc susceptibles d'être plus stables mais si elles existent, les différences fonctionnelles de ces classes sont inconnues[1]. La similitude entre les gènes de la région rend difficile l'étude de l'ADN en utilisant la technologie actuelle de séquençage. En conséquence, le groupe de gènes MUPs est l'un des rares parties du génome de la souris présentant encore des lacunes et où d'autres gènes peuvent être encore ignorés[1],[21].
L'urine du rat contient également des protéines urinaires homologues; bien qu'elles aient reçu au départ un nom différent -les α2u-globulines[9],[10]-, elles sont maintenant connues comme les rat MUPs[22],[23]. Les rats ont 9 gènes MUPS distincts et 13 autres pseudogènes regroupés dans 1,1 mégabase d'ADN sur le chromosome 5. Comme chez la souris, le groupe est formé de nombreuses duplications. Toutefois, cela s'est produit de façon indépendante des duplications chez la souris, ce qui signifie que ces deux genres de rongeurs ont élargi leurs familles de gènes MUPs séparément, mais en parallèle[1],[24].
Non-rongeurs
La plupart des autres mammifères étudiés, y compris le porc, la vache, le chat, le chien, le galago, le macaque, le chimpanzé et l'orang-outan, ont un seul gène MUP. Certains, toutefois, en ont un plus grand nombre: le cheval a trois gènes MUP et le Microcèbe mignon en a au moins deux. Insectes, poissons, amphibiens, oiseaux et marsupiaux semblent avoir une synténie perturbée au niveau de la position du groupe de gènes MUPs, suggérant que cette famille de gènes est peut-être spécifique aux mammifères placentaires[1]. L'homme est le seuls mammifère placentaire n'ayant pas de gène MUP actif, mais plutôt qui a un pseudogène unique contenant une mutation qui provoque un mauvas épissage, le rendant non fonctionnel[1].
Rôles des protéines de transport
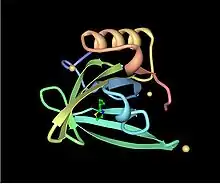
Les MUPs appartiennent à une grande famille de protéines de bas poids moléculaire (~ 19 kDa) appelées lipocalines[26]. Elles ont une structure caractéristique faite de huit feuillets beta antiparallèles formant une sorte de tonneau ouvert, avec des hélices alpha aux deux extrémités[26]. Elles ont par conséquent, une forme caractéristique de gant, comprenant une poche qui peut fixer de petits produits chimiques organiques ayant une haute affinité[1],[27]. Un certain nombre de ligands se fixent ainsi aux MUPs de souris, comme le 2-sec-butyl-4,5-dihydrothiazole (en abrégé SBT ou DHT), le 6-hydroxy-6-méthyl-3-heptanone (HMH) et la 2,3 dihydro-exo-brévicomine (DHB)[28],[29],[30]. Ce sont tous des produits chimiques spécifiques de l'urine qui se sont montrés être des phéromones c'est-à-dire des produits excrétés par un individu et qui déclenchent une réaction innée de comportement d'un autre membre de la même espèce[28],[31]. On a également démontré que les MUPs de souris servaient de stabilisateurs de phéromone, permettant une libération lente du produit qui prolonge la durée de vie des phéromones urinaires volatiles utilisées par les mâles pour marquer leurs territoires[32]. Compte tenu de la diversité des MUPs chez les rongeurs, on a d'abord pensé que les différents MUPs avaient des poches de formes différentes et fixaient donc des phéromones différentes. Toutefois, des études détaillées ont permis de constater que la plupart des sites variables sont situés à la surface des protéines et semblent avoir peu d'effet sur la liaison du ligand[33].
Les MUPs de rats fixent différents produits chimiques de petite taille. Le 1-chlorodécane est le ligand le plus commun, alors que le 2-méthyl-N-phényl-2-amide hexadécane et le 2,6,11-triméthyl décane semblent un peu moins communs[34]. Les MUPs de certaines espèces de rats fixent également le limonène-1,2-époxyde, ce qui entraîne une maladie du rein chez l'hôte, la néphropathie à gouttelettes hyalines qui évolue en cancer. D'autres espèces ne développent pas cette maladie parce que leur MUPs ne se lient pas à ce produit chimique[35]. Lorsque des souris transgéniques ont été génétiquement modifiées pour exprimer ce MUP de rat, leurs reins développent la maladie[36]. Cette MUP, retrouvée chez les porcs, nommée lipocaline salivaire (SAL), est produite par les glandes salivaires des mâles et se lie étroitement à l'androsténone et à l'androsténol, deux phéromones qui provoquent chez les femelles une position d'accouplement[1],[15].
Les phéromones
On a mené des études pour connaître le rôle précis des Mups dans les communications par phéromones. On a montré que ces protéines provoquaient l'apparition de la puberté et accéléraient l'œstrus chez les souris femelles, induisant les effets Vandenbergh et Whitten[37],[38]. Toutefois, dans les deux cas, les MUPs devaient être présentées aux femelles dissoutes dans l'urine des mâles, indiquant que la protéine nécessite un certain complément urinaire pour fonctionner. En 2007, des MUPs que l'on trouve normalement dans l'urine de souris mâles ont été synthétisées par des bactéries transgéniques. Elles étaient donc dépourvues de leurs ligands habituels. Ces Mups se sont avérées suffisantes pour déclencher un comportement agressif chez les mâles, même en l'absence d'urine[20]. En outre, ces Mups faites par des bactéries peuvent activer les neurones sensoriels olfactifs de l'organe voméronasal (VNO), une partie du nez qui détecte les phéromones spécifiques via des récepteurs sensoriels, chez les souris et les rats[20],[39]. L'ensemble de ces faits démontre que les protéines MUPs peuvent se comporter comme des phéromones eux-mêmes, indépendamment de leurs ligands[40].

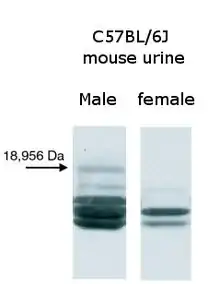
En accord avec le comportement agressif des souris mâles entre elles, on a constaté que les souris mâles adultes produisaient davantage de MUPs dans leur urine que les femelles, les jeunes ou les mâles castrés. Le mécanisme précis de l'origine de cette différence entre sexes est complexe, mais au moins trois hormones: testostérone, hormone de croissance et thyroxine sont connues pour influer positivement sur la production de MUPs chez la souris[41]. L'urine des souris communes sauvages contient des proportions variables de quatre à sept protéines MUPs distinctes par souris[42]. Certaines souches consanguines de souris de laboratoire, telles que BALB/c et C57BL/6, ont également différentes protéines dans leur urine[21]. Cependant, contrairement aux souris sauvages, les différents individus d'une même souche produisent le même modèle de protéine, un artefact dû à de nombreuses générations de consanguinité[43],[44]. Un MUP est un peu moins variable que les autres: il est toujours produit dans de fortes proportions chez les souris mâles sauvages et n'est presque jamais retrouvé dans l'urine des femelles. Lorsque ce MUP a été synthétisé par des bactéries et utilisé pour des tests de comportement, on a constaté qu'il attirait les souris femelles. D'autres MUPs ont été testés, mais ils n'ont pas les mêmes qualités attrayantes, ce qui suggère que ce MUP spécifique du sexe masculin se comporte comme une phéromone sexuelle[45]. Les scientifiques ont appelé ce MUP Darcin, référence humoristique à Fitzwilliam Darcy, le héros romantique de « Orgueil et Préjugés »[46],[47]. Dans l'ensemble, les modèles complexes de MUPs permettent théoriquement de fournir des informations à distance sur l'animal producteur, comme le sexe, la fécondité, la dominance sociale, l'âge, la diversité génétique ou la parenté[20],[48],[49]. Les souris sauvages (à la différence des souris de laboratoire qui sont génétiquement identiques et qui ont donc également des MUPs identiques) ont des modes d'expression individuelle par leurs MUPs urinaires qui agissent comme un code-barres pour identifier le propriétaire d'une odeur caractéristique[48].
Les kairomones
En plus de servir de signaux sociaux entre membres de la même espèce, les MUPs peuvent agir comme kairomones, ces substances chimiques qui transmettent des informations entre espèces[50],[51],[52]. Les souris sont instinctivement peur lorsqu'elles détectent l'odeur de leurs prédateurs naturels, comme les chats et les rats. Cela se produit même chez des souris de laboratoire qui ont été isolées des prédateurs depuis des centaines de générations[53]. Lorsque les signaux chimiques responsables de la réaction de peur ont été purifiés à partir de la salive de chat et de l'urine du rat, deux protéines homologues ont été identifiées: Fel d 4 (Felis domesticus allergène 4), produite par le gène MUP des chats, et Rat n 1 (Rattus norvegicus allergène 1), produit par le gène Mup13 du rat[51]. Les souris ont peur en sentant ces Mups même quand ils sont produits par des bactéries, alors que des animaux mutants, incapables de détecter le Mups, n'ont montré aucune peur des rats, ce qui démontre leur importance dans l'apparition du comportement de peur[50],[54]. On ne sait pas exactement comment les MUPs provenant de différentes espèces provoquent des comportements disparates, mais on a démontré que les MUPs de souris et les MUPs de prédateurs activaient les mêmes neurones sensoriels du nez des souris. Cela implique que la souris les perçoit différemment, par le biais des circuits neuronaux distincts[50],[51]. Les récepteurs de phéromones responsables de la détection des MUPs sont également inconnus, même si l'on pense qu'ils sont de la classe des récepteurs V2R[20],[51].
Allergènes
Avec d'autres membres de la famille des lipocalines, les protéines urinaires majeures peuvent être des allergènes puissants pour les humains[56]. La raison n'en est pas connue mais la ressemblance moléculaire entre les MUPs et des lipocalines humaines structurellement similaires est une explication possible[57]. La protéine produite par le gène MUP17 de la souris, connue sous le nom de Mus m 1, Ag1 ou MA1 figure parmi les plus puissants allergènes de l'urine de souris[1],[58]. Cette protéine est extrêmement stable dans l'environnement. Des études l'ont trouvé dans 95 % des foyers urbains et 82 % de tous les types de logements aux États-Unis en ont un niveau détectable dans au moins une pièce[59],[60]. De même, Rat n 1 est un allergène connu pour l'homme[56]. Une étude américaine a constaté sa présence dans 33 % des logements urbains et 21 % de leurs occupants ont été sensibilisés à l'allergène[61]. L'exposition et la sensibilisation aux protéines MUPs de rongeurs est considérée comme un facteur de risque pour l'asthme infantile et une cause majeure d'allergie aux animaux de laboratoire (AAL)-une maladie professionnelle des techniciens et des scientifiques travaillant sur ce type d'animaux[62],[63],[64],[65]. Une étude a révélé que les deux tiers des travailleurs de laboratoire qui ont développé des réactions asthmatiques à des animaux présentaient des anticorps contre le MUP Rat n 1[66].
Les gènes MUPs d'autres mammifères codent aussi pour des protéines allergisantes, par exemple Fel d 4 est une protéine produite principalement par les glandes salivaires sous-maxillaires et que le chat dépose sur ses poils lorsqu'il fait sa toilette. Une étude a montré que 63 % des personnes allergiques aux chats ont des anticorps contre cette protéine. La plupart avaient des titres d'anticorps anti-Fel d 4 supérieurs à ceux anti-Fel d 1, un autre allergène des plus connus du chat[14]. De même, Equ c1 (Equus caballus allergène 1) est une protéine MUP de cheval produite par le foie et les glandes salivaires submaxillaires et sublinguales[1],[67]. Elle est responsable d'environ 80 % des anticorps retrouvés chez les patients exposés de façon chronique aux allergènes de cheval[67].
Métabolisme
Bien qu'on ait étudié des Mups excrétés par d'autres animaux, on connait peu de choses sur leur rôle fonctionnel. Toutefois, en 2009, on a montré que les Mups se sont avérés être associés à la régulation de la dépense énergétique chez la souris. Les scientifiques ont découvert que des souris génétiquement induites obèses et diabétiques produisaient trente fois moins d'ARN de MUPs que leurs congénères de poids normal[68]. Quand on injecte directement des protéines Mup dans le sang de ces souris, on observe une augmentation de leur dépense énergétique, de leur activité physique et de leur température corporelle ainsi qu'une diminution correspondante de leur intolérance au glucose (f;] et de leur résistance à l'insuline. Il semble que les effets bénéfiques des Mups sur le métabolisme énergétique soient dus à l'amélioration de la fonction mitochondriale dans les muscles du squelette[68]. Une étude a montré que les Mups diminuaient chez les souris rendues obèses par l'alimentation. Dans ce cas, la présence de Mups dans la circulation sanguine des souris diminuait la production de glucose en inhibant directement l'expression des gènes dans le foie[69].
Voir aussi
- Acétate de vaccenyl, une phéromone de drosophile
- Complexe majeur d'histocompatibilité
- Protéines produites et sécrétées par le foie
- Fel d 1
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Major urinary proteins » (voir la liste des auteurs).
- (en) DW LoganW, TF Marton, L Stowers, « Species specificity in major urinary proteins by parallel evolution », PLoS ONE, vol. 3, no 9, , e3280 (PMID 18815613, PMCID 2533699, DOI 10.1371/journal.pone.0003280)
- C'est cette même année que Richard Bright décrivit pour la première fois une maladie connue sous le nom de maladie de Bright ou insuffisance rénale chronique avec présence d'albumine dans l'urine.
- (en) WD Comper, LM Hilliard, DJ Nikolic-Paterson, LM Russo, « Disease-dependent mechanisms of albuminuria », Am. J. Physiol. Renal Physiol., vol. 295, no 6, , F1589–600 (PMID 18579704, DOI 10.1152/ajprenal.00142.2008)
- (en) KV Lemley, L. Pauling, « Thomas Addis: 1881–1949 », Biographical Memoirs, National Academy of Sciences, vol. 63, , p. 1–46 (lire en ligne)
- (en) T. Addis, « Proteinuria and cylinduria », Proceedings of the California Academy of Sciences, vol. 2, , p. 38–52
- (en) Bell ME., « Albuminuria in the normal male rat », Journal of Physiology, vol. 79, no 2, , p. 191–93 (PMID 16994453, PMCID 1394952)
- (en) IA Parfentjev, WA Perlzweig, « The Composition of the Urine of White Mice », The Journal of Biological Chemistry, vol. 100, , p. 551–55 (lire en ligne)
- (en) JS Finlayson, R Asofsky, M Potter, CC Runner, « Major urinary protein complex of normal mice: origin », Science, vol. 149, no 687, , p. 981–82 (PMID 5827345, DOI 10.1126/science.149.3687.981)
- (en) AK Roy, OW Neuhaus, « Identification of rat urinary proteins by zone and immunoelectrophoresis », Proceedings of the Society for Experimental Biology and Medicine, vol. 121, no 3, , p. 894–99 (PMID 4160706)
- (en) AK Roy, OW Neuhaus, « Proof of the hepatic synthesis of a sex-dependent protein in the rat », Biochimica et Biophysica Acta, vol. 127, no 1, , p. 82–87 (PMID 4165835, DOI 10.1016/0304-4165(66)90478-8)
- (en) WA Held, JF Gallagher, « Rat alpha 2u-globulin mRNA expression in the preputial gland », Biochemical Genetics, vol. 23, nos 3–4, , p. 281–90 (PMID 2409959, DOI 10.1007/BF00504325)
- (en) RM Gubits, KR Lynch, AB Kulkarni, et al., « Differential regulation of alpha 2u globulin gene expression in liver, lachrymal gland, and salivary gland », The Journal of Biological Chemistry, vol. 259, no 20, , p. 12803–809 (PMID 6208189, lire en ligne)
- (en) K Shahan, M Denaro, M Gilmartin, Y Shi, E Derman, « Expression of six mouse major urinary protein genes in the mammary, parotid, sublingual, submaxillary, and lachrymal glands and in the liver », Molecular and Cellular Biology, vol. 7, no 5, , p. 1947–54 (PMID 3600653, PMCID 365300, lire en ligne)
- (en) Smith W, Butler AJ, Hazell LA, et al., « Fel d 4, a cat lipocalin allergen », Clinical and Experimental Allergy, vol. 34, no 11, , p. 1732–38 (PMID 15544598, DOI 10.1111/j.1365-2222.2004.02090.x)
- (en) D Loebel, A Scaloni, S Paolini, et al., « Cloning, post-translational modifications, heterologous expression and ligand-binding of boar salivary lipocalin », The Biochemical Journal, vol. 350, no Pt 2, , p. 369–79 (PMID 10947950, PMCID 1221263, DOI 10.1042/0264-6021:3500369)
- (en) RJ Beynon, JL Hurst, « Multiple roles of major urinary proteins in the house mouse, Mus domesticus », Biochemical Society Transactions, vol. 31, no Pt 1, , p. 142–46 (PMID 12546672, DOI 10.1042/BST0310142)
- (en) DT Kurtz, « Rat alpha 2u globulin is encoded by a multigene family », Journal of Molecular and Applied Genetics, vol. 1, no 1, , p. 29–38 (PMID 6180115)
- (en) ND Hastie, WA Held, JJ Toole, « Multiple genes coding for the androgen-regulated major urinary proteins of the mouse », Cell, vol. 17, no 2, , p. 449–57 (PMID 88267, DOI 10.1016/0092-8674(79)90171-5)
- (en) JO Bishop, AJ Clark, PM Clissold, S Hainey, U Francke, « Two main groups of mouse major urinary protein genes, both largely located on chromosome 4 », The EMBO Journal, vol. 1, no 5, , p. 615–20 (PMID 6329695, PMCID 553096)
- (en) P Chamero, TF Marton, DW Logan, et al., « Identification of protein pheromones that promote aggressive behaviour », Nature, vol. 450, no 7171, , p. 899–902 (PMID 18064011, DOI 10.1038/nature05997)
- (en) JM Mudge, SD Armstrong, K McLaren, et al., « Dynamic instability of the major urinary protein gene family revealed by genomic and phenotypic comparisons between C57 and 129 strain mice », Genome Biology, vol. 9, no 5, , R91 (PMID 18507838, PMCID 2441477, DOI 10.1186/gb-2008-9-5-r91)
- (en) J Hurst, RJ Beynon, SC Roberts, TD Wyatt, Urinary Lipocalins in Rodenta:is there a Generic Model? , Springer New York, coll. « Chemical Signals in Vertebrates 11 », (ISBN 978-0-387-73944-1)
- (en) Cavaggioni A, Mucignat-Caretta C, « Major urinary proteins, alpha(2U)-globulins and aphrodisin », Biochimica et Biophysica Acta, vol. 1482, nos 1–2, , p. 218–28 (PMID 11058763, DOI 10.1016/S0167-4838(00)00149-7)
- (en) DA McFadyen, W Addison, J Locke, « Genomic organization of the rat alpha 2u-globulin gene cluster », Mammalian Genome, vol. 10, no 5, , p. 463–70 (PMID 10337619, DOI 10.1007/s003359901024)
- Z. Böcskei, C. R. Groom, D. R. Flower et al., « Pheromone binding to two rodent urinary proteins revealed by X-ray crystallography », Nature, vol. 360, no 6400, , p. 186–188 (PMID 1279439, DOI 10.1038/360186a0)
- (en) DR Flower, « The lipocalin protein family: structure and function », The Biochemical Journal, vol. 318, no 1, , p. 1–14 (PMID 8761444, PMCID 1217580, lire en ligne)
- (en) MD Ganfornina, G Gutiérrez, M Bastiani, D Sánchez, « A phylogenetic analysis of the lipocalin protein family », Molecular Biology and Evolution, vol. 17, no 1, , p. 114–26 (PMID 10666711, lire en ligne)
- (en) M Halpern, A Martínez-Marcos, « Structure and function of the vomeronasal system: an update », Progress in Neurobiology, vol. 70, no 3, , p. 245–318 (PMID 12951145, DOI 10.1016/S0301-0082(03)00103-5)
- (en) DE Timm, LJ Baker, H Mueller, L Zidek, MV Novotny, « Structural basis of pheromone binding to mouse major urinary protein (MUP-I) », Protein Science, vol. 10, no 5, , p. 997–1004 (PMID 11316880, PMCID 2374202, DOI 10.1110/ps.52201)
- (en) SD Armstrong, DH Robertson, SA Cheetham, JL Hurst, RJ Beynon, « Structural and functional differences in isoforms of mouse major urinary proteins: a male-specific protein that preferentially binds a male pheromone », The Biochemical Journal, vol. 391, no Pt 2, , p. 343–50 (PMID 15934926, PMCID 1276933, DOI 10.1042/BJ20050404)
- (en) L Stowers, TF Marton, « What is a pheromone? Mammalian pheromones reconsidered », Neuron, vol. 46, no 5, , p. 699–702 (PMID 15924856, DOI 10.1016/j.neuron.2005.04.032)
- (en) JL Hurst, DHL Robertson, U Tolladay, RJ Beynon, « Proteins in urine scent marks of male house mice extend the longevity of olfactory signals », Animal Behaviour, vol. 55, no 5, , p. 1289–97 (PMID 9632512, DOI 10.1006/anbe.1997.0650)
- (en) A Darwish Marie, C Veggerby, DH Robertson, et al., « Effect of polymorphisms on ligand binding by mouse major urinary proteins », Protein Science, vol. 10, no 2, , p. 411–17 (PMID 11266626, PMCID 2373947, DOI 10.1110/ps.31701)
- (en) R Rajkumar, R Ilayaraja, C Mucignat, A Cavaggioni, G Archunan, « Identification of alpha2u-globulin and bound volatiles in the Indian common house rat (Rattus rattus) », Indian Journal of Biochemistry & Biophysics, vol. 46, no 4, , p. 319–24 (PMID 19788064)
- (en) LD Lehman-McKeeman, D Caudill, « Biochemical basis for mouse resistance to hyaline droplet nephropathy: lack of relevance of the alpha 2u-globulin protein superfamily in this male rat-specific syndrome », Toxicology and Applied Pharmacology, vol. 112, no 2, , p. 214–21 (PMID 1371614, DOI 10.1016/0041-008X(92)90190-4)
- (en) LD Lehman-McKeeman, D Caudill, « d-Limonene induced hyaline droplet nephropathy in alpha 2u-globulin transgenic mice », Fundamental and Applied Toxicology, vol. 23, no 4, , p. 562–68 (PMID 7532604, DOI 10.1006/faat.1994.1141)
- (en) C Mucignat-Caretta, A Caretta, A Cavaggioni, « Acceleration of puberty onset in female mice by male urinary proteins », J. Physiol. (Lond.), vol. 486 (Pt 2), , p. 517–22 (PMID 7473215, PMCID 1156539, lire en ligne)
- (en) A Marchlewska-koj, A Caretta, C Mucignat-Caretta, P Olejniczak, « Stimulation of estrus in female mice by male urinary proteins », Journal of Chemical Ecology, vol. 26, no 10, , p. 2355–65 (DOI 10.1023/A:1005578911652)
- (en) J Krieger, A Schmitt, D Löbel, et al., « Selective activation of G protein subtypes in the vomeronasal organ upon stimulation with urine-derived compounds », The Journal of Biological Chemistry, vol. 274, no 8, , p. 4655–62 (PMID 9988702, DOI 10.1074/jbc.274.8.4655)
- (en) « Aggression protein found in mice », BBC News, (5 décembre 2007) (consulté le )
- (en) JL Knopf, JF Gallagher, WA Held, « Differential, multihormonal regulation of the mouse major urinary protein gene family in the liver », Molecular and Cellular Biology, vol. 3, no 12, , p. 2232–40 (PMID 6656765, PMCID 370094, lire en ligne)
- (en) DH Robertson, JL Hurst, MS Bolgar, SJ Gaskell, RJ Beynon, « Molecular heterogeneity of urinary proteins in wild house mouse populations », Rapid Communications in Mass Spectrometry, vol. 11, no 7, , p. 786–90 (PMID 9161047, DOI 10.1002/(SICI)1097-0231(19970422)11:7<786::AID-RCM876>3.0.CO;2-8)
- (en) DH Robertson, KA Cox, SJ Gaskell, RP Evershed, RJ Beynon, « Molecular heterogeneity in the Major Urinary Proteins of the house mouse Mus musculus », The Biochemical Journal, vol. 316, no Pt 1, , p. 265–72 (PMID 8645216, PMCID 1217333, lire en ligne)
- (en) SA Cheetham, AL Smith, SD Armstrong, RJ Beynon, JL Hurst, « Limited variation in the major urinary proteins of laboratory mice », Physiology & Behavior, vol. 96, no 2, , p. 253–61 (PMID 18973768, DOI 10.1016/j.physbeh.2008.10.005)
- (en) Brennan PA, « On the scent of sexual attraction », BMC Biol, vol. 8, no 1, , p. 71 (PMID 20504292, PMCID 2880966, DOI 10.1186/1741-7007-8-71, lire en ligne)
- (en) SA Roberts, DM Simpson, SD Armstrong, et al., « Darcin: a male pheromone that stimulates female memory and sexual attraction to an individual male's odour », BMC Biol, vol. 8, no 1, , p. 75 (PMID 20525243, PMCID 2890510, DOI 10.1186/1741-7007-8-75)
- (en) Moskowitz, C, « Biologists Learn Why Mice Go Gaga for Urine », FoxNews.com, FOX News Network, (consulté le )
- (en) JL Hurst, CE Payne, CM Nevison, et al., « Individual recognition in mice mediated by major urinary proteins », Nature, vol. 414, no 6864, , p. 631–34 (PMID 11740558, DOI 10.1038/414631a)
- (en) MD Thom, P Stockley, F Jury, WE Ollier, RJ Beynon, JL Hurst, « The direct assessment of genetic heterozygosity through scent in the mouse », Current Biology, vol. 18, no 8, , p. 619–23 (PMID 18424142, DOI 10.1016/j.cub.2008.03.056)
- (en) F Papes, DW Logan, L Stowers, « The Vomeronasal Organ Mediates Interspecies Defensive Behaviors through Detection of Protein Pheromone Homologs », Cell, vol. 141, no 4, , p. 692–703 (PMID 20478258, PMCID 2873972, DOI 10.1016/j.cell.2010.03.037, lire en ligne)
- (en) I Rodriguez, « The chemical MUPpeteer », Cell, vol. 141, no 4, , p. 568–70 (PMID 20478249, DOI 10.1016/j.cell.2010.04.032)
- (en) « Why mice fear the smell of cats », BBC News, (17 mai 2010) (consulté le )
- (en) Rachel Ehrenberg, « Fight or flee, it's in the pee », Science News, (lire en ligne)
- (en) Sindya Bhanoo, « When a Mouse Smells a Rat », The New York Times, (lire en ligne)
- (en) Lascombe MB, Grégoire C, Poncet P, et al., « Crystal structure of the allergen Equ c 1. A dimeric lipocalin with restricted IgE-reactive epitopes », The Journal of Biological Chemistry, vol. 275, no 28, , p. 21572–77 (PMID 10787420, DOI 10.1074/jbc.M002854200)
- (en) R Lockey, DK Ledford, Allergens and Allergen Immunotherapy, Informa Health Care, coll. « Volume 21 of Clinical allergy and immunology », , 201–218 p. (ISBN 978-1-4200-6197-0), « Mammalian Allergens »
- (en) T Virtanen, T Zeiler, R Mäntyjärvi, « Important animal allergens are lipocalin proteins: why are they allergenic? », Int. Arch. Allergy Immunol., vol. 120, no 4, , p. 247–58 (PMID 10640908, DOI 10.1159/000024277)
- (en) JR Lorusso, S Moffat, JL Ohman, « Immunologic and biochemical properties of the major mouse urinary allergen (Mus m 1) », The Journal of Allergy and Clinical Immunology, vol. 78, no 5 Pt 1, , p. 928–37 (PMID 3097107, DOI 10.1016/0091-6749(86)90242-3)
- (en) RD Cohn, SJ Arbes, M Yin, R Jaramillo, DC Zeldin, « National prevalence and exposure risk for mouse allergen in US households », The Journal of Allergy and Clinical Immunology, vol. 113, no 6, , p. 1167–71 (PMID 15208600, DOI 10.1016/j.jaci.2003.12.592)
- (en) Phipatanakul W, Eggleston PA, Wright EC, Wood RA, « Mouse allergen. I. The prevalence of mouse allergen in inner-city homes. The National Cooperative Inner-City Asthma Study », The Journal of Allergy and Clinical Immunology, vol. 106, no 6, , p. 1070–74 (PMID 11112888, DOI 10.1067/mai.2000.110796)
- (en) T Perry, E Matsui, B Merriman, T Duong, P Eggleston, « The prevalence of rat allergen in inner-city homes and its relationship to sensitization and asthma morbidity », The Journal of Allergy and Clinical Immunology, vol. 112, no 2, , p. 346–52 (PMID 12897741, DOI 10.1067/mai.2003.1640)
- (en) RA Wood, « Laboratory animal allergens », ILAR Journal, vol. 42, no 1, , p. 12–16 (PMID 11123185)
- (en) JM Gaffin, W Phipatanakul, « The role of indoor allergens in the development of asthma », Current Opinion in Allergy and Clinical Immunology, vol. 9, no 2, , p. 128–35 (PMID 19326507, PMCID 2674017, DOI 10.1097/ACI.0b013e32832678b0)
- (en) JA Pongracic, CM Visness, RS Gruchalla, R Evans, HE Mitchell, « Effect of mouse allergen and rodent environmental intervention on asthma in inner-city children », Annals of Allergy, Asthma & Immunology, vol. 101, no 1, , p. 35–41 (PMID 18681082, DOI 10.1016/S1081-1206(10)60832-0)
- (en) S Gordon, R Preece, « Prevention of laboratory animal allergy », Occupational Medicine, vol. 53, no 6, , p. 371–77 (PMID 14514903, DOI 10.1093/occmed/kqg117)
- (en) TA Platts-Mills, J Longbottom, J Edwards, A Cockroft, S Wilkins, « Occupational asthma and rhinitis related to laboratory rats: serum IgG and IgE antibodies to the rat urinary allergen », The Journal of Allergy and Clinical Immunology, vol. 79, no 3, , p. 505–15 (PMID 3819230, DOI 10.1016/0091-6749(87)90369-1)
- (en) Gregoire C, Rosinski-Chupin I, Rabillon J, Alzari PM, David B, Dandeu JP, « cDNA cloning and sequencing reveal the major horse allergen Equ c1 to be a glycoprotein member of the lipocalin superfamily », The Journal of Biological Chemistry, vol. 271, no 51, , p. 32951–59 (PMID 8955138, DOI 10.1074/jbc.271.51.32951)
- (en) Hui X, Zhu W, Wang Y, et al., « Major urinary protein-1 increases energy expenditure and improves glucose intolerance through enhancing mitochondrial function in skeletal muscle of diabetic mice », The Journal of Biological Chemistry, vol. 284, no 21, , p. 14050–57 (PMID 19336396, PMCID 2682853, DOI 10.1074/jbc.M109.001107)
- (en) Zhou Y, Jiang L, Rui L, « Identification of MUP1 as a regulator for glucose and lipid metabolism in mice », The Journal of Biological Chemistry, vol. 284, no 17, , p. 11152–59 (PMID 19258313, PMCID 2670120, DOI 10.1074/jbc.M900754200)
- Portail de la biochimie
- Portail des odeurs, des senteurs et du parfum