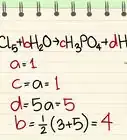X
wikiHow es un "wiki", lo que significa que muchos de nuestros artículos están escritos por varios autores. Para crear este artículo, 49 personas, algunas anónimas, han trabajado para editarlo y mejorarlo con el tiempo.
Este artículo ha sido visto 7125 veces.
Aprende a inflar un globo haciendo este experimento científico tan divertido y utilizando solo unos cuantos ingredientes que encontrarás en tu cocina. Los globos inflados de esta forma se llenan con el dióxido de carbono producido por la reacción de los dos ingredientes. No contienen helio, por lo que no flotarán en el aire.
Pasos
Parte 1
Parte 1 de 2:Inflar el globo
Parte 1
-
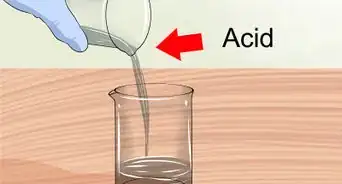
1Vierte un poco de vinagre en una botella de plástico. Elige una botella de plástico u otra botella con el cuello estrecho. Vierte entre 2,5 y 5 cm (entre 1 y 2 pulgadas) de vinagre en la botella, utilizando un embudo, si tienes. Utiliza vinagre blanco, también llamado "vinagre destilado", para obtener un resultado óptimo.
- Puedes hacer este experimento con cualquier tipo de vinagre, pero es posible que, si no usas vinagre blanco, el globo tarde más en inflarse o necesites más cantidad para que funcione. Además, el vinagre blanco suele ser el más económico.
- El vinagre puede dañar los recipientes de metal, dejando un sabor desagradable en los alimentos ahí guardados. Si no tienes botellas de plástico, utiliza una botella de agua de acero inoxidable de buena calidad para minimizar el riesgo de que esto ocurra. Disolver el vinagre en la misma cantidad de agua también puede ayudar, y no impedirá que el globo se infle.[1]
-
2Utiliza un embudo o una pajita para introducir un poco de bicarbonato sódico en un globo desinflado. Puedes utilizar un globo de cualquier forma o color. Sujétalo por el cuello, sin cerrarlo, con la parte abierta mirando hacia ti. Introduce la parte inferior de un embudo (si tienes) en el cuello del globo y, después, echa unas dos cucharadas (30 ml) de bicarbonato sódico en su interior, o, simplemente, llena el globo hasta la mitad de su capacidad.[2]
- Si no tienes un embudo, puedes colocar una pajita de plástico sobre un montón de bicarbonato sódico, tapar el agujero superior con el dedo y, después, introducir la pajita en el globo y levantar el dedo. Golpea suavemente la pajita para que caita todo el bicarbonato sódico y repite la operación hasta llenar aproximadamente 1/3 del globo.[3]
-
3Estira el cuello del globo alrededor y por encima de la boca de la botella. Ten cuidado de que no se salga el bicarbonato sódico al hacerlo. Sujeta el cuello del globo con ambas manos y estíralo alrededor y por encima de la boca de la botella en la que antes has vertido el vinagre. Si la mesa o la botella se tambalean, pídele a un amigo que sujete firmemente la botella.[4]
-
4Coloca el globo verticalmente sobre la botella y observa la reacción. El bicarbonato sódico saldrá del globo y atravesará el cuello de la botella, cayendo sobre el vinagre que hay al fondo. Llegado este punto, las dos sustancias químicas reaccionarán y burbujearán, convirtiéndose en otras sustancias. Una de ellas es el dióxido de carbono, un gas que hará que el globo se infle y se tense hacia arriba.
- Agita suavemente la botella para mezclar los dos ingredientes si ves que no hay muchas burbujas.
-
5Si no funciona a la primera, prueba otra vez usando más vinagre o más bicarbonato. Si el burbujeo para y el globo no se ha inflado a la cuenta de 100, vacía la botella e inténtalo de nuevo usando más vinagre y bicarbonato sódico. Los restos que hayan quedado en la botella, se habrán convertido en otras sustancias, principalmente agua, por lo que no podrás reutilizarlos.
- No te excedas con el vinagre. El vinagre no debe superar, en ningún caso, 1/3 de la capacidad total de la botella.
Parte 2
Parte 2 de 2:Comprender cómo funciona el proceso
Parte 2
-
1Conoce las distintas reacciones químicas. Prácticamente todo lo que te rodea está compuesto de moléculas de distintos tipos de sustancias. En muchos casos, dos tipos de moléculas reaccionan entre sí, descomponiéndose y formando moléculas distintas a partir de los nuevos fragmentos.
-
2Infórmate sobre la soda y el vinagre. Los reactivos, o las sustancias que has visto formar burbujas al reaccionar entre sí, son el bicarbonato sódico y el vinagre. A diferencia de muchos otros ingredientes que puedes encontrar en la cocina, estos dos son sustancias químicas simples en lugar de mezclas complejas compuestas por muchas sustancias químicas:[5]
- El bicarbonato sódico también es conocido como "bicarbonato de sodio".
- El vinagre blanco es una mezcla de ácido acético y agua. El ácido acético es la única sustancia que reacciona con el bicarbonato sódico.
-
3Lee acerca de esta reacción. El bicarbonato sódico es un tipo de sustancia llamada "base". El vinagre, o ácido acético, es un tipo de sustancia llamada "ácido". Las bases y los ácidos reaccionan entre sí, descomponiéndose parcialmente y dando lugar a otras sustancias. Este proceso se conoce como "neutralización" porque el resultado no es ni una base, ni un ácido. En este caso, las nuevas sustancias son agua, un tipo de sal y dióxido de carbono.[6] El dióxido de carbono (un gas) abandonará la mezcla líquida, expandiéndose en el interior de la botella y del globo, haciendo que este se infle.
- Aunque la definición de ácido y base puede complicarse, puedes comparar las características de las sustancias originales y del resultado neutralizado para ver si hay cambios obvios. Por ejemplo, el vinagre tiene un olor muy fuerte y se puede utilizar para disolver suciedad y mugre. Una vez mezclado con el bicarbonato sódico, tiene un olor mucho más suave y no es más eficaz que el agua para limpiar.
-
4Estudia la fórmula química. Si tienes nociones de química, o sientes curiosidad por la descripción científica de una reacción, consulta la siguiente fórmula, que describe la reacción entre el bicarbonato de sodio NaHCO3 y el ácido acético H C2H3O2(aq)NaC2H3O2. ¿Eres capaz de averiguar cómo se divide y se recompone cada molécula?
- NaHCO3(ac) + HC2H3O2(ac) → NaC2H3O2(ac) + H2O(l) + CO2(g)
- Las letras entre paréntesis indican el estado en el que se encuentra cada sustancia química durante y después de la reacción: (g)aseoso, (l)íquido, or (ac)uoso. "Acuoso" significa que la sustancia química está disuelta en agua.
Consejos
- También se puede utilizar este método para hacer cohetes caseros de cartón o plástico, y podrás hacerlos volar a lo largo de largas distancias, si los ingredientes son los adecuados. La razón por la que se produce este efecto propulsor es que la reacción genera gas, y la presión se acumula hasta ser liberada.
- Puedes usar jugo de lima en lugar de vinagre.
Advertencias
- Si el globo está totalmente inflado y el líquido sigue burbujeando, es posible que esté a punto de estallar. Decide si tienes tiempo para retirar el globo, o si lo único que puedes hacer es cubrirte la cara antes de que te salpique.
Cosas que necesitarás
- un globo
- vinagre
- bicarbonato sódico
- una botella de cuello estrecho
- un embudo (opcional)
- una toalla
Referencias
- ↑ https://www.exploratorium.edu/science_explorer/balloon_blowup.html
- ↑ http://www.education.com/science-fair/article/balloon-gas-chemical-reaction/
- ↑ https://www.exploratorium.edu/science_explorer/balloon_blowup.html
- ↑ https://www.education.com/science-fair/article/balloon-gas-chemical-reaction/
- ↑ https://www.wonderopolis.org/wonder/what-happens-when-you-mix-vinegar-and-baking-soda
- ↑ https://www.wonderopolis.org/wonder/what-happens-when-you-mix-vinegar-and-baking-soda