Ácido adípico
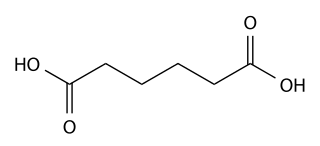
El ácido adípico o ácido hexanodioico es el compuesto orgánico con la fórmula (CH2)4(CO2H)2. Desde la perspectiva industrial, es el más importante ácido dicarboxílico: Anualmente se producen unos 2,500 millones de kilogramos de este polvo blanco cristalino, principalmente como un precursor de la producción del nailon. El ácido adípico en raras ocasiones se hace presente en la naturaleza.[3] A pesar de su nombre (del Latín adipis, grasa corporal), este ácido no es constituyente de grasas naturales, pero sí se encuentra como producto de degradación oxidativa de aceites.[4]
| Ácido adípico | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| ácido hexanodioico | ||
| General | ||
| Otros nombres |
Ácido butano-1,4-dicarboxílico Ácido hexano-1,6-dioico" | |
| Fórmula semidesarrollada | (CH2)4(CO2H)2 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 124-04-9[1] | |
| ChEBI | 30832 | |
| ChEMBL | CHEMBL1157 | |
| ChemSpider | 191 | |
| PubChem | 196 | |
| UNII | 76A0JE0FKJ | |
| KEGG | C06104 D08839, C06104 | |
| Propiedades físicas | ||
| Apariencia | cristal blanco | |
| Densidad | 1360 kg/m³; 1,36 g/cm³ | |
| Masa molar | 146,14 g mol−1 g/mol | |
| Punto de fusión | 425 K (152 °C) | |
| Punto de ebullición | 610 K (337 °C) | |
| Propiedades químicas | ||
| Acidez | 4.42, 5.42 pKa | |
| Solubilidad en agua | bastante soluble[2] | |
| Peligrosidad | ||
| Punto de inflamabilidad | 469 K (196 °C) | |
| NFPA 704 |
1
2
0
| |
| Temperatura de autoignición | 693 K (420 °C) | |
| Frases R | R36 | |
| Compuestos relacionados | ||
| ácidos dicarboxílicos |
ácido glutárico ácido pimélico | |
| compuestos | ácido hexanoico | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Preparación
Se obtuvo por Dieterle et al.[5] por la oxidación del aceite de ricino con ácido nítrico. Fue sintetizado en 1902 a partir de bromuro de tetrametileno. Históricamente, el ácido adípico ha sido preparado de diferentes formas usando oxidación. Actualmente este ácido es producido por la mezcla de ciclohexanol y ciclohexanona llamada "aceite KA", que proviene de la abreviación "ketone-alcohol" ("cetona-alcohol"). El aceite KA es oxidado con ácido nítrico para procesar el ácido adípico. Al comienzo de la reacción el ciclohexanol es convertido en cetona, liberando óxido nitroso:
- HOC6H11 + HNO3 → OC6H10 + HNO2 + H2O
Entre sus varias reacciones, el ciclohexano se torna nitroso, determinando la etapa para la escisión del enlace C-C:
- HNO2 + HNO3 → NO+NO3- + H2O
- OC6H10 + NO+ → OC6H9-2-NO + H+
Entre los productos derivados del método se incluyen a los ácidos glutáricos y succínicos.
Procesos relacionados comienzan a partir de ciclohexanol, el cual es obtenido de la hidrogenación del fenol.
Métodos alternativos de producción
Muchos métodos se han desarrollado por la carbonilación de butadieno. Por ejemplo, hidrocarboxilación procede de la siguiente forma:
- CH2=CHCH=CH2 + 2 CO + 2 H2O → HO2C(CH2)4CO2H
Usos
La mayor parte de los 2500 millones kg de ácido adípico producido anualmente es utilizado como un monómero para la producción de nailon por una reacción de policondensación formando nailon 6,6. Otra de las más relevantes aplicaciones involucran también polímeros, con lo cual el monómero utilizado en la producción de poliuretano y sus ésteres son plastificadores, especialmente en los PVC.
En comidas
Las cantidades pequeñas pero significativas de ácido adípico se utilizan como ingrediente en las comidas como un aromatizante, aunque también ayuda de gelificación.
Seguridad
El ácido adípico, al igual que la mayoría de ácidos carboxílicos, es un leve irritante para la piel. Mientras que es levemente tóxico, con una DL50 de 3600 mg/kg por ingestión oral, para las ratas.[3]
Referencias
- Número CAS
- A. N. Gaivoronskii and V. A. Granzhan (2005). «Solubility of Adipic Acid in Organic Solvents and Water». Russian Journal of Applied Chemistry 78 (3): 404-408. doi:10.1007/s11167-005-0305-0.
- M. T. Musser, "Adipic Acid" in Ullmann's Encylopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi 269 10.1002/14356007.a01 269
- DICARBOXYLIC ACIDS http://www.cyberlipid.org/fa/acid0004.htm Archivado el 7 de septiembre de 2011 en Wayback Machine.
- Ber. 1884, 17, 2221
Apéndice
- Número E E355.
- Citaciones del U.S. FDA - GRAS (21 CFR 184.1009), Aditivo indirecto (21 CFR 175.300, 21 CFR 175.320, 21 CFR 176.170, 21 CFR 176.180, 21 CFR 177.1200, 21 CFR 177.1390, 21 CFR 177.1500, 21 CFR 177.1630, 21 CFR 177.1680, 21 CFR 177.2420, 21 CFR 177.2600)
- Citaciones de la Unión Europea - Decisión 1999/217/EC - Sustancia saborizante; Directiva 95/2/EC, Annex IV - Aditivo alimentario permitido; 2002/72/EC, Annex A - Monómero autorizado para plásticos de contacto con comida.
Véase también
- Adipato de sodio y de potasio
