Ibrutinib
Ibrutinib (USAN,[1] también conocido como PCI-32765 y comercializado bajo el nombre de Imbruvica™) es un inhibidor de la Tirosina kinasa de Bruton (BTK), un fármaco antineoplásico —anticanceroso— dirigido contra el cáncer producido por células B. Fue aprobado por la FDA en noviembre de 2013 para el tratamiento del linfoma de células de manto[2][3] y en febrero de 2014 para el tratamiento de la leucemia linfática crónica.[4] Se administra por vía oral.[5][6][7][8] En enero de 2015, ibrutinib fue aprobado por la FDA para el tratamiento de la macroglobulinemia de Waldenstrom, un tipo de linfoma no-Hodgkin. El tratamiento con ibrutinib mejora en algunos pacientes los síntomas de la enfermedad de injerto contra huésped (EICH) después de recibir un trasplante de células madre de sangre donada, conocido como trasplante alogénico.[9][10]
| Ibrutinib | ||
|---|---|---|
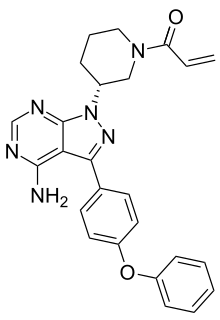 | ||
| Nombre (IUPAC) sistemático | ||
| 1-[(3R)-3-[4-amino-3-(4-fenoxyfenil)pirazolo[3,4-d]pirimidin-1-yl]piperidin-1-il]prop-2-en-1-ona | ||
| Identificadores | ||
| Número CAS | 936563-96-1 | |
| Código ATC | L01XE27 | |
| PubChem | 24821094 | |
| ChemSpider | 26637187 | |
| Datos químicos | ||
| Fórmula | C25H24N6O2 | |
|
InChI=1S/C25H24N6O2/c1-2-21(32)30-14-6-7-18(15-30)31-25-22(24(26)27-16-28-25)23(29-31)17-10-12-20(13-11-17)33-19-8-4-3-5-9-19/h2-5,8-13,16,18H,1,6-7,14-15H2,(H2,26,27,28)/t18-/m1/s1
Key: XYFPWWZEPKGCCK-GOSISDBHSA-N | ||
| Datos clínicos | ||
| Estado legal | Aprobado - ensayos clínicos | |
| Vías de adm. | Oral | |
Mecanismo de acción
En estudios preclínicos con células de leucemia linfocítica crónica (LLC), ibrutinib promovía su apoptosis, inhibía su proliferación, y también evitaba la supervivencia de dichas células impidiendo la respuesta a estímulos proporcionados por el microambiente.[11][12][13][14] Estos mecanismos confirmarían que la señalización de Ibrutinib inducen la apoptosis y/o altera tanto la migración celular como la adherencia a microambientes que protegerían a las células tumorales.
En los primeros estudios clínicos, la actividad de ibrutinib se ha descrito incluyendo una rápida reducción de la linfadenopatía acompañada por una linfocitosis transitoria.[12]
Ibrutinib ha reducido la quimiotaxis de células LLC hacia las quimiocinas CXCL12 y CXCL13, inhibiendo la adhesión celular después de la estimulación en los receptorres de células B.[15][16]
Juntos, estos datos son consistentes con un modelo mecánico mediante el cual Ibrutinib bloquea las señales BCR, lo que impulsa la apoptosis celular e interrumpe la migración celular y su adhesión a microambientes que protegen el tumor.
Efectos adversos del ibrutinib
Los efectos adversos según la incidencia pueden ser:[17][18]
Muy común (frecuencia superior al 10 %):
- Aumento de creatinina
- Trombocitopenia
- Diarrea
- Hemorragia
- Neutropenia
- Anemia
- Fatiga
- Dolores musculoesqueléticos
- Edema periférico
- Infecciones urinarias
- Náuseas
- Moratones
- Disnea
- Estreñimiento
- Erupción
- Dolor abdominal
- Vómitos
- Disminución del apetito
- Tos
- Pirexia
- Estomatitis
- Infección UTI
- Neumonía
- Infecciones de la piel
- Astenia
- Espasmos musculares
- Mareos
- Sinusitis
- Dolor de cabeza
- Deshidratación
- Dispepsia (indigestión)
- Petequias
- Artralgia
- Epistaxis (hemorragia nasal)
Frecuentes (del 1 al 10 %):
- Hemorragia (grado 3/4)
- Malignidades primarias secundarias
Recaída en tratamiento con Ibrutinib
El tratamiento de la LLC con ibrutinib ha supuesto un cambio de paradigma ya que las recaídas han sido infrecuentes, no obstante, éstas se han producido y pueden ser debidas a las mutaciones en BTK y PLCG2 si bien los datos son todavía limitados.[19][20]
Tratamiento después de la suspensión de Ibrutinib
Cuando es necesario suspender el tratamiento con Ibrutinib el tratamiento posterior resulta difícil en la mayoría de los pacientes refractarios con recaída con LLC.[21] La incorporación de nuevos fármacos (acalabrutinib y venetoclax) al tratamiento de la leucemia linfática crónica, el linfoma de células de manto y el Macroglobulinemia de Waldenstrom puede ser útil para los enfermos que tengan que discontinuar el tratamiento con ibrutinib y también como alternativa inicial.[22]
Historia del Ibrutinib
Desarrollo de Ibrutinib - PCI-32765
Ibrutinib, de Pharmacyclics Inc. y Johnson & Johnson's Janssen Pharmaceutical, fue diseñado y sintetizado en Celera Genomics por Zhengying Pan, quien junto a un equipo de químicos y biólogos diseñaron en 2007 la estructura para la creación de una serie de pequeñas moléculas que inactivan la tirosina kinasa de Bruton (BTK) mediante la unión covalente de cisteína-481 cerca del dominio de unión a ATP de la BTK. Estas pequeñas moléculas inhibieron irreversiblemente la BTK mediante el uso de un aceptor de Michael para unirse a la cisteína de destino. En abril de 2006, Pharmacyclics adquirió todo el programa de descubrimiento y desarrollo de Celera Genomics sobre el inhibidor de BTK inhibidor, que incluía el compuesto denominado PCI-32765 (conocido como compuesto 13 inicialmente) y que posteriormente fue elegido para un mayor desarrollo preclínico basado en el descubrimiento de sus propiedades en vivo frente al linfoma. Desde 2006, los científicos de Pharmacyclics habían probado la molécula en varios ensayos clínicos donde se identificaron varias indicaciones clínicas específicas para el fármaco.[23][6][7][24][25][26][27]
Aprobación para su uso médico en LCM y LLC
La FDA aprobó su uso para el tratamiento del linfoma de células de manto (LCM),[17][28] la leucemia linfática crónica[4] y para la leucemia linfática crónica (LLC).[29]
El Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamento (EMA), en julio de 2014, emitió un comunicado en el que recomendandaba la concesión de una autorización de comercialización de ibrutinib (Imbruvica) destinado para el tratamiento recidivante del linfoma de células de manto refractario (MCL) y la leucemia linfocítica crónica (CLL).[30]
En 2018 se aprobó la ampliación del uso en Europa para los pacientes con leucemia linfocítica crónica (LLC) sin tratamiento previo —tratamiento de primera línea—.[31] En España se aprobó su aplicación para pacientes sin tratamiento en enero de 2018.[32] La ampliación del tratamiento con ibrutinib a primera línea se basó en los datos del ensayo clínico fase 3, aleatorizado y abierto RESONATE™-2, publicados en The New England Journal of Medicine (NEJM) en 2015.[33]
Ensayos clínicos
Se han realizado numerosos estudios clínicos en distintas fases de Ibrutinib en monoterapia[34] o combinado con otros fármacos (Rituximab, bendamustina, ofatumumab, ciclofosfamida, doxorubicin, vincristina, prednisona y lenalidomida, entre otros).[35][36][37] También se han realizado de Ibrutinib en combinación con venetoclax en pacientes con recidivas[38] y tratados con venetoclax cuando ibrutinib no ha parado la progresión.[39]
Está siendo estudiado para el tratamientos de linfoma linfocítico pequeño, linfoma difuso de células B grandes,[8] mieloma múltiple y macroglobulinemia de Waldenstrom.[40] Tiene potenciales efectos para el tratamiento de la artritis reumatoide (autoinmune).[41][34] Un estudio publicado en 2014 mostró una mayor efectividad de ibrutinib frente a ofatumumab.[42]
Los resultados de un estudio en fase 2 en combinación con ublituximab (anticuerpo monoclona anti-CD20) ha mostrado tasas de respuesta rápidas y altas debiendose definir, en ensayos de fase 3 el beneficio clínico a largo plazo de ublituximab en combinación con ibrutinib (ensayo de fase 3 NCT 02301156).[43]
Toxicidad
La dosis recomendada para el tratamiento de CLL es de 420 mg/día[44] mediante una administración oral de cápsula con agua.
Los inhibidores de la tirosina cinasa, entre ellos el ibrutinib, producen efectos indeseados, fundamentalmente hemorragias y fibrilación auricular, aunque dependiendo de la molécula en distinto grado y gravedad.[45]
Los pacientes deben ser informados que un extra en la dosis del ibrutinib no compensa la dosis omitida. Al estar clasificado como medicamento peligroso, se han de tomar precauciones apropiadas para el manejo y la disposición.
El tratamiento debería ser interrumpido para cualquier grado más alto que el 3 en toxicidad hematológica, neutropenia con infección o fiebre. En la tabla[44] se muestra la modificación de la dosis recomendada para estas toxicidades:
| Primera presencia | volver a empezar con 420 mg/día |
|---|---|
| Segunda presencia | volver a empezar con 280 mg/día |
| Tercera presencia | volver a empezar con 140 mg/día |
| Cuarta presencia | interrumpir tratamiento |
Advertencias y precauciones de empleo
Se debe tener en cuenta la toxicidad, la interacción con otros medicamentos así como otras precauciones en su administración:[46][47]
- Interacción con otros medicamentos
El metabolismo de ibrutinib es principalmente por el CYP3A4,la administración conjunta de inhibidores potentes o moderados del CYP3A4 con ibrutinib puede aumentar su exposición y en consecuencia, aumentar el riesgo de toxicidad.
Por el contrario, la administración conjunta de inductores del CYP3A4 puede reducir la exposición, y en consecuencia, producir un riesgo de falta de eficacia.
Por tanto, en la medida de lo posible, se debe evitar el uso concomitante de ibrutinib con inhibidores/inductores potentes o moderados del CYP3A4 y se debe considerar su administración conjunta únicamente cuando los posibles beneficios sean mayores que los riesgos potenciales.
En el caso de que se tenga que utilizar un inhibidor del CYP3A4, se debe vigilar estrechamente a los paciente por si presentaran signos de toxicidad debidos a ibrutinib. En el caso de que se tenga que utilizar un inductor del CYP3A4, se debe vigilar estrechamente al paciente por si presentara signos de falta de eficacia.[48]
Aunque ibrutinib no tenga contraindicaciones tiene posibles efectos que requieren supervisión como:
- Leucostasis
Se han notificado casos de leucostasis en pacientes tratados con ibrutinib. Un número elevado de linfocitos circulantes (> 400 000/μl) puede aumentar el riesgo. Se debe considerar suspender temporalmente la administración del fármaco.[48]
- Infecciones
En pacientes tratados se han observado infecciones (incluyendo septicemia, septicemia neutropénica, infecciones bacterianas, víricas o fúngicas). La mayor parte de los pacientes con infecciones mortales tenían también neutropenia.[48] El riesgo de infecciones con ibrutinib en relación con los tratamientos de quimioterapia tradicionales sigue siendo alto.[49]
- Citopenias
Se han notificado citopenias (neutropenia, trombocitopenia y anemia) de grado 3 o 4 aparecidas durante el tratamiento. Se debe vigilar el hemograma completo una vez al mes.[48]
- Fibrilación auricular/flutter
Se ha notificado fibrilación auricular y flutter auricular en pacientes tratados con Ibrutinib especialmente en pacientes con factores de riesgo cardíaco, infecciones agudas y antecedentes de fibrilación auricular.[48]
- Efectos sobre el intervalo QT
En un estudio de fase II, las evaluaciones del ECG mostraron que Ibrutinib́ producía una ligera disminución del intervalo QTF (media de 7,5 ms). Aunque no se conoce el mecanismo subyacente ni la relevancia de este hallazgo para la seguridad.[48]
Toxicidad para la reproducción
No debe utilizarse durante el embarazo. No hay datos relativos al uso de ibrutinib en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción.[50]
Polémica por el precio de ibrutinib
El periódico Wall Street Journal publicaba en enero de 2016 que el ibrutinib, un medicamento muy específico, tenía un precio o coste de entre 116.000 y 155.400 dólares estadounidenses (USD) el tratamiento anual en los Estados Unidos. A pesar de los previsibles descuentos y el seguro médico, el precio seguía resultando prohibitivo por lo que algunos pacientes no pueden adquirir el medicamento.[51]
La empresa comercializadora del fármaco, Abbvie, adquirió el fármaco en mayo de 2015 y aseguraba que la proyección de ventas mundiales podría alcanzar la cifra 1000 millones USD en 2016 y 5000 millones en 2020.[51]
Véase también
- Acalabrutinib
- Venetoclax
- Duvelisib
- Ublituximab
Referencias
- «Statement on a Nonproprietary Name Adopted by the USAN Council».
- «FDA Press Release».
- Ibrutinib logra “resultados espectaculares” en leucemia crónica, redacción médica, 9 de diciembre de 2015
- Azvolinsky, PhD, Anna. «FDA Approves Ibrutinib for Chronic Lymphocytic Leukemia». Cancer Network. Archivado desde el original el 22 de febrero de 2014. Consultado el 14 de febrero de 2014.
- Pan, Z; Scheerens, H; Li, SJ; Schultz, BE; Sprengeler, PA; Burrill, LC; Mendonca, RV; Sweeney, MD; Scott, KC; Grothaus, Paul G.; Jeffery, Douglas A.; Spoerke, Jill M.; Honigberg, Lee A.; Young, Peter R.; Dalrymple, Stacie A.; Palmer, James T. (2007). «Discovery of selective irreversible inhibitors for Bruton's tyrosine kinase». ChemMedChem 2 (1): 58-61. PMID 17154430. doi:10.1002/cmdc.200600221.
- «Celera Genomics Announces Sale of Therapeutic Programs to Pharmacyclics». Archivado desde el original el 13 de noviembre de 2013.
- «United States patent 7514444».
- Emerging drug profiles: Bruton tyrosine kinase (BTK) inhibitor ibrutinib (PCI-32765), Burger JA, Buggy JJ., Leuk Lymphoma. 2013 Feb 21
- «Ibrutinib alivia síntomas de enfermedad crónica de injerto contra receptor». Instituto Nacional del Cáncer (U.S.A.). 11 de enero de 2017. Consultado el 11 de septiembre de 2017.
- Burger, Jan A.; O'Brien, Susan (2018). «Evolution of CLL treatment — from chemoimmunotherapy to targeted and individualized therapy». Nature Reviews Clinical Oncology. doi:10.1038/s41571-018-0037-8. Consultado el 22 de mayo de 2018.
- Herman SE, Gordon AL, Hertlein E, Ramanunni A, Zhang X, Jaglowski S, Flynn J, Jones J, Blum KA, Buggy J.J., Hamdy A, Johnson AJ, Byrd JC. (2011) Bruton's tyrosine kinase represents a promising therapeutic target for treatment of chronic lymphocytic leukemia and is effectively targeted by PCI-32765. Blood 117: 6287-6296
- The Bruton's tyrosine kinase (BTK) inhibitor PCI-32765 (P) in treatment-naive (TN) chronic lymphocytic leukemia (CLL) patients (pts): Interim results of a phase Ib II study.J Clin Oncol 30, 2012 (suppl; abstr 6507)
- Ponader S, Chen SS, Buggy JJ, Balakrishnan K, Gandhi V, Wierda WG, Keating MJ, O'Brien S, Chiorazzi N, Burger JA. (2012) The Bruton tyrosine kinase inhibitor PCI-32765 thwarts chronic lymphocytic leukemia cell survival and tissue homing in vitro and in vivo. Blood 119: 1182-1189.
- de Rooij MF, Kuil A, Geest CR, Eldering E, Chang BY, Buggy JJ, Pals ST, Spaargaren M. (2012) The clinically active BTK inhibitor PCI-32765 targets B-cell receptor (BCR)- and chemokine-controlled adhesion and migration in chronic lymphocytic leukemia. Blood 119: 2590-2594.
- Ponader S, Chen SS, Buggy JJ, Balakrishnan K, Gandhi V, Wierda WG, Keating MJ, O'Brien S, Chiorazzi N, Burger JA (2012). The Bruton tyrosine kinase inhibitor PCI-32765 thwarts chronic lymphocytic leukemia cell survival and tissue homing in vitro and in vivo 119. Blood. pp. 1182-1189.
- de Rooij MF, Kuil A, Geest CR, Eldering E, Chang BY, Buggy JJ, Pals ST, Spaargaren M (2012). «The clinically active BTK inhibitor PCI-32765 targets B-cell receptor (BCR)- and chemokine-controlled adhesion and migration in chronic lymphocytic leukemia». Blood 2012: 2590-2594.
- «Imbruvica (Ibrutinib)». Medscape Reference. WebMD. Consultado el 13 de enero de 2014.
- «IMBRUVICA (ibrutinib) capsule [Pharmacyclics, Inc]». DailyMed. Pharmacyclics, Inc. noviembre de 2013. Consultado el 13 de enero de 2013.
- BTKC481S - Mediated Resistance to Ibrutinib in Chronic Lymphocytic Leukemia, DOI: 10.1200/JCO.2016.70.2282 Journal of Clinical Oncology 35, no. 13 (May 2017) 1437-1443. PMID 28418267
- Clonal evolution leading to ibrutinib resistance in chronic lymphocytic leukemia, Blood 2017 129:1469-1479; doi: https://doi.org/10.1182/blood-2016-06-719294
- Outcomes of patients with chronic lymphocytic leukemia (CLL) after discontinuing ibrutinib, january 8, 2015, Blood -
- Dos fármacos muestran eficacia contra una forma común de leucemia, Instituto Nacional del Cáncer -cancer.gov-, 5 de enero de 2016
- Pan, Z; Scheerens, H; Li, SJ; Schultz, BE; Sprengeler, PA; Burrill, LC; Mendonca, RV; Sweeney, MD et al. (2007). «Discovery of selective irreversible inhibitors for Bruton's tyrosine kinase». ChemMedChem 2 (1): 58-61. PMID 17154430. doi:10.1002/cmdc.200600221.
- Honigberg, LA; Smith, AM; Sirisawad, M; Verner, E; Loury, D; Chang, B; Li, S; Pan, Z; Thamm, DH; Miller, RA; Buggy, JJ (2010). «The Bruton tyrosine kinase inhibitor PCI-32765 blocks B-cell activation and is efficacious in models of autoimmune disease and B-cell malignancy». Proceedings of the National Academy of Sciences of the United States of America 107 (29): 13075-80. PMID 20615965. doi:10.1073/pnas.1004594107.
- «Janssen Biotech, Inc. Announces Collaborative Development and Worldwide License Agreement for Investigational Anti-Cancer Drug, PCI-32765».
- «Clinical trials involve PCI-32765».
- «Clinical trials involve ibrutinib».
- «Imbruvica MCL - For previously treated MCL».
- «Imbruvica CLL - For previously treated CLL».
- «Summary of opinion (initial authorisation) Ibrutinib - Imbruvica». EMA - CHMP (EMA/CHMP/414325/2014). julio de 2014.
- La UE amplía el uso de ibrutinib a primera línea de leucemia linfática, redacción médica, 2 de junio de 2016]
- Imbruvica® (ibrutinib) recibe en España la aprobación como tratamiento en primera línea en LLC, medicina21.com, 18 de enero 2018
- Ibrutinib as Initial Therapy for Patients with Chronic Lymphocytic Leukemia, Jan A. Burger, M.D. et al.; December 17, 2015, N Engl J Med 2015; 373:2425-2437 DOI: 10.1056/NEJMoa1509388
- Ibrutinib Receives Third Oncology Breakthrough Therapy Designation from U.S. Food and Drug Administration, febrero de 2013
- «Clinical Trials PCI-32765, en clinicaltrials.gov».
- «Good News Continues for Ibrutinib in CLL. 8 Dec 2012».
- Bruton Tyrosine Kinase Inhibitor Ibrutinib (PCI-32765) Has Significant Activity in Patients With Relapsed/Refractory B-Cell Malignancies, Ranjana H. Advani⇓,Joseph J. Buggy, Jeff P. Sharman, Sonali M. Smith, Thomas E. Boyd, Barbara Grant, Kathryn S. Kolibaba, Richard R. Furman, Sara Rodriguez, Betty Y. Chang, Juthamas Sukbuntherng, Raquel Izumi, Ahmed Hamdy, Eric Hedrick and Nathan H. Fowler, October 8, 2012, doi: 10.1200/JCO.2012.42.7906 JCO January 1, 2013 vol. 31 no. 1 88-94
- Ibrutinib/Venetoclax Combo Impresses in Early CLL Data, 10 de diciembre de 2017
- Venetoclax for chronic lymphocytic leukaemia progressing after ibrutinib: an interim analysis of a multicentre, open-label, phase 2 trial, Jeffrey A Jones et al.; The Lancet, Volume 19, No. 1, p65–75, January 2018
- «Ibrutinib (PCI-32765), BTK-inhibitor – Oncology». www.pharmacyclics.com. Archivado desde el original el 17 de mayo de 2012. Consultado el 19 de mayo de 2012.
- Chang, BY; Huang, MM; Francesco, M; Chen, J; Sokolove, J; Magadala, P; Robinson, WH; Buggy, JJ (2011). «The Bruton tyrosine kinase inhibitor PCI-32765 ameliorates autoimmune arthritis by inhibition of multiple effector cells». Arthritis research & therapy 13 (4): R115. PMID 21752263. doi:10.1186/ar3400.
- Ibrutinib versus Ofatumumab in Previously Treated Chronic Lymphoid Leukemia, NEJM, 2014, 31 de mayo, DOI: 10.1056/NEJMoa1400376
- Ublituximab (TG-1101), a novel glycoengineered anti-CD20 antibody, in combination with ibrutinib is safe and highly active in patients with relapsed and/or refractory chronic lymphocytic leukaemia: results of a phase 2 trial
- Parmar, Sapna; Patel, Khilna; Pinilla-Ibarz, Javier (12 de noviembre de 2016). «Ibrutinib (Imbruvica): A Novel Targeted Therapy for Chronic Lymphocytic Leukemia». Pharmacy and Therapeutics 39 (7): 483-519. ISSN 1052-1372. PMC 4103574. PMID 25083126. Consultado el 12 de noviembre de 2016.
- Alteraciones en la hemostasia inducidas por los nuevos tratamientos antineoplásicos dirigidos a la inhibición de tirosina cinasas José Ramón González Porras, Fermín Sánchez-Guijo, Marcos González, José María BastidaUnidad de Trombosis y Hemostasia. Servicio de Hematología. Hospital Universitario de Salamanca-IBSAL-USAL. Salamanca; en Ponencias y Comunicaciones del XXXIV Congreso Nacional de la SETH · Granada, 2018
- Cancer, Cleveland Clinic. «Ibrutinib | Medicinas para Quimioterapia | Chemocare.com». www.chemocare.com. Consultado el 12 de noviembre de 2016.
- «Ibrutinib: MedlinePlus medicinas». medlineplus.gov. Consultado el 12 de noviembre de 2016.
- «Ficha técnica o resumen de las características del producto». Imbruvica, INN-Ibrutinib- Europa.
- Analysis of the risk of infection in patients with chronic lymphocytic leukemia in the era of novel therapies, AnnaLynn M. Williams et al.; Journal Leukemia & Lymphoma, Volume 59, 2018 - Issue 3
- Germany, gofeminin.de GmbH, 51149 Koeln,. «Efectos secundarios - IBRUTINIB - Onmeda.es». onmeda.es. Consultado el 12 de noviembre de 2016.
- Walker, Joseph (1 de enero de 2016). «Patients Struggle With High Drug Prices: Out-of-pocket costs for pricey new drugs leave even some insured and relatively affluent patients with hard choices on how to afford them». Belleville, Illinois: Wall Street Journal. Consultado el 1 de enero de 2016.
Enlaces externos
- BTK inhibitor PCI-32765, National Cancer Institute Drug Dictionary
- Official Imbruvica patient website
- Ibrutinib (PCI-32765), BTK-inhibitor – Oncology en Pharmacyclis.
- Ibrutinib - Agencia Española de Medicamentos y Productos Sanitarios AEMPS
- Ensayos clínicos
- Clinical Trials PCI-32765, en clinicaltrials.gov
- Ibrutinib - Chronic Lymphocytic Leukemia / Small Lymphocytic Lymphoma - Leucemia linfática crónica / Linfoma linfocítico pequeño
- Ibrutinib - Diffuse Large B-cell Lymphoma - Linfoma difuso de células B grandes
- Ibrutinib - Mantle Cell Lymphoma - Linfoma de células de manto
- Ibrutinibi - Multiple Myeloma - Mieloma múltiple
- Noticias
- 2016 - Ibrutinib desembarca en España con indicación en LLC, LCM y MW, gacetamedica.com, 5 de febrero de 2016
- 2013 - Ibrutinib Receives Third Oncology Breakthrough Therapy Designation from U.S. Food and Drug Administration, febrero de 2013