Serpina
Las serpinas (del inglés, serine protease inhibitors) son una superfamilia de proteínas caracterizadas principalmente por ser inhibidores de proteasa, ampliamente distribuida en los seres vivos ya que se pueden encontrar en todos los eucariotas y en algunos procariotas. Si bien la mayoría de las serpinas tienen la función de inhibir serina proteasas, otras inhiben caspasas, y cisteína proteasas como la papaína. También se encuentran serpinas con otras funciones tales como el transporte de hormonas, chaperonas moleculares o la supresión de tumores.[1][2][3][4][5][6]
| Serpina | ||
|---|---|---|
| Identificadores | ||
| Símbolo | Serpin, SERPIN (root symbol of family) | |
| Pfam | PF00079 | |
| InterPro | IPR000215 | |
| SCOP | 1hle | |
| CDD | cd00172 | |
Estructuras PDB disponibles: 1m37
A:1-378 1hle B:349-379 1jrr A:1-415 1by7 A:1-415 1ova A:1-385 1uhg A:1-385 1jti B:1-385 1att B:77-433 1nq9 L:76-461 1oyh I:76-461 1e03 L:76-461 1e05 I:76-461 1br8 L:76-461 1r1l L:76-461 1lk6 L:76-461 1ant L:76-461 2beh L:76-461 1dzh L:76-461 1ath A:78-461 1tb6 I:76-461 2ant I:76-461p 1dzg I:76-461 1azx L:76-461 1jvq I:76-461 1sr5 A:76-461 1e04 I:76-461 1xqg A:1-375 1xu8 B:1-375 1wz9 B:1-375 1xqj A:1-375 1c8o A:1-300 1m93 A:1-55 1f0c A:1-305 1k9o I:18-392 1sek :18-369 1atu
:45-415
1ezx B:383-415 8api A:43-382 1qmb A:49-376 1iz2 A:43-415 1oo8 A:43-415 1d5s B:378-415 7api A:44-382 1qlp A:43-415 1oph A:43-415 1kct :44-415 2d26
:47-415 1hp7
A:43-415 3caa A:50-383 1qmn A:43-420 4caa B:390-420 2ach A:47-383 1as4 A:48-383 1yxa B:42-417 1lq8 F:376-406 2pai B:374-406 1pai B:374-406 1jmo A:119-496 1jmj A:119-496 1oc0 A:25-402 1dvn A:25-402 1b3k D:25-402 1dvm D:25-402 1a7c A:25-402 1c5g A:25-402 1db2 B:26-402 9pai A:25-402 1lj5 A:25-402 1m6q A:138-498 1jjo D:101-361 1imv A:49-415 | ||
Las serpinas regulan tanto los procesos de formación de coágulos (trombosis) como los de la disolución de ellos (trombólisis), la respuesta inmune, la reparación del tejido conectivo, la apoptosis, el transporte de hormonas, la unión de corticosteroides, la función neuronal y la presión sanguínea.[1][7]
Las serpinas son «inhibidores suicidas» que actúan como carnada para sus serina proteasas objetivos. Este inusual mecanismo de acción consiste en inhibir la proteasa de manera irreversible, puesto que al unirse ambas moléculas son sometidas a un gran cambio conformacional que altera sus sitios activos quedando inactivas en forma permanente.[1][7][8]
Consecuentemente estas proteínas son el objetivo de investigación médica, ya que su cambio conformacional único las vuelve de alto interés biológico estructural y de investigación a cerca del doblaje de proteínas.[9][10]
El mecanismo de cambio conformacional contiene ciertas ventajas, pero también algunas desventajas. Por un lado, las serpinas son vulnerables a mutaciones que pueden resultar en serpinopatías como el doblaje erróneo de las proteínas y la formación de polímeros inactivos de cadenas largas.[11][12] La polimerización de serpinas no solo reduce la cantidad de inhibidores activos sino que también conlleva la acumulación de los polímeros, causando muerte celular y falla de órganos .[10]
Aunque la mayoría de las serpinas controlan las cascadas proteolíticas, algunas proteínas con estructura de serpina no son inhibidores de enzimas, pero realizan diversas funciones como almacenamiento (como en el huevo blanco—ovoalbúmina), transporte como en las proteínas de transporte de hormonas (Globulina fijadora de tiroxina, globulina fijadora de cortisol) y de proteína chaperona(HSP47).[13] El término serpina se usa para describir a estos miembro también, a pesar de su función no inhibitoria ya que están relacionados evolutivamente.[5]
Historia
El acrónimo serpina fue establecido porque las primeras serpinas en ser identificadas actuaban como quimotripsina serina proteasa.
La actividad inhibidora de la proteasa en el plasma de la sangre se reportó por primera vez a finales de 1800,[14] hasta los 50 que las serpinas antitrombina y alfa 1-antitripsina fueron aisladas.[15] la investigación inicial se concentraba en el papel sobre la enfermedad humana: deficiencia de alfa 1-antitripsina que es uno de los desórdenes genéticos más comunes, causa enfisema,[11][16][17] y la deficiencia de antitrombina resulta en trombosis.[18][19]
En la década de los 80, se volvió claro que estos inhibidores eran parte de una superfamilia de proteínas relacionadas entre sí que incluían inhibidores de proteasa (alfa 1-antitrpsina) y no inhibidores (ovalbúlima).[20] Durante el mismo periodo de tiempo, las primeras estructuras de la serpina fueron estudiadas (primero en su conformación relajada y después en la estresada).[21][22] La estructura indicaba que el mecanismo inhibidor involucraba un cambio conformacional inusual y promovía el siguiente punto de enfoque estructural en los estudios de la serpina.[9][22]
Hasta ahora han sido identificadas más de 1000 serpinas incluyendo, 36 proteínas humanas, además de moléculas en todos los reinos.[6][23][24] En los 2000, una nomenclatura sistemática fue introducida para categorizar miembros de la superfamilia de serpinas basado en sus relaciones evolutivas.[5] Las serpinas son, por lo tanto, la superfamilia más grande y diversa de inhibidores de proteasa.[25]
Clasificación
Las serpinas constituyen la familia de inhibidores de proteasas más numerosa y diversa. Se han identificado alrededor de 1500 serpinas en todos los reinos, incluyendo las 36 serpinas humanas. Las serpinas se han clasificado en clados de acuerdo a las similitudes en sus secuencias. Los clados se clasifican de la A a la P, de los cuales los 9 clados de la A a la I representan las serpinas humanas. El gen que los codifica se ha denominado SERPIN, y para efectos de la clasificación de la serina específica, la letra del clado se anota a continuación y finalmente se le agrega el número del gen, por ejemplo, para la alfa 1-antitripsina la identificación es SERPINA1 (serpina del clado A, gen 1).[1][6]
Distribución
Humanos
El genoma humano codifica 9 clados de serpinas, que van desde el clado A (SERPINA) hasta el clado I (SERPINI), incluyendo 29 proteínas de serpina inhibitorias y 7 no inhibitorias.[1]
El sistema usado para nombrar las serpinas humanas está basado en un análisis filogenético de aproximadamente 500 serpinas del 2001, con proteínas llamada serpin XY, donde X es el clado de proteína y Y el número de proteínas dentro de ese clado. Las funciones de las serpinas humanas han sido determinadas por una combinación de estudios bioquímicos, desórdenes humanos genéticos, y modelos de ratones knockout T.
Otros mamíferos
Muchas serpinas de mamíferos han sido identificadas demostrando no tener una ortología obvia que compartir con la contraparte humana de la serpina. Ejemplos incluyen numeroras serpinas de roedores (particularmente algunas de las serpinas de murino intraelular) como también las serpinas uterinas. El término serpina uterina se refiere a los miembros del clado A de serpinas que son codificadas por el gen SERPINA14. Las serpinas uterinas son producidas por el endometrio en un grupo restringido de mamíferos bajo la influencia de progesterona y estrógeno.[116] Probablemente son inhibidores de proteinasa no funcionales y pueden funcionar durante el embarazo para inhibir la respuesta inmune materna contra el zigoto o para participar en el transporte transplacentaria.[117]
Insectos
El genoma de Drosophila melanogaster contiene 29 genes codificadores de serpina. El análisis de la secuencia de aminoácidos ha colocado 14 de estas serpinas en el clado de serpinas Q y 3 serpinas en el clado K con las 12 restantes clasificadas como serpinas huérfanas al no pertenecer a ningún clado.[118] El sistema de clasificación de clados es difícil de usar para Drosophila serpins y en lugar, un sistema de nomenclatura se adoptó basado en la posición de los genes de serpina en los cromosomas de Drosophila. Trece de las serpinas de Drosophila se encuentran como genes aislados en el genoma (incluyendo Serpina-27A,), con las 16 restantes organizadas en 5 agrupaciones de genes que ocurren en las posiciones del cromosoma 28D (2 serpinas), 42D (5 serpinas), 43A (4 serpinas), 77B (3 serpinas) y 88E (2 serpinas).[118][119][120]
Estudios en las serpinas de Drosophila revelan que la Serpina-27A inhibe la proteasa de pascua(la proteasa final en el Nudel) Al igual que su rol central en los patrones embriónicos, la señalización también es importante para la respuesta inmune innata en insectos. Aparentemente, la serpina-27A también funciona para controlar la respuesta inmune de los insectos.[121][122][123][124]
Nemátodos
El genoma del gusano nematodo C. elegans contiene 9 serpinas, de las que ninguna tiene secuencias de señalización y por lo tanto son intracelulares.[125] Sin embargo, solo 5 de estas serpinas parecen funcionas como inhibidores de proteasa.[125] Un, SRP-6, realiza una función protectora y protege contra la ruptura inducida por estrés asociada con calpaína. Además, SRP-6 inhibe las proteasas de cisteían lisosomales liberadas por la ruptura del lisosoma.[126]
Plantas
Las serpinas de las plantas estaban entre los primeros miembros de la superfamilia en ser identificados.[127] Las serpinas de plantas son poderosos inhibidores de proteasas de serina como quimotripsina de mamíferos, in vitro, el ejemplo mejor estudiado siendo la serpina Zx (BSZx), que es capaz de inhibir tripsina y quimotripsina al igual que a diversos factores de coagulación.[128] Sin embargo, parientes cercanos de la proteasa de serina como quimotripsina están ausentes en plantas. El RCL de varias serpinas de grano de trigo y centeno contiene secuencias que repiten poli-Q similares a esas presentes en las proteínas de almacenamiento de prolamina del endoesperma.[129] Ha sido entonces sugerido que las serpinas de las plantas funcionen mejor en inhibir proteasas de insectos o microbios que de otra manera digerirían las proteínas de almacenamiento de granos. Soportando esta hipótesis diferentes serpinas de plantas han sido identificadas en la savia del floema de la calabaza (CmPS-1)[130] y plantas de pepino.[131][132] Aunque se observó una correlación inversa entre la expresión de CmPS-1 y la supervivencia áfida, in vitro más experimentación reveló que el CmPS-1 recombinante no parecía afectar la supervivencia de los insectos.[130]
Roles alternativos y las proteasas objetivo para las serpinas de las plantas han sido propuestos. La serpina Arabidopsis, AtSerpin1 (At1g47710; 3LE2 ), regula el punto de control sobre la muerte celular programada al marcar como objetivo (RD21) la proteasa de cisteína como papaína.[133][134][135] Otras dos serpinas Arabidopsis , AtSRP2 (At2g14540) y AtSRP3 (At1g64030) parecen estar relacionadas con respuestas al daño del ADN.[136]
Hongos
Una sola serpina fungal ha sido caracterizada: celpina de Piromyces spp. cepa E2. Piromyces es géneroode hongo anaeróbico encontrado en el intestino de los rumiantes y es importante para la digestión de plantas. Se predice que la celpina es inhibitoria y contiene dos dominion con terminales-N además del dominio de la serpina.[24] se sugiere que la celpina pueda proteger la celulosoma de proteasas de plantas.[137]
Procariotas
Genes predichos de serpina están distribuidos esporádicamente en procariotas. Estudios In vitro de algunas de las moléculas han revelado que son capaces de inhibir proteasas, y se sugiere que funcionan como inhibidores in vivo. Varias serpinas procariotas se encuentran en extremofilos. En contraste con las serpinas de mamíferos, estas moléculas poseen gran resistencia a la desnaturalización por calor.[138][139] El papel preciso de la mayoría de las serpinas bacterianas permanece sin conocerse, aunque la serpina de Clostridium thermocellum se localiza en la celulosoma. Se considera que el rol de las serpinas asociadas a la celulosoma puedan ser de prevención de la actividad de proteasas no deseadas contra la celulosoma.[137]
Viral
Las serpinas también se expresan en virus como una manera de evitar la defensas inmunes del huésped.[140] En particular, las serpinas se expresan por virus de viruela, incluyendo viruela de la vaca (vaccinia) y viruela del conejo (myxoma), son de interés porque su uso potencial como nueva terapia para desórdenes inmunes e inflamatorios como para terapia de trasplante.[141][142] Serp1 suprime la respuesta inmune innata de TLR y permite la supervivencia del injerto cardiaco en ratas.[141][143] Crma y Serp2 son ambos inhibidores de clases cruzadas y tienen como objetivo tanto proteasas de serina como de cisteína.[144][145] En comparación con su contraparte en mamíferos, las serpinas virales contienen deleciones significativas de elementos de estructura secundaria. Específicamente, el crmA carece de la hélice-D en la misma proporción que las hélices A y E.[146]
Estructura
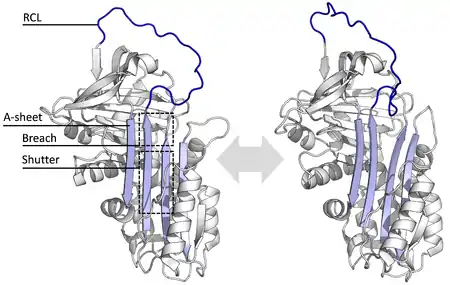
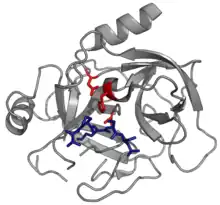
La serpina, en su forma nativa o activa, es una molécula monomérica compuesta por una secuencia de 330 a 550 aminoácidos con una estructura secundaria de hélices y láminas. En la práctica esta molécula puede encontrarse en diferentes estados: activa, latente, dividida, delta y polimérica.[1]
Las diferentes serpinas comparten similitudes en su secuencia que varían entre un 17 a un 95%, sin embargo, su estructura posee secuencias clave comunes que permiten una conformación estable que típicamente está compuesta por tres láminas beta plegadas (denominadas A, B y C) y ocho o nueve hélices alfa (denominadas hA a hI) y un ciclo central reactivo (RCL, por el inglés reactive center loop).[1][149][4]
Las regiones más significantes para la función de la serpina son la plegada-A y su loop de centro reactivo(RCL). La plegada-a incluye dos hebras-β que están en orientación paralela con una región entre ellas llamada 'shutter', y una región arriba llamada 'brecha'. El RCL forma la interacción inicial con la proteasa como objetivo en moléculas inhibidoras. Se han descifrado estructuras mostrando el RCL ya sea totalmente expuesto o parcialmente insertado en la plegada-A, y se piensa que las serpinas están en equilibrio dinámico entre estos dos estados. El RCL también hace interacciones temporales con el resto de la estructura y es por lo tanto sumamente flexible y es expuesto al solvente.[9][21][22]
Las estructuras de serpinas que han sido determinadas, cubren varios tipos diferentes de conformaciones, que han sido necesarias para el entendimiento de su mecanismo de acción de múltiples pasos. La biología estructural ha jugado un papel centrar en el entendimiento de la función y biología de las serpinas.[9]
Función biológica y ubicación
Funciones
La mayoría de las serpinas controlan por inhibición cascadas proteolíticas catalizadas por enzimas proteasas de la familia de las quimotripsinas, mientras que otras no son inhibitorias de otras enzimas sino que realizan funciones variadas, tales como almacenamiento (es el caso de la ovoalbumina), proteínas de transporte hormonal (globulina fijadora de tiroxina, globulina fijadora de cortisol), genes supresores tumorales (como la maspina), regulación de la tensión arterial y desarrollo de linfocitos B, entre muchas otras.[150] Se emplea el término serpina para este tipo de enzimas no inhibitorias, a pesar de su contradictoria función.[151]
Inhibición de la proteasa
La mayoría de las serpinas son inhibidores de proteasa, siendo su objetivo las proteasas de serina como quimotripsina. Estas proteasas poseen un residuo de una serina nucleofílicaMen una tríada catalítica. Algunos ejemplos, incluyen trombina, tripsina y las elastas de neutrófilos humanos.[152] Las serpinas actúan como inhibidores irreversibles y suicidas al atrapar un intermediario del mecanismo catalítico de la proteasa.[153]
Algunas serpinas inhiben otra clase de proteasas, normalmente proteasas de cisteína y se le conoce como inhibidores de clase cruzada. Estas enzimas difieren de la serinaproteasas en que una cisteína nucleofílica en lugar de una serina en su sitio activo.[154] No obstante, la química enzimática es la misma para las dos clases de proteasa.[155] Ejemplos de serpinas inhibidoras de clase cruzada incluyen la serpina B4, un antigen 1 de carcinomas de células escamosas(SCCA-1) y la serpina aviar, una proteína de etapa específica, mieloide y eritoride de terminación nuclear.[63][156][157]
Aproximadamente dos tercios de las serpinas humanas realizan roles extracelulares, inhibiendo proteasas en el flujo sanguíneo para modular sus actividades. Por ejemplo las serpinas extracelulares regulan las cascadas proteicas esenciales para la coagulación de la sangre (antitrombina), las respuestas inmune e inflamatoria (antitripsina, antiquimotripsina y el inhibidor C1) y remodelación de tejido (PAI-1).[13] Al inhibir las proteasas de señalización de cascada, solo pueden afectar el desarrollo. La tabla de serpinas humanas encontrado al final del documento proporciona ejemplos del rango de funciones realizadas por las serpinas humanas al igual que algunas de las enfermedades que resultan de la deficiencia de serpinas.[158][121]
Las proteasas, objetivo de las serpinas inhibiidoras intracelulares han sido difíciles de identificar debido a que varias de estas moléculas parecen realizar tareas que se superponen. Además muchas serpinas humanas carecen de los equivalentes funcionales precisos en organismos modelos como el ratón. Sin embargo, una función importante de las serpinas intracelulares puede ser proteger de la actividad inapropiada de las proteasas dentro de la célula.[159] Por ejemplo, uno de las serpinas mejor caracterizadas es la serpina B9, que inhibe la proteasa de gránulo citotóxico, granzima B. Al hacerlo, la serpina B9 puede proteger contra la liberación inadvertida de granzima B y la activación prematura o no deseada de los mecanismos de muerte celular.[160]
Algunos virus usan serpinas para interrumpir las funciones de las proteasas en su huésped. La serpina viral de la viruela de las vacas CrmA se usa para evitar respuestas inflamatorias y apoptóticas de las células huéspedes infectadas. La CrmA aumenta la infección al suprimir la respuesta inflamatoria del huésped a través de la inhibición de IL-1 y el procesamiento de L-18 por la proteasa de cisteína caspasa-1 .[161] En eucariontes una serpina de planta inhibe metacaspasas y una proteasa de cisteína como papaína[135][133]
Roles no inhibitorios
Las serpinas extracelulares no inhibitorias también realizan un gran conjunto de roles importantes La globulina fijadora de tiroxina y la transcortina transportan las hormonas tiroxina y cortisol respectivamente.[41][43] La serpina de ovalbúlmina, no inhibitoria es la proteína más abundante del huevo blanco. Su función exacta no se conoce, pero se cree que es una proteína de almacenamiento para fetos en desarrollo.[162] La serpina de choque térmico 47 es una chaperona, esencial para del doblaje apropiado del colágeno. Actúa estabilizando la triple hélice del colágeno mientras está siendo procesada en el retículo endoplasmático.[107]
Algunas serpinas son tanto inhibidoras de proteasas y realizan otras tareas. Por ejemplo, el inhibidor nuclear de proteasas de cisteina MENT, en pájaros también actúa como una molécula remodeladora de cromatina en las células rojas de un ave.[156][163]
Cambio conformacional y mecanismo inhibitorio
Las serpinas inhibitorias no inhiben a su objetivo, las proteasas por su típico mecanismo competitivo (candado y llave) usado por la mayoría de los inhibidores de proteasa pequeños ( Kunitz-type inhibitors). En lugar de eso, las serpinas usan un cambio conformacional inusual, el cual altera la estructura de la proteasa y previene que complete la catálisis. El cambio conformacional incluye que el RCL se mueva al extremo contrario de la proteína e insertando una β-plegada A, formando una hebra-β extra antiparalela. Esto convierte a la serpina de un estado estresado a un estado relajado de baja energía(transición de S a R).[9][164]
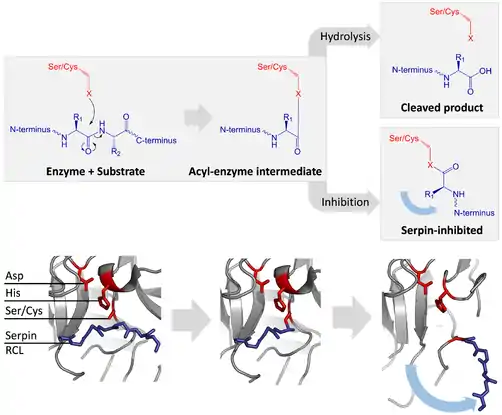
La serpina y las proteasas de cisteína catalizan el rompimiento de un enlace peptídico por un proceso de dos pasos. Inicialmente, los residuos catalíticos del sitio activo de la tríada realiza un ataque nucleofílico en el enlace peptídico del sustrato, esto libera las nuevas terminales-N y forma un enlace de éster covalente entre la enzima y el sustrato. Este complejo covalente entre la enzima y el sustrato se llama un intermediario acil-enzima. Para sustratos estándares, el puente de éster es hidrolizado y una nueva terminal-C se libera para completar la catálisis. Sin embargo, cuando una serpina es separada por una proteasa, rápidamente atraviesa una transición de S a R antes de que el intermediario acil-enzima sea hidrolizado. La eficiencia de la inhibición depende del hecho que la velocidad cinética relativa del cambio conformacional sea varios órdenes de magnitud más rápida que la hidrólisis de la proteasa.
Ya que el RCL está atado todavía covalentemente a la proteasa por el enlace de éster, la transición de S a R, toma a la proteasa de la cima al fondo de la serpina y distorsiona la tríada catalítica. La proteasa distorsionada solo puede hidrolizar el intermediarios acil-anzima extremadamente despacio, y entonces la proteasa permanece covalentemente unida desde días hasta semanas.[153] Las serpinas se clasifican como inhibidores irreversibles y como inhibidores suicidas ya que cada proteína de serpina inactiva permanentemente una sola proteasa y solo puede funcionar una vez.[2]
.png.webp)
Activación alostérica
.png.webp)
La movilidad conformacional de las serpinas proporciona una ventaja clave sobre los inhibidores de proteasa de candado y llave.[87] En particular, la función de serpinas inhibitorias puede ser regulada por interacciones alostéricas con los factores específicos. Las estructuras cristalinas en rayos X de la antitrombina, el cofacto heparina II, MENT y la antiquimotripsina revelan que estas serpinas adoptan una conformación cuando en los primeros dos aminoácidos del RCL, están insertadas las β-plegadas A. La conformación parcialmente insertada es importante porque los cofactores pueden cambiar conformacionalmente ciertas serpinas insertadas parcialmente en una forma completamente expulsada.[165][166] Este arreglo confromacional hace a la serpina un inhibidor más eficiente.
El ejemplo arquetípico de esta situación es la antitrombina, que circula en el plasma en un estado relativamente inactivo al estar parcialmente insertado. Un ejemplo de esta situación es la antitrombina, que circula en el plasma en un estado parcialmente inactivo parcialmente inactivo. Lo primero que se determina es que el residuo (de arginina P1) apunta hacia el cuerpo de la serpina y no está disponible para la proteasa. Después de unirse, una secuencia de pentasacáridos de gran afinidad en una cadena larga de heparina, la antitrombina sufre un cambio conformacional, la expulsión del RCL, y la exposición de la arginina P1. La heparina de pentasacáridos de antitrombina es, entonces un inhibidor más eficiente de la trombina y factor Xa.[167][168] Además, las proteasas de coagulación también contienen sitio de unión (llamados exositios) para la heparina. La heparina, por lo tanto, también actúa como un templados para la unión de ambas, la proteasa y la serpina, acelerando dramáticamente la interacción entre las dos entidades. Después de la interacción inicial, el complejo final de la serpina se forma y la mitad de la heparina se libera. Esta interacción es fisiológicamente importante. Por ejemplo después de una herida a la pared de los vasos sanguíneos, la heparina es expuesta y la antitrombina se activa para controlar la respuesta de coagulación. Entender la base molecular de esta interacción permite el desarrollo de Fondaparinux, una forma sintética de heparina pentasacárida usada como un fármaco anticoagulante.[169][170]
Conformación latente
.png.webp)
Ciertas serpinas son sometidas espontáneamente a la transición de S a R sin haber sido cortadas por una proteasa, para formar una conformación denominada como el estado latente. Las serpinas latentes son incapaces de interactuar con proteasas y por lo tanto ya no son inhibidores de proteasa. El cambio conformacional a estado latente no es exactamente lo mismo que la transición de S a R de una serpina cortada. Ya que el RCL, sigue intacto, la primera hebra de la plegada-C tiene que despegarse para permitir la inserción completa del RCL.[171]
La regulación de la transición a estado latente puede actuar como un mecanismo de control en algunas serpinas como en PAI-1. Aunque PAI-1 se produce en la conformación inhibitoria S, se auto.inactiva aal cambiar a estado latente, a menos que se una al cofactor vitronectina.[171] De manera similar, la antitrombina puede convertirse espontáneamente a su estado latente, como un mecanismo de modulación adicional a su activación alostérica con heparina.[172] Finalmente, la terminal-N, una serpina de Thermoanaerobacter tengcongensis, se necesita para asegurar la molécula en su estado nativo inhibitorio. La ruptura de las interacciones hechas por la región de la terminal N resultan es cambios conformacionales espontáneos de la serpina a su conformación latente. .[173][174]
Cambio conformacional en funciones no inhibitorias
Algunas serpinas no inhibitorias también usan el cambio conformacional de la serpina como parte de su función. Por ejemplo, la forma nativa (S) de la globulina fijadora de tiroxina tiene una gran afinidad por la tiroxina, mientras que la forma cortada (R) tiene poca afinidad . De manera similar, la transcortina tiene mayor afinidad por el cortisol cuando está en su estado nativo (S) que cuando está en su estado cortado (R). Entonces, en estas serpinas, el RCL cortado y la transición de S a R se requiere para permitir la liberación de ligandos en lugar de la inhibición de proteasas.[41][43][175]
En algunas serpinas, la transición de S a R puede activar eventos de señalización celular. En estos caso, una serpina que ha formado un complejo con su proteasa objetivo, es reconocida por un receptor. El evento de unión entonces conduce a una disminución de señalización por el receptor.[176] La transición de S a R es usada para alertar células de la presencia de actividad de proteasa.[176] Esto difiere de su mecanismo usual donde, las serpinas afectan la señalización simplemente al inhibir proteasas implicadas en una cascada de señalización.[158][121]
Degradación
Cuando una serpina inhibe una proteasa, forma un complejo permanente que necesita ser eliminado. Para las serpinas extracelulares, los complejos finales de serpina-enzima son rápidamente limpiados de la circulación. Un mecanismo por el que esto ocurre en mamíferos es a través de la proteína relacionada con el receptor de lipoproteínas de baja densidad (LRP) que se une a complejos inhibitorios hechos por la antitrombina, PA1-1, y la neuroserpina, provocando captación celular.[176][177] De manera similar, la serpina de Drosophila se degrada en el lisosoma después de haber sido llevada dentro de la célula por el recpeto Lipoforina 1 (homólogo al recepeto LDL de la familia de mamíferos.[178]
Enfermedad y serpinopatías
Las serpinas son parte de un gran arreglo de funciones fisiológicas, y por lo tanto, las mutaciones en los genes codificándolas pueden causar una serie de enfermedades. Mutaciones que cambian la actividad, la especificidad o propiedades agregadas de las serpinas pueden afectar la manera en que funcionan. La mayoría de las enfermedades relacionadas con las serpinas son el resultado de una polimerización de serpinas en conjuntos, aunque otro tipo de mutaciones ligadas a enfermedades pueden ocurrir.[9][179] El desorden de la deficiencia de α-Antitripsina es una de las enfermedades hereditarias más comunes.[11][17]
Inactividad o ausencia
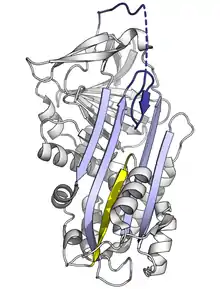
Ya que el doblaje de la serpina estresada es de energía alta, las mutaciones pueden causar que se cambien incorrectamente a conformaciones de baja energía(relajadas o latentes) antes de que realicen correctamente su función inhibitoria.[10]
Las mutaciones que afectan la velocidad o que tanto se inserta el RCL en la plegada-A puede causar que la serpina sufra su cambio conformacional de S a R antes de haber interactuado con una proteasa. Como una serpina solo puede hacer este cambio conformacional una sola vez, la serpina ahora es inactiva e incapaz de controlar apropiadamente a la proteasa.[10][180] De igual manera, las mutaciones que promueven la transición inapropiada hacia el monomérico estado latente causan enfermedades al reducir la cantidad de serpina inhibitoria. Por ejemplo, ambas variantes enfermas de antitrombina wibble y wobble,[181] promueven la formación del estado latente.
La estructura de la antiquimotripsina enferma (L55P) reveló otra, "la conformación- δ" inactiva. En la conformación- δ, se insertan cuatro residuos del RCL en la parte superior de la β-plegada A. La mitad del fondo de la plegada se llena como resultado de una de las α-hélices (hélice F) cambiando parcialmente a una conformación de hebra-β, completando la unión de hidrógeno de la β-plegada.[182] No está claro si otras serpinas pueden adoptar este confórmero y si esta conformación tiene un tarea funcional, pero se especula que la conformación-δ puede ser adoptada por la globulina fijadora de tiroxina durante la liberación de tiroxinas.[43] Las proteínas no inhibitorias relacionadas con las serpinas también pueden causar enfermedades cuando mutan. Por ejemplo la mutaciones en SERPINF1 causan osteogenesis imperfecta tipo VI en humanos.[99]
En la ausencia de la serpina requerida, la proteasa que normalmente regularía está hiperactiva, conduciendo a patologías.[10] Consecuentemente, una simple deficiencia de serpinas (una mutación nula) puede resultar en enfermedad.[183][26]
Cambio de especificidad
En algunos casos raros, un solo cambio en los aminoácidos del RCL de la serpina altera su especificidad y ataca a la proteasa incorrecta. Por ejemplo la mutación de Antitripsina-Pittsburgh (M358R) causa que la serpina α1-antitrypsin inhiba a la trombina causando un desorden de hemorragia.[184]
Polimerización y acumulación
La mayoría de las enfermedades de serpinas se deben a la acumulación de proteínas y se denominan como "serpinopatías".[12][182] Las serpinas son vulnerables a mutaciones que causen enfermedades que promueven la formación de polímeros mal doblados debido a sus estructuras inestables.[182] Serpinpatías bien caracterizadas incluyen la deficiencia de α1-antitropsina, que puede causar enfisema familiial y en algunos casos cirrosis, ciertas formas familiales de trombosis relacionadas con la deficiencia de antritrombina,[11][12][185]
Cada monómero del acumulado de serpinas existe es su conformación inactiva, relajada (con el RCL insertado en la plegada-A). Los polímeros son, por lo tanto, hiperestables a temperatura e incapaces de inhibir proteasas. Las serpinopatías entonces causan patologías similares a otra protepatías (enfermedades de prion) a través de dos mecanismos.[11][12] Primero, la ausencia de serpinas activas resulta en la actividad incontrolable de las proteasas y la destrucción de tejidos. Segundo, los polímeros hiperestables obstruyen el retículo endoplasmático de las células que sintetizan las serpinas, eventualmente resultando en muerte celular y daño de tejidos. En el caso de la deficiencia de antitripsina, los polímeros de antitripsina provocan la muerte de células hepáticas y cirrosis. Dentro de la célula, los polímeros de serpina se remueven lentamente por degradación en el retículo endoplasmático.[186] Sin embargo, los detalles de como los polímeros de serpina causan la muerte celular todavía no se entiende completamente.[11]
Se cree que los polímeros fisiológicos de serpina se forman a través de un cambio de dominio, donde un segmento de una proteína de serpina se inserta en otro.[187] Los cambios de dominio ocurren cuando las mutaciones o los factores ambientales interfieren con las etapas finales del doblaje de la serpina, haciendo que los intermediarios de alta energía se doblen mal.[188] Tanto las estructuras de los dímeros como de los trímeros que sufrieron cambio de dominio han sido resueltas. En el dímero (de antitrombina), el RCL y parte de la plegada-A se incorporan en la plegada-A de otra molécula de serpina.[187] el trímero de dominio cambiado (de antitripsina) forma, a través del intercambio de una región completamente diferente de la estructura, la beta-plegada (con el RCL de cada molécula insertado en su propia plegada-A).[189] También se ha propuesto que las serpinas puedan formar cambios de dominio al insertar el RCL de una proteína en la plegada-A de otra (polimerización de plegada-A).[185][190] Estas estructuras de dímeros y trímeros con cambio de dominio son suficientemente fuertes para ser los componentes de los acumulados de polímeros causantes de enfermedades, pero el mecanismo todavía no es claro.[187][188][189][191]
Estrategias terapéuticas
Varios acercamientos terapéuticos están siendo investigados para tratar la serinpatía más común, la deficiencia de antitripsina.[11] La terapia de aumento de antitripsina es aprobada para la deficiencia severa de antitripsina, relacionada con enfisema pulmonar.[192] En esta terpia, la antitripsina es pruificada del plasma de donadores de sangre y administrada por intravenosa (Prolastin).[11][193] Para tratar la deficiencia severa de antitripsina, el trasplante de pulmones e hígado ha sido efectivo.[11][194] En modelos animales el direccionamiento de genes en células madre pluripotentes inducidas ha sido exitosamente usado para corregir el defecto de polimerización de antitripsina y para restaurar la habilidad del hígado mamífero de secretar antitripsina activa.[195] Pequeñas moléculas también han sido diseñadas que bloquean la polimerización de antitripsina in vitro.[196][197]
Evolución
Las serpinas son la superfamilia de proteínas inhibidoras más grande y más distribuida.[5][25] Se pensaba que estaban restringidas a organismos eucariotes. pero desde entonces, han sido encontradas en bacteria, arquea y algunos virus.[6][23][198] Permanece incierto si los genes procariotes son descendientes de una serpina procariótica ancestral o el producto de una transferencia genética horizontal de eucariontes. La mayoría de las serpinas permanecen a un clado filogenético, si vienen de plantas o animales, indicando que las serpinas intracelulares y extracelulares pueden haberse separado antes de las plantas y los animales.[199] Excepciones incluyen la serpina de choque intracelular de calor HSP47, que es una chaperon esencial para el doblaje apropiado del colágeno y ciclos entre cis-Golgi y el retículo endoplasmático.[107]
La inhibición de proteasa es considerada la función ancestral, con miembros no inhibidores resultado de neofuncionamiento evolucionario de la estructura. El cambio conformacional de S a R también ha sido aaptado por algunas serpinas que se unen para regular la afinidad por sus objetivos.[43]
Investigaciones
Como las serpinas controlan procesos celulares tales como la coagulación y la inflamación, son proteínas blanco para investigaciones científicas. Las serpinas también tienen importancia para la genómica estructural y el estudio del plegamiento de proteínas debido a que son capaces de dramáticos y muy únicos cambios en sus estructuras en el proceso de la inhibición enzimática.[200] Esa característica es poco usual, ya que los inhibidores de las proteasas tienden a fusionarse con la sencillez de una llave y su cerradura, con formas moleculares precisas en el sitio activo de la enzima. La desventaja de los mecanismos conformacionales de las serpinas es que las hace susceptibles a mutaciones que causan polímeros de larga cadena que son inactivas.[201][202]
Véase también
Referencias
- Heit, Claire; Jackson, Brian C.; McAndrews, Monica.; Wright, Mathew W.; Thompson, David C.; Silverman, Gary A.; et al (octubre de 2013). «Update of the human and mouse SERPIN gene superfamily» [Actualización de la superfamilia de genes SERPIN humanos y de ratón]. Hum Genomics (en inglés) (BioMed Central) 7 (1): 22. PMC 3880077. PMID 24172014. doi:10.1186/1479-7364-7-22. Consultado el 10 de noviembre de 2018.
- Gatto, Mariele & & & & & (enero de 2013). «Serpins, Immunity and Autoimmunity: Old Molecules,New Functions» [Serpinas, inmunidad y autoinmunidad: moléculas antiguas, funciones nuevas]. Clinic Rev Allerg Immunol (en inglés) (Nueva York: Springer) 45 (2). doi:10.1007/s12016-013-8353-3. Consultado el 10 de noviembre de 2018.
- Silverman, Gary A.; Whisstock, James C.; Bottomley, Stephen P.; Huntington, James A.; Kaiserman, Dion; Luke, Cliff J.; et al (agosto de 2010). «Serpins Flex Their Muscle. PUTTING THE CLAMPS ON PROTEOLYSIS IN DIVERSE BIOLOGICAL SYSTEMS» [Las serpinas flexionan sus músculos. Colocando las pinzas en la proteólisis de diversos sistemas biológicos]. J Biol Chem (en inglés) (American Society for Biochemistry and Molecular Biology) 285 (32): 24299-24305. PMC 2915665. PMID 20498369. doi:10.1074/jbc.R110.112771. Consultado el 7 de noviembre de 2018.
- Law, Ruby H. P.; Zhang, Qingwei; McGowan, Sheena; Buckle, Ashley M.; Silverman, Gary A.; Wong, Wilson; et al (mayo de 2006). «An overview of the serpin superfamily» [Una mirada general a la superfamilia de las serpinas]. Genome Biol (en inglés) (BioMed Central) 7 (5): 216. PMID 16737556. doi:10.1186/gb-2006-7-5-216. Consultado el 7 de noviembre de 2018.
- Silverman GA, Bird PI, Carrell RW, Church FC, Coughlin PB, Gettins PG, Irving JA, Lomas DA, Luke CJ, Moyer RW, Pemberton PA, Remold-O'Donnell E, Salvesen GS, Travis J, Whisstock JC (septiembre de 2001). «The serpins are an expanding superfamily of structurally similar but functionally diverse proteins. Evolution, mechanism of inhibition, novel functions, and a revised nomenclature». The Journal of Biological Chemistry 276 (36): 33293-6. PMID 11435447. doi:10.1074/jbc.R100016200.
- Irving, James A.; Pike, Robert N.; Lesk, Arthur M.; Whisstock, James C. (november de 2000). «Phylogeny of the Serpin Superfamily: Implications of Patterns of Amino Acid Conservation for Structure and Function» [Filogenia de la superfamilia serpina: implicaciones de la conservación del patrón de aminoácidos en la estructura y función]. Genome Res (en inglés) (Cold Spring Harbor Laboratory Press) 10: 1845-1864. ISSN 1549-5469. PMID 11116082. doi:10.1101/gr.147800. Consultado el 10 de noviembre de 2018.
- Chen, Hao; Zheng, Donghang; Davids, Jennifer; Bartee, Mee Yong; Dai, Erbin; Liu, Liying; et al (2011). «Viral Serpin Therapeutics: From Concept to Clinic» [Terapéutica con serpinas virales: del concepto a la clínica]. Methods Enzymol (en inglés) 499: 301-329. PMC 3558843. PMID 21683260. doi:10.1016/B978-0-12-386471-0.00015-8. Consultado el 9 de noviembre de 2018.
- Huntington, James A. (julio de 2011). «Serpin structure, function and dysfunction» [Estructura, función y disfunción de la serpina]. Journal of Thrombosis and Haemostasis (en inglés) (John Wiley & Sons, Inc) 9: 26-34. doi:10.1111/j.1538-7836.2011.04360.x. Consultado el 9 de noviembre de 2018.
- Whisstock JC, Bottomley SP (diciembre de 2006). «Molecular gymnastics: serpin structure, folding and misfolding». Current Opinion in Structural Biology 16 (6): 761-8. PMID 17079131. doi:10.1016/j.sbi.2006.10.005.
- Stein PE, Carrell RW (febrero de 1995). «What do dysfunctional serpins tell us about molecular mobility and disease?». Nature Structural Biology 2 (2): 96-113. PMID 7749926. doi:10.1038/nsb0295-96.
- Janciauskiene SM, Bals R, Koczulla R, Vogelmeier C, Köhnlein T, Welte T (agosto de 2011). «The discovery of α1-antitrypsin and its role in health and disease». Respiratory Medicine 105 (8): 1129-39. PMID 21367592. doi:10.1016/j.rmed.2011.02.002.
- Carrell RW, Lomas DA (julio de 1997). «Conformational disease». Lancet 350 (9071): 134-8. PMID 9228977. doi:10.1016/S0140-6736(97)02073-4.
- Law RH, Zhang Q, McGowan S, Buckle AM, Silverman GA, Wong W, Rosado CJ, Langendorf CG, Pike RN, Bird PI, Whisstock JC (2006). «An overview of the serpin superfamily». Genome Biology 7 (5): 216. PMC 1779521. PMID 16737556. doi:10.1186/gb-2006-7-5-216.
- Fermi, C; Personsi, L (1984). «Untersuchungen uber die enzyme, Vergleichende Studie» [Studies on the enzyme, Comparative study]. Z Hyg Infektionskr (en alemán) (18): 83-89.
- Schultz, H; Guilder, I; Heide, K; Schoenenberger, M; Schwick, G (1955). «Zur Kenntnis der alpha-globulin des menschlichen normal serums» [For knowledge of the alpha - globulin of human normal serums]. Naturforsch (en alemán) (10): 463.
- Laurell CB, Eriksson S (2013). «The electrophoretic α1-globulin pattern of serum in α1-antitrypsin deficiency. 1963». Copd. 10 Suppl 1: 3-8. PMID 23527532. doi:10.3109/15412555.2013.771956.
- de Serres, Frederick J. (1 de noviembre de 2002). «Worldwide Racial and Ethnic Distribution of α-Antitrypsin Deficiency». CHEST Journal 122 (5): 1818-1829. doi:10.1378/chest.122.5.1818.
- Egeberg O (junio de 1965). «Inherited antithrombin deficiency causing thrombophilia». Thrombosis Et Diathesis Haemorrhagica 13: 516-30. PMID 14347873.
- Patnaik MM, Moll S (noviembre de 2008). «Inherited antithrombin deficiency: a review». Haemophilia 14 (6): 1229-39. PMID 19141163. doi:10.1111/j.1365-2516.2008.01830.x.
- Hunt LT, Dayhoff MO (julio de 1980). «A surprising new protein superfamily containing ovalbumin, antithrombin-III, and alpha 1-proteinase inhibitor». Biochemical and Biophysical Research Communications 95 (2): 864-71. PMID 6968211. doi:10.1016/0006-291X(80)90867-0.
- Loebermann H, Tokuoka R, Deisenhofer J, Huber R (agosto de 1984). «Human alpha 1-proteinase inhibitor. Crystal structure analysis of two crystal modifications, molecular model and preliminary analysis of the implications for function». Journal of Molecular Biology 177 (3): 531-57. PMID 6332197. doi:10.1016/0022-2836(84)90298-5.
- Stein PE, Leslie AG, Finch JT, Turnell WG, McLaughlin PJ, Carrell RW (septiembre de 1990). «Crystal structure of ovalbumin as a model for the reactive centre of serpins». Nature 347 (6288): 99-102. PMID 2395463. doi:10.1038/347099a0.
- Irving JA, Steenbakkers PJ, Lesk AM, Op den Camp HJ, Pike RN, Whisstock JC (noviembre de 2002). «Serpins in prokaryotes». Molecular Biology and Evolution 19 (11): 1881-90. PMID 12411597. doi:10.1093/oxfordjournals.molbev.a004012.
- Steenbakkers PJ, Irving JA, Harhangi HR, Swinkels WJ, Akhmanova A, Dijkerman R, Jetten MS, van der Drift C, Whisstock JC, Op den Camp HJ (agosto de 2008). «A serpin in the cellulosome of the anaerobic fungus Piromyces sp. strain E2». Mycological Research 112 (Pt 8): 999-1006. PMID 18539447. doi:10.1016/j.mycres.2008.01.021.
- Rawlings ND, Tolle DP, Barrett AJ (marzo de 2004). «Evolutionary families of peptidase inhibitors». The Biochemical Journal 378 (Pt 3): 705-16. PMC 1224039. PMID 14705960. doi:10.1042/BJ20031825.
- Heit C, Jackson BC, McAndrews M, Wright MW, Thompson DC, Silverman GA, Nebert DW, Vasiliou V (30 de octubre de 2013). «Update of the human and mouse SERPIN gene superfamily». Human Genomics 7: 22. PMC 3880077. PMID 24172014. doi:10.1186/1479-7364-7-22.
- Stoller JK, Aboussouan LS (2005). «Alpha1-antitrypsin deficiency». Lancet 365 (9478): 2225-36. PMID 15978931. doi:10.1016/S0140-6736(05)66781-5.
- Münch J, Ständker L, Adermann K, Schulz A, Schindler M, Chinnadurai R, Pöhlmann S, Chaipan C, Biet T, Peters T, Meyer B, Wilhelm D, Lu H, Jing W, Jiang S, Forssmann WG, Kirchhoff F (abril de 2007). «Discovery and optimization of a natural HIV-1 entry inhibitor targeting the gp41 fusion peptide». Cell 129 (2): 263-75. PMID 17448989. doi:10.1016/j.cell.2007.02.042.
- Gooptu B, Dickens JA, Lomas DA (febrero de 2014). «The molecular and cellular pathology of α₁-antitrypsin deficiency». Trends in Molecular Medicine 20 (2): 116-27. PMID 24374162. doi:10.1016/j.molmed.2013.10.007.
- Seixas S, Suriano G, Carvalho F, Seruca R, Rocha J, Di Rienzo A (febrero de 2007). «Sequence diversity at the proximal 14q32.1 SERPIN subcluster: evidence for natural selection favoring the pseudogenization of SERPINA2». Molecular Biology and Evolution 24 (2): 587-98. PMID 17135331. doi:10.1093/molbev/msl187.
- Kalsheker NA (septiembre de 1996). «Alpha 1-antichymotrypsin». The International Journal of Biochemistry & Cell Biology 28 (9): 961-4. PMID 8930118. doi:10.1016/1357-2725(96)00032-5.
- Santamaria M, Pardo-Saganta A, Alvarez-Asiain L, Di Scala M, Qian C, Prieto J, Avila MA (abril de 2013). «Nuclear α1-antichymotrypsin promotes chromatin condensation and inhibits proliferation of human hepatocellular carcinoma cells». Gastroenterology 144 (4): 818-828.e4. PMID 23295442. doi:10.1053/j.gastro.2012.12.029.
- Zhang S, Janciauskiene S (abril de 2002). «Multi-functional capability of proteins: alpha1-antichymotrypsin and the correlation with Alzheimer's disease». Journal of Alzheimer's Disease 4 (2): 115-22. PMID 12214135.
- Chao J, Stallone JN, Liang YM, Chen LM, Wang DZ, Chao L (julio de 1997). «Kallistatin is a potent new vasodilator». The Journal of Clinical Investigation 100 (1): 11-7. PMC 508159. PMID 9202051. doi:10.1172/JCI119502.
- Miao RQ, Agata J, Chao L, Chao J (noviembre de 2002). «Kallistatin is a new inhibitor of angiogenesis and tumor growth». Blood 100 (9): 3245-52. PMID 12384424. doi:10.1182/blood-2002-01-0185.
- Liu Y, Bledsoe G, Hagiwara M, Shen B, Chao L, Chao J (octubre de 2012). «Depletion of endogenous kallistatin exacerbates renal and cardiovascular oxidative stress, inflammation, and organ remodeling». American Journal of Physiology. Renal Physiology 303 (8): F1230-8. PMID 22811485. doi:10.1152/ajprenal.00257.2012.
- Geiger M (marzo de 2007). «Protein C inhibitor, a serpin with functions in- and outside vascular biology». Thrombosis and Haemostasis 97 (3): 343-7. PMID 17334499. doi:10.1160/th06-09-0488.
- Baumgärtner P, Geiger M, Zieseniss S, Malleier J, Huntington JA, Hochrainer K, Bielek E, Stoeckelhuber M, Lauber K, Scherfeld D, Schwille P, Wäldele K, Beyer K, Engelmann B (noviembre de 2007). «Phosphatidylethanolamine critically supports internalization of cell-penetrating protein C inhibitor». The Journal of Cell Biology 179 (4): 793-804. PMC 2080921. PMID 18025309. doi:10.1083/jcb.200707165.
- Uhrin P, Dewerchin M, Hilpert M, Chrenek P, Schöfer C, Zechmeister-Machhart M, Krönke G, Vales A, Carmeliet P, Binder BR, Geiger M (diciembre de 2000). «Disruption of the protein C inhibitor gene results in impaired spermatogenesis and male infertility». The Journal of Clinical Investigation 106 (12): 1531-9. PMC 381472. PMID 11120760. doi:10.1172/JCI10768.
- Han MH, Hwang SI, Roy DB, Lundgren DH, Price JV, Ousman SS, Fernald GH, Gerlitz B, Robinson WH, Baranzini SE, Grinnell BW, Raine CS, Sobel RA, Han DK, Steinman L (febrero de 2008). «Proteomic analysis of active multiple sclerosis lesions reveals therapeutic targets». Nature 451 (7182): 1076-81. PMID 18278032. doi:10.1038/nature06559.
- Klieber MA, Underhill C, Hammond GL, Muller YA (octubre de 2007). «Corticosteroid-binding globulin, a structural basis for steroid transport and proteinase-triggered release». The Journal of Biological Chemistry 282 (40): 29594-603. PMID 17644521. doi:10.1074/jbc.M705014200.
- Torpy DJ, Ho JT (agosto de 2007). «Corticosteroid-binding globulin gene polymorphisms: clinical implications and links to idiopathic chronic fatigue disorders». Clinical Endocrinology 67 (2): 161-7. PMID 17547679. doi:10.1111/j.1365-2265.2007.02890.x.
- Zhou A, Wei Z, Read RJ, Carrell RW (septiembre de 2006). «Structural mechanism for the carriage and release of thyroxine in the blood». Proceedings of the National Academy of Sciences of the United States of America 103 (36): 13321-6. PMC 1557382. PMID 16938877. doi:10.1073/pnas.0604080103.
- Bartalena L, Robbins J (1992). «Variations in thyroid hormone transport proteins and their clinical implications». Thyroid 2 (3): 237-45. PMID 1422238. doi:10.1089/thy.1992.2.237.
- Persani L (septiembre de 2012). «Clinical review: Central hypothyroidism: pathogenic, diagnostic, and therapeutic challenges». The Journal of Clinical Endocrinology and Metabolism 97 (9): 3068-78. PMID 22851492. doi:10.1210/jc.2012-1616.
- Kumar R, Singh VP, Baker KM (julio de 2007). «The intracellular renin-angiotensin system: a new paradigm». Trends in Endocrinology and Metabolism 18 (5): 208-14. PMID 17509892. doi:10.1016/j.tem.2007.05.001.
- Tanimoto K, Sugiyama F, Goto Y, Ishida J, Takimoto E, Yagami K, Fukamizu A, Murakami K (diciembre de 1994). «Angiotensinogen-deficient mice with hypotension». The Journal of Biological Chemistry 269 (50): 31334-7. PMID 7989296.
- Jeunemaitre X, Gimenez-Roqueplo AP, Célérier J, Corvol P (1999). «Angiotensinogen variants and human hypertension». Current Hypertension Reports 1 (1): 31-41. PMID 10981040. doi:10.1007/s11906-999-0071-0.
- Sethi AA, Nordestgaard BG, Tybjaerg-Hansen A (julio de 2003). «Angiotensinogen gene polymorphism, plasma angiotensinogen, and risk of hypertension and ischemic heart disease: a meta-analysis». Arteriosclerosis, Thrombosis, and Vascular Biology 23 (7): 1269-75. PMID 12805070. doi:10.1161/01.ATV.0000079007.40884.5C.
- Dickson ME, Sigmund CD (julio de 2006). «Genetic basis of hypertension: revisiting angiotensinogen». Hypertension 48 (1): 14-20. PMID 16754793. doi:10.1161/01.HYP.0000227932.13687.60.
- Frazer JK, Jackson DG, Gaillard JP, Lutter M, Liu YJ, Banchereau J, Capra JD, Pascual V (octubre de 2000). «Identification of centerin: a novel human germinal center B cell-restricted serpin». European Journal of Immunology 30 (10): 3039-48. PMID 11069088. doi:10.1002/1521-4141(200010)30:10<3039::AID-IMMU3039>3.0.CO;2-H.
- Paterson MA, Horvath AJ, Pike RN, Coughlin PB (agosto de 2007). «Molecular characterization of centerin, a germinal centre cell serpin». The Biochemical Journal 405 (3): 489-94. PMC 2267310. PMID 17447896. doi:10.1042/BJ20070174.
- Paterson MA, Hosking PS, Coughlin PB (julio de 2008). «Expression of the serpin centerin defines a germinal center phenotype in B-cell lymphomas». American Journal of Clinical Pathology 130 (1): 117-26. PMID 18550480. doi:10.1309/9QKE68QU7B825A3U.
- Ashton-Rickardt PG (abril de 2013). «An emerging role for Serine Protease Inhibitors in T lymphocyte immunity and beyond». Immunology Letters 152 (1): 65-76. PMID 23624075. doi:10.1016/j.imlet.2013.04.004.
- Han X, Fiehler R, Broze GJ (noviembre de 2000). «Characterization of the protein Z-dependent protease inhibitor». Blood 96 (9): 3049-55. PMID 11049983.
- Hida K, Wada J, Eguchi J, Zhang H, Baba M, Seida A, Hashimoto I, Okada T, Yasuhara A, Nakatsuka A, Shikata K, Hourai S, Futami J, Watanabe E, Matsuki Y, Hiramatsu R, Akagi S, Makino H, Kanwar YS (julio de 2005). «Visceral adipose tissue-derived serine protease inhibitor: a unique insulin-sensitizing adipocytokine in obesity». Proceedings of the National Academy of Sciences of the United States of America 102 (30): 10610-5. PMC 1180799. PMID 16030142. doi:10.1073/pnas.0504703102.
- Feng R, Li Y, Wang C, Luo C, Liu L, Chuo F, Li Q, Sun C (octubre de 2014). «Higher vaspin levels in subjects with obesity and type 2 diabetes mellitus: a meta-analysis». Diabetes Research and Clinical Practice 106 (1): 88-94. PMID 25151227. doi:10.1016/j.diabres.2014.07.026.
- Remold-O'Donnell E, Chin J, Alberts M (junio de 1992). «Sequence and molecular characterization of human monocyte/neutrophil elastase inhibitor». Proceedings of the National Academy of Sciences of the United States of America 89 (12): 5635-9. PMC 49347. PMID 1376927. doi:10.1073/pnas.89.12.5635.
- Benarafa C, Priebe GP, Remold-O'Donnell E (agosto de 2007). «The neutrophil serine protease inhibitor serpinb1 preserves lung defense functions in Pseudomonas aeruginosa infection». The Journal of Experimental Medicine 204 (8): 1901-9. PMC 2118684. PMID 17664292. doi:10.1084/jem.20070494.
- Antalis TM, La Linn M, Donnan K, Mateo L, Gardner J, Dickinson JL, Buttigieg K, Suhrbier A (junio de 1998). «The serine proteinase inhibitor (serpin) plasminogen activation inhibitor type 2 protects against viral cytopathic effects by constitutive interferon alpha/beta priming». The Journal of Experimental Medicine 187 (11): 1799-811. PMC 2212304. PMID 9607921. doi:10.1084/jem.187.11.1799.
- Zhao A, Yang Z, Sun R, Grinchuk V, Netzel-Arnett S, Anglin IE, Driesbaugh KH, Notari L, Bohl JA, Madden KB, Urban JF, Antalis TM, Shea-Donohue T (junio de 2013). «SerpinB2 is critical to Th2 immunity against enteric nematode infection». Journal of Immunology 190 (11): 5779-87. PMID 23630350. doi:10.4049/jimmunol.1200293.
- Dougherty KM, Pearson JM, Yang AY, Westrick RJ, Baker MS, Ginsburg D (enero de 1999). «The plasminogen activator inhibitor-2 gene is not required for normal murine development or survival». Proceedings of the National Academy of Sciences of the United States of America 96 (2): 686-91. PMC 15197. PMID 9892694. doi:10.1073/pnas.96.2.686.
- Schick C, Brömme D, Bartuski AJ, Uemura Y, Schechter NM, Silverman GA (noviembre de 1998). «The reactive site loop of the serpin SCCA1 is essential for cysteine proteinase inhibition». Proceedings of the National Academy of Sciences of the United States of America 95 (23): 13465-70. PMC 24842. PMID 9811823. doi:10.1073/pnas.95.23.13465.
- Takeda A, Yamamoto T, Nakamura Y, Takahashi T, Hibino T (febrero de 1995). «Squamous cell carcinoma antigen is a potent inhibitor of cysteine proteinase cathepsin L». FEBS Letters 359 (1): 78-80. PMID 7851535. doi:10.1016/0014-5793(94)01456-b.
- Turato C, Pontisso P (marzo de 2015). «SERPINB3 (serpin peptidase inhibitor, clade B (ovalbumin), member 3)». Atlas of Genetics and Cytogenetics in Oncology and Haematology 19 (3): 202-209. PMC 4430857. PMID 25984243. doi:10.4267/2042/56413.
- Sivaprasad U, Askew DJ, Ericksen MB, Gibson AM, Stier MT, Brandt EB, Bass SA, Daines MO, Chakir J, Stringer KF, Wert SE, Whitsett JA, Le Cras TD, Wills-Karp M, Silverman GA, Khurana Hershey GK (enero de 2011). «A nonredundant role for mouse Serpinb3a in the induction of mucus production in asthma». The Journal of Allergy and Clinical Immunology 127 (1): 254-61, 261.e1-6. PMC 3058372. PMID 21126757. doi:10.1016/j.jaci.2010.10.009.
- Schick C, Kamachi Y, Bartuski AJ, Cataltepe S, Schechter NM, Pemberton PA, Silverman GA (enero de 1997). «Squamous cell carcinoma antigen 2 is a novel serpin that inhibits the chymotrypsin-like proteinases cathepsin G and mast cell chymase». The Journal of Biological Chemistry 272 (3): 1849-55. PMID 8999871. doi:10.1074/jbc.272.3.1849.
- Teoh SS, Whisstock JC, Bird PI (abril de 2010). «Maspin (SERPINB5) is an obligate intracellular serpin». The Journal of Biological Chemistry 285 (14): 10862-9. PMC 2856292. PMID 20123984. doi:10.1074/jbc.M109.073171.
- Zou Z, Anisowicz A, Hendrix MJ, Thor A, Neveu M, Sheng S, Rafidi K, Seftor E, Sager R (enero de 1994). «Maspin, a serpin with tumor-suppressing activity in human mammary epithelial cells». Science 263 (5146): 526-9. PMID 8290962. doi:10.1126/science.8290962.
- Teoh SS, Vieusseux J, Prakash M, Berkowicz S, Luu J, Bird CH, Law RH, Rosado C, Price JT, Whisstock JC, Bird PI (2014). «Maspin is not required for embryonic development or tumour suppression». Nature Communications 5: 3164. PMC 3905777. PMID 24445777. doi:10.1038/ncomms4164.
- Gao F, Shi HY, Daughty C, Cella N, Zhang M (abril de 2004). «Maspin plays an essential role in early embryonic development». Development 131 (7): 1479-89. PMID 14985257. doi:10.1242/dev.01048.
- Scott FL, Hirst CE, Sun J, Bird CH, Bottomley SP, Bird PI (marzo de 1999). «The intracellular serpin proteinase inhibitor 6 is expressed in monocytes and granulocytes and is a potent inhibitor of the azurophilic granule protease, cathepsin G». Blood 93 (6): 2089-97. PMID 10068683.
- Tan J, Prakash MD, Kaiserman D, Bird PI (julio de 2013). «Absence of SERPINB6A causes sensorineural hearing loss with multiple histopathologies in the mouse inner ear». The American Journal of Pathology 183 (1): 49-59. PMID 23669344. doi:10.1016/j.ajpath.2013.03.009.
- Scarff KL, Ung KS, Nandurkar H, Crack PJ, Bird CH, Bird PI (mayo de 2004). «Targeted disruption of SPI3/Serpinb6 does not result in developmental or growth defects, leukocyte dysfunction, or susceptibility to stroke». Molecular and Cellular Biology 24 (9): 4075-82. PMC 387772. PMID 15082799. doi:10.1128/MCB.24.9.4075-4082.2004.
- Naz, Sadaf (2012). Genetics of Nonsyndromic Recessively Inherited Moderate to Severe and Progressive Deafness in Humans. InTech. p. 260. ISBN 978-953-51-0366-0. doi:10.5772/31808.
- Miyata T, Li M, Yu X, Hirayama N (mayo de 2007). «Megsin gene: its genomic analysis, pathobiological functions, and therapeutic perspectives». Current Genomics 8 (3): 203-8. PMC 2435355. PMID 18645605. doi:10.2174/138920207780833856.
- Kubo A (agosto de 2014). «Nagashima-type palmoplantar keratosis: a common Asian type caused by SERPINB7 protease inhibitor deficiency». The Journal of Investigative Dermatology 134 (8): 2076-9. PMID 25029323. doi:10.1038/jid.2014.156.
- Dahlen JR, Jean F, Thomas G, Foster DC, Kisiel W (enero de 1998). «Inhibition of soluble recombinant furin by human proteinase inhibitor 8». The Journal of Biological Chemistry 273 (4): 1851-4. PMID 9442015. doi:10.1074/jbc.273.4.1851.
- Sun J, Bird CH, Sutton V, McDonald L, Coughlin PB, De Jong TA, Trapani JA, Bird PI (noviembre de 1996). «A cytosolic granzyme B inhibitor related to the viral apoptotic regulator cytokine response modifier A is present in cytotoxic lymphocytes». The Journal of Biological Chemistry 271 (44): 27802-9. PMID 8910377. doi:10.1074/jbc.271.44.27802.
- Zhang M, Park SM, Wang Y, Shah R, Liu N, Murmann AE, Wang CR, Peter ME, Ashton-Rickardt PG (abril de 2006). «Serine protease inhibitor 6 protects cytotoxic T cells from self-inflicted injury by ensuring the integrity of cytotoxic granules». Immunity 24 (4): 451-61. PMID 16618603. doi:10.1016/j.immuni.2006.02.002.
- Rizzitelli A, Meuter S, Vega Ramos J, Bird CH, Mintern JD, Mangan MS, Villadangos J, Bird PI (octubre de 2012). «Serpinb9 (Spi6)-deficient mice are impaired in dendritic cell-mediated antigen cross-presentation». Immunology and Cell Biology 90 (9): 841-51. PMID 22801574. doi:10.1038/icb.2012.29.
- Riewald M, Chuang T, Neubauer A, Riess H, Schleef RR (febrero de 1998). «Expression of bomapin, a novel human serpin, in normal/malignant hematopoiesis and in the monocytic cell lines THP-1 and AML-193». Blood 91 (4): 1256-62. PMID 9454755.
- Askew DJ, Cataltepe S, Kumar V, Edwards C, Pace SM, Howarth RN, Pak SC, Askew YS, Brömme D, Luke CJ, Whisstock JC, Silverman GA (agosto de 2007). «SERPINB11 is a new noninhibitory intracellular serpin. Common single nucleotide polymorphisms in the scaffold impair conformational change». The Journal of Biological Chemistry 282 (34): 24948-60. PMID 17562709. doi:10.1074/jbc.M703182200.
- Finno CJ, Stevens C, Young A, Affolter V, Joshi NA, Ramsay S, Bannasch DL (abril de 2015). «SERPINB11 frameshift variant associated with novel hoof specific phenotype in Connemara ponies». PLoS Genetics 11 (4): e1005122. PMID 25875171. doi:10.1371/journal.pgen.1005122.
- Askew YS, Pak SC, Luke CJ, Askew DJ, Cataltepe S, Mills DR, Kato H, Lehoczky J, Dewar K, Birren B, Silverman GA (diciembre de 2001). «SERPINB12 is a novel member of the human ov-serpin family that is widely expressed and inhibits trypsin-like serine proteinases». The Journal of Biological Chemistry 276 (52): 49320-30. PMID 11604408. doi:10.1074/jbc.M108879200.
- Welss T, Sun J, Irving JA, Blum R, Smith AI, Whisstock JC, Pike RN, von Mikecz A, Ruzicka T, Bird PI, Abts HF (junio de 2003). «Hurpin is a selective inhibitor of lysosomal cathepsin L and protects keratinocytes from ultraviolet-induced apoptosis». Biochemistry 42 (24): 7381-9. PMID 12809493. doi:10.1021/bi027307q.
- Huntington JA (agosto de 2006). «Shape-shifting serpins--advantages of a mobile mechanism». Trends in Biochemical Sciences 31 (8): 427-35. PMID 16820297. doi:10.1016/j.tibs.2006.06.005.
- Ishiguro K, Kojima T, Kadomatsu K, Nakayama Y, Takagi A, Suzuki M, Takeda N, Ito M, Yamamoto K, Matsushita T, Kusugami K, Muramatsu T, Saito H (octubre de 2000). «Complete antithrombin deficiency in mice results in embryonic lethality». The Journal of Clinical Investigation 106 (7): 873-8. PMC 517819. PMID 11018075. doi:10.1172/JCI10489.
- Huntington JA (julio de 2011). «Serpin structure, function and dysfunction». Journal of Thrombosis and Haemostasis. 9 Suppl 1: 26-34. PMID 21781239. doi:10.1111/j.1538-7836.2011.04360.x.
- Vicente CP, He L, Pavão MS, Tollefsen DM (diciembre de 2004). «Antithrombotic activity of dermatan sulfate in heparin cofactor II-deficient mice». Blood 104 (13): 3965-70. PMID 15315969. doi:10.1182/blood-2004-02-0598.
- Aihara K, Azuma H, Akaike M, Ikeda Y, Sata M, Takamori N, Yagi S, Iwase T, Sumitomo Y, Kawano H, Yamada T, Fukuda T, Matsumoto T, Sekine K, Sato T, Nakamichi Y, Yamamoto Y, Yoshimura K, Watanabe T, Nakamura T, Oomizu A, Tsukada M, Hayashi H, Sudo T, Kato S, Matsumoto T (junio de 2007). «Strain-dependent embryonic lethality and exaggerated vascular remodeling in heparin cofactor II-deficient mice». The Journal of Clinical Investigation 117 (6): 1514-26. PMC 1878511. PMID 17549254. doi:10.1172/JCI27095.
- Cale JM, Lawrence DA (septiembre de 2007). «Structure-function relationships of plasminogen activator inhibitor-1 and its potential as a therapeutic agent». Current Drug Targets 8 (9): 971-81. PMID 17896949. doi:10.2174/138945007781662337.
- Lino MM, Atanasoski S, Kvajo M, Fayard B, Moreno E, Brenner HR, Suter U, Monard D (abril de 2007). «Mice lacking protease nexin-1 show delayed structural and functional recovery after sciatic nerve crush». The Journal of Neuroscience 27 (14): 3677-85. PMID 17409231. doi:10.1523/JNEUROSCI.0277-07.2007.
- Murer V, Spetz JF, Hengst U, Altrogge LM, de Agostini A, Monard D (marzo de 2001). «Male fertility defects in mice lacking the serine protease inhibitor protease nexin-1». Proceedings of the National Academy of Sciences of the United States of America 98 (6): 3029-33. PMC 30601. PMID 11248026. doi:10.1073/pnas.051630698.
- Lüthi A, Van der Putten H, Botteri FM, Mansuy IM, Meins M, Frey U, Sansig G, Portet C, Schmutz M, Schröder M, Nitsch C, Laurent JP, Monard D (junio de 1997). «Endogenous serine protease inhibitor modulates epileptic activity and hippocampal long-term potentiation». The Journal of Neuroscience 17 (12): 4688-99. PMID 9169529.
- Doll JA, Stellmach VM, Bouck NP, Bergh AR, Lee C, Abramson LP, Cornwell ML, Pins MR, Borensztajn J, Crawford SE (junio de 2003). «Pigment epithelium-derived factor regulates the vasculature and mass of the prostate and pancreas». Nature Medicine 9 (6): 774-80. PMID 12740569. doi:10.1038/nm870.
- Becerra SP, Perez-Mediavilla LA, Weldon JE, Locatelli-Hoops S, Senanayake P, Notari L, Notario V, Hollyfield JG (noviembre de 2008). «Pigment epithelium-derived factor binds to hyaluronan. Mapping of a hyaluronan binding site». The Journal of Biological Chemistry 283 (48): 33310-20. PMC 2586245. PMID 18805795. doi:10.1074/jbc.M801287200.
- Andreu-Agulló C, Morante-Redolat JM, Delgado AC, Fariñas I (diciembre de 2009). «Vascular niche factor PEDF modulates Notch-dependent stemness in the adult subependymal zone». Nature Neuroscience 12 (12): 1514-23. PMID 19898467. doi:10.1038/nn.2437.
- Homan EP, Rauch F, Grafe I, Lietman C, Doll JA, Dawson B, Bertin T, Napierala D, Morello R, Gibbs R, White L, Miki R, Cohn DH, Crawford S, Travers R, Glorieux FH, Lee B (diciembre de 2011). «Mutations in SERPINF1 cause osteogenesis imperfecta type VI». Journal of Bone and Mineral Research 26 (12): 2798-803. PMC 3214246. PMID 21826736. doi:10.1002/jbmr.487.
- Wiman B, Collen D (septiembre de 1979). «On the mechanism of the reaction between human alpha 2-antiplasmin and plasmin». The Journal of Biological Chemistry 254 (18): 9291-7. PMID 158022.
- Lijnen HR, Okada K, Matsuo O, Collen D, Dewerchin M (abril de 1999). «Alpha2-antiplasmin gene deficiency in mice is associated with enhanced fibrinolytic potential without overt bleeding». Blood 93 (7): 2274-81. PMID 10090937.
- Carpenter SL, Mathew P (noviembre de 2008). «Alpha2-antiplasmin and its deficiency: fibrinolysis out of balance». Haemophilia 14 (6): 1250-4. PMID 19141165. doi:10.1111/j.1365-2516.2008.01766.x.
- Favier, R.; Aoki, N.; De Moerloose, P. (1 de julio de 2001). «Congenital α2-plasmin inhibitor deficiencies: a review». British Journal of Haematology 114 (1): 4-10. ISSN 1365-2141. doi:10.1046/j.1365-2141.2001.02845.x.
- Beinrohr L, Harmat V, Dobó J, Lörincz Z, Gál P, Závodszky P (julio de 2007). «C1 inhibitor serpin domain structure reveals the likely mechanism of heparin potentiation and conformational disease». The Journal of Biological Chemistry 282 (29): 21100-9. PMID 17488724. doi:10.1074/jbc.M700841200.
- Mollnes TE, Jokiranta TS, Truedsson L, Nilsson B, Rodriguez de Cordoba S, Kirschfink M (septiembre de 2007). «Complement analysis in the 21st century». Molecular Immunology 44 (16): 3838-49. PMID 17768101. doi:10.1016/j.molimm.2007.06.150.
- Triggianese P, Chimenti MS, Toubi E, Ballanti E, Guarino MD, Perricone C, Perricone R (agosto de 2015). «The autoimmune side of hereditary angioedema: insights on the pathogenesis». Autoimmunity Reviews 14 (8): 665-9. PMID 25827463. doi:10.1016/j.autrev.2015.03.006.
- Mala JG, Rose C (noviembre de 2010). «Interactions of heat shock protein 47 with collagen and the stress response: an unconventional chaperone model?». Life Sciences 87 (19-22): 579-86. PMID 20888348. doi:10.1016/j.lfs.2010.09.024.
- Nagai N, Hosokawa M, Itohara S, Adachi E, Matsushita T, Hosokawa N, Nagata K (septiembre de 2000). «Embryonic lethality of molecular chaperone hsp47 knockout mice is associated with defects in collagen biosynthesis». The Journal of Cell Biology 150 (6): 1499-506. PMC 2150697. PMID 10995453. doi:10.1083/jcb.150.6.1499.
- Marini JC, Reich A, Smith SM (agosto de 2014). «Osteogenesis imperfecta due to mutations in non-collagenous genes: lessons in the biology of bone formation». Current Opinion in Pediatrics 26 (4): 500-7. PMC 4183132. PMID 25007323. doi:10.1097/MOP.0000000000000117.
- Byers PH, Pyott SM (1 de enero de 2012). «Recessively inherited forms of osteogenesis imperfecta». Annual Review of Genetics 46: 475-97. PMID 23145505. doi:10.1146/annurev-genet-110711-155608.
- Osterwalder T, Cinelli P, Baici A, Pennella A, Krueger SR, Schrimpf SP, Meins M, Sonderegger P (enero de 1998). «The axonally secreted serine proteinase inhibitor, neuroserpin, inhibits plasminogen activators and plasmin but not thrombin». The Journal of Biological Chemistry 273 (4): 2312-21. PMID 9442076. doi:10.1074/jbc.273.4.2312.
- Crowther DC (julio de 2002). «Familial conformational diseases and dementias». Human Mutation 20 (1): 1-14. PMID 12112652. doi:10.1002/humu.10100.
- Belorgey D, Hägglöf P, Karlsson-Li S, Lomas DA (1 de marzo de 2007). «Protein misfolding and the serpinopathies». Prion 1 (1): 15-20. PMC 2633702. PMID 19164889. doi:10.4161/pri.1.1.3974.
- Ozaki K, Nagata M, Suzuki M, Fujiwara T, Miyoshi Y, Ishikawa O, Ohigashi H, Imaoka S, Takahashi E, Nakamura Y (julio de 1998). «Isolation and characterization of a novel human pancreas-specific gene, pancpin, that is down-regulated in pancreatic cancer cells». Genes, Chromosomes & Cancer 22 (3): 179-85. PMID 9624529. doi:10.1002/(SICI)1098-2264(199807)22:3<179::AID-GCC3>3.0.CO;2-T.
- Loftus SK, Cannons JL, Incao A, Pak E, Chen A, Zerfas PM, Bryant MA, Biesecker LG, Schwartzberg PL, Pavan WJ (septiembre de 2005). «Acinar cell apoptosis in Serpini2-deficient mice models pancreatic insufficiency». PLoS Genetics 1 (3): e38. PMC 1231717. PMID 16184191. doi:10.1371/journal.pgen.0010038.
- Padua MB, Kowalski AA, Cañas MY, Hansen PJ (febrero de 2010). «The molecular phylogeny of uterine serpins and its relationship to evolution of placentation». FASEB Journal 24 (2): 526-37. PMID 19825977. doi:10.1096/fj.09-138453.
- Padua MB, Hansen PJ (octubre de 2010). «Evolution and function of the uterine serpins (SERPINA14)». American Journal of Reproductive Immunology 64 (4): 265-74. PMID 20678169. doi:10.1111/j.1600-0897.2010.00901.x.
- Reichhart JM (diciembre de 2005). «Tip of another iceberg: Drosophila serpins». Trends in Cell Biology 15 (12): 659-65. PMID 16260136. doi:10.1016/j.tcb.2005.10.001.
- Tang H, Kambris Z, Lemaitre B, Hashimoto C (octubre de 2008). «A serpin that regulates immune melanization in the respiratory system of Drosophila». Developmental Cell 15 (4): 617-26. PMC 2671232. PMID 18854145. doi:10.1016/j.devcel.2008.08.017.
- Scherfer C, Tang H, Kambris Z, Lhocine N, Hashimoto C, Lemaitre B (noviembre de 2008). «Drosophila Serpin-28D regulates hemolymph phenoloxidase activity and adult pigmentation». Developmental Biology 323 (2): 189-96. PMID 18801354. doi:10.1016/j.ydbio.2008.08.030.
- Hashimoto C, Kim DR, Weiss LA, Miller JW, Morisato D (diciembre de 2003). «Spatial regulation of developmental signaling by a serpin». Developmental Cell 5 (6): 945-50. PMID 14667416. doi:10.1016/S1534-5807(03)00338-1.
- Rushlow C (enero de 2004). «Dorsoventral patterning: a serpin pinned down at last». Current Biology 14 (1): R16-8. PMID 14711428. doi:10.1016/j.cub.2003.12.015.
- Ligoxygakis P, Roth S, Reichhart JM (diciembre de 2003). «A serpin regulates dorsal-ventral axis formation in the Drosophila embryo». Current Biology 13 (23): 2097-102. PMID 14654000. doi:10.1016/j.cub.2003.10.062.
- Jiang R, Zhang B, Kurokawa K, So YI, Kim EH, Hwang HO, Lee JH, Shiratsuchi A, Zhang J, Nakanishi Y, Lee HS, Lee BL (octubre de 2011). «93-kDa twin-domain serine protease inhibitor (Serpin) has a regulatory function on the beetle Toll proteolytic signaling cascade». The Journal of Biological Chemistry 286 (40): 35087-95. PMC 3186399. PMID 21862574. doi:10.1074/jbc.M111.277343.
- Pak SC, Kumar V, Tsu C, Luke CJ, Askew YS, Askew DJ, Mills DR, Brömme D, Silverman GA (abril de 2004). «SRP-2 is a cross-class inhibitor that participates in postembryonic development of the nematode Caenorhabditis elegans: initial characterization of the clade L serpins». The Journal of Biological Chemistry 279 (15): 15448-59. PMID 14739286. doi:10.1074/jbc.M400261200.
- Hejgaard J, Rasmussen SK, Brandt A, SvendsenI (1985). «Sequence homology between barley endosperm protein Z and protease inhibitors of the alpha-1-antitrypsin family». FEBS Lett. 180 (1): 89-94. doi:10.1016/0014-5793(85)80238-6.
- Dahl SW, Rasmussen SK, Petersen LC, Hejgaard J (septiembre de 1996). «Inhibition of coagulation factors by recombinant barley serpin BSZx». FEBS Letters 394 (2): 165-8. PMID 8843156. doi:10.1016/0014-5793(96)00940-4.
- Ostergaard H, Rasmussen SK, Roberts TH, Hejgaard J (octubre de 2000). «Inhibitory serpins from wheat grain with reactive centers resembling glutamine-rich repeats of prolamin storage proteins. Cloning and characterization of five major molecular forms». The Journal of Biological Chemistry 275 (43): 33272-9. PMID 10874043. doi:10.1074/jbc.M004633200.
- Yoo BC, Aoki K, Xiang Y, Campbell LR, Hull RJ, Xoconostle-Cázares B, Monzer J, Lee JY, Ullman DE, Lucas WJ (noviembre de 2000). «Characterization of cucurbita maxima phloem serpin-1 (CmPS-1). A developmentally regulated elastase inhibitor». The Journal of Biological Chemistry 275 (45): 35122-8. PMID 10960478. doi:10.1074/jbc.M006060200.
- la Cour Petersen M, Hejgaard J, Thompson GA, Schulz A (diciembre de 2005). «Cucurbit phloem serpins are graft-transmissible and appear to be resistant to turnover in the sieve element-companion cell complex». Journal of Experimental Botany 56 (422): 3111-20. PMID 16246856. doi:10.1093/jxb/eri308.
- Roberts TH, Hejgaard J (febrero de 2008). «Serpins in plants and green algae». Functional & Integrative Genomics 8 (1): 1-27. PMID 18060440. doi:10.1007/s10142-007-0059-2.
- Lampl N, Budai-Hadrian O, Davydov O, Joss TV, Harrop SJ, Curmi PM, Roberts TH, Fluhr R (abril de 2010). «Arabidopsis AtSerpin1, crystal structure and in vivo interaction with its target protease responsive to desiccation (RD21)». The Journal of Biological Chemistry 285 (18): 13550-60. PMC 2859516. PMID 20181955. doi:10.1074/jbc.M109.095075.
- Lampl N, Alkan N, Davydov O, Fluhr R (mayo de 2013). «Set-point control of RD21 protease activity by AtSerpin1 controls cell death in Arabidopsis». The Plant Journal 74 (3): 498-510. PMID 23398119. doi:10.1111/tpj.12141.
- Vercammen D, Belenghi B, van de Cotte B, Beunens T, Gavigan JA, De Rycke R, Brackenier A, Inzé D, Harris JL, Van Breusegem F (diciembre de 2006). «Serpin1 of Arabidopsis thaliana is a suicide inhibitor for metacaspase 9». Journal of Molecular Biology 364 (4): 625-36. PMID 17028019. doi:10.1016/j.jmb.2006.09.010.
- Ahn JW, Atwell BJ, Roberts TH (2009). «Serpin genes AtSRP2 and AtSRP3 are required for normal growth sensitivity to a DNA alkylating agent in Arabidopsis». BMC Plant Biology 9: 52. PMC 2689219. PMID 19426562. doi:10.1186/1471-2229-9-52.
- Kang S, Barak Y, Lamed R, Bayer EA, Morrison M (junio de 2006). «The functional repertoire of prokaryote cellulosomes includes the serpin superfamily of serine proteinase inhibitors». Molecular Microbiology 60 (6): 1344-54. PMID 16796673. doi:10.1111/j.1365-2958.2006.05182.x.
- Irving JA, Cabrita LD, Rossjohn J, Pike RN, Bottomley SP, Whisstock JC (abril de 2003). «The 1.5 A crystal structure of a prokaryote serpin: controlling conformational change in a heated environment». Structure 11 (4): 387-97. PMID 12679017. doi:10.1016/S0969-2126(03)00057-1.
- Fulton KF, Buckle AM, Cabrita LD, Irving JA, Butcher RE, Smith I, Reeve S, Lesk AM, Bottomley SP, Rossjohn J, Whisstock JC (marzo de 2005). «The high resolution crystal structure of a native thermostable serpin reveals the complex mechanism underpinning the stressed to relaxed transition». The Journal of Biological Chemistry 280 (9): 8435-42. PMID 15590653. doi:10.1074/jbc.M410206200.
- Turner PC, Moyer RW (septiembre de 2002). «Poxvirus immune modulators: functional insights from animal models». Virus Research 88 (1-2): 35-53. PMID 12297326. doi:10.1016/S0168-1702(02)00119-3.
- Richardson J, Viswanathan K, Lucas A (2006). «Serpins, the vasculature, and viral therapeutics». Frontiers in Bioscience 11: 1042-56. PMID 16146796. doi:10.2741/1862.
- Jiang J, Arp J, Kubelik D, Zassoko R, Liu W, Wise Y, Macaulay C, Garcia B, McFadden G, Lucas AR, Wang H (noviembre de 2007). «Induction of indefinite cardiac allograft survival correlates with toll-like receptor 2 and 4 downregulation after serine protease inhibitor-1 (Serp-1) treatment». Transplantation 84 (9): 1158-67. PMID 17998872. doi:10.1097/01.tp.0000286099.50532.b0. (requiere suscripción).
- Dai E, Guan H, Liu L, Little S, McFadden G, Vaziri S, Cao H, Ivanova IA, Bocksch L, Lucas A (mayo de 2003). «Serp-1, a viral anti-inflammatory serpin, regulates cellular serine proteinase and serpin responses to vascular injury». The Journal of Biological Chemistry 278 (20): 18563-72. PMID 12637546. doi:10.1074/jbc.M209683200.
- Turner PC, Sancho MC, Thoennes SR, Caputo A, Bleackley RC, Moyer RW (agosto de 1999). «Myxoma virus Serp2 is a weak inhibitor of granzyme B and interleukin-1beta-converting enzyme in vitro and unlike CrmA cannot block apoptosis in cowpox virus-infected cells». Journal of Virology 73 (8): 6394-404. PMC 112719. PMID 10400732.
- Munuswamy-Ramanujam G, Khan KA, Lucas AR (diciembre de 2006). «Viral anti-inflammatory reagents: the potential for treatment of arthritic and vasculitic disorders». Endocrine, Metabolic & Immune Disorders Drug Targets 6 (4): 331-43. PMID 17214579. doi:10.2174/187153006779025720.
- Renatus M, Zhou Q, Stennicke HR, Snipas SJ, Turk D, Bankston LA, Liddington RC, Salvesen GS (julio de 2000). «Crystal structure of the apoptotic suppressor CrmA in its cleaved form». Structure 8 (7): 789-97. PMID 10903953. doi:10.1016/S0969-2126(00)00165-9.
- Elliott PR, Lomas DA, Carrell RW, Abrahams JP (agosto de 1996). «Inhibitory conformation of the reactive loop of alpha 1-antitrypsin». Nature Structural Biology 3 (8): 676-81. PMID 8756325. doi:10.1038/nsb0896-676.
- Horvath AJ, Irving JA, Rossjohn J, Law RH, Bottomley SP, Quinsey NS, Pike RN, Coughlin PB, Whisstock JC (diciembre de 2005). «The murine orthologue of human antichymotrypsin: a structural paradigm for clade A3 serpins». The Journal of Biological Chemistry 280 (52): 43168-78. PMID 16141197. doi:10.1074/jbc.M505598200.
- Whisstock, James C.; Silverman, Gary A.; Bird, Phillip I.; Bottomley, Stephen P.; Kaiserman, Dion; Luke, Cliff J.; et al (agosto de 2010). «Serpins Flex Their Muscle II. STRUCTURAL INSIGHTS INTO TARGET PEPTIDASE RECOGNITION, POLYMERIZATION, AND TRANSPORT FUNCTIONS» [Las serpinas flexionan sus músculos. Comprensión estructural en el reconocimiento de dianas, polimerización y funciones de transporte]. J Biol Chem (en inglés) (American Society for Biochemistry and Molecular Biology) 285 (32): 24307-24312. PMC 2915666. PMID 20498368. doi:10.1074/jbc.R110.141408. Consultado el 7 de noviembre de 2018.
- KORIN, Jorge. Antithrombin: 25 years later: A tribute to a long lasting source of knowledge in Hemostasis. Acta Bioquím. Clín. Latinoam. [online]. Jul./Sept. 2006, vol.40, no.3 [cited 19 March 2008], p.299-305. Available from World Wide Web: . ISSN 0325-2957.
- Silverman GA, Bird PI, Carrell RW, Church FC, Coughlin PB, Gettins PG, Irving JA, Lomas DA, Luke CJ, Moyer RW, Pemberton PA, Remold-O'Donnell E, Salvesen GS, Travis J, Whisstock JC. (2001). «'The serpins are an expanding superfamily of structurally similar but functionally diverse proteins. Evolution, mechanism of inhibition, novel functions, and a revised nomenclature.». J Biol Chem 276: 33293-6. PMID 11435447.
- Barrett AJ, Rawlings ND (abril de 1995). «Families and clans of serine peptidases». Archives of Biochemistry and Biophysics 318 (2): 247-50. PMID 7733651. doi:10.1006/abbi.1995.1227.
- Huntington JA, Read RJ, Carrell RW (octubre de 2000). «Structure of a serpin-protease complex shows inhibition by deformation». Nature 407 (6806): 923-6. PMID 11057674. doi:10.1038/35038119.
- Barrett AJ, Rawlings ND (mayo de 2001). «Evolutionary lines of cysteine peptidases». Biological Chemistry 382 (5): 727-33. PMID 11517925. doi:10.1515/BC.2001.088.
- Irving JA, Pike RN, Dai W, Brömme D, Worrall DM, Silverman GA, Coetzer TH, Dennison C, Bottomley SP, Whisstock JC (abril de 2002). «Evidence that serpin architecture intrinsically supports papain-like cysteine protease inhibition: engineering alpha(1)-antitrypsin to inhibit cathepsin proteases». Biochemistry 41 (15): 4998-5004. PMID 11939796. doi:10.1021/bi0159985.
- McGowan S, Buckle AM, Irving JA, Ong PC, Bashtannyk-Puhalovich TA, Kan WT, Henderson KN, Bulynko YA, Popova EY, Smith AI, Bottomley SP, Rossjohn J, Grigoryev SA, Pike RN, Whisstock JC (julio de 2006). «X-ray crystal structure of MENT: evidence for functional loop-sheet polymers in chromatin condensation». The EMBO Journal 25 (13): 3144-55. PMC 1500978. PMID 16810322. doi:10.1038/sj.emboj.7601201.
- Ong PC, McGowan S, Pearce MC, Irving JA, Kan WT, Grigoryev SA, Turk B, Silverman GA, Brix K, Bottomley SP, Whisstock JC, Pike RN (diciembre de 2007). «DNA accelerates the inhibition of human cathepsin V by serpins». The Journal of Biological Chemistry 282 (51): 36980-6. PMID 17923478. doi:10.1074/jbc.M706991200.
- Acosta H, Iliev D, Grahn TH, Gouignard N, Maccarana M, Griesbach J, Herzmann S, Sagha M, Climent M, Pera EM (marzo de 2015). «The serpin PN1 is a feedback regulator of FGF signaling in germ layer and primary axis formation». Development 142 (6): 1146-58. PMID 25758225. doi:10.1242/dev.113886.
- Bird PI (febrero de 1999). «Regulation of pro-apoptotic leucocyte granule serine proteinases by intracellular serpins». Immunology and Cell Biology 77 (1): 47-57. PMID 10101686. doi:10.1046/j.1440-1711.1999.00787.x.
- Bird CH, Sutton VR, Sun J, Hirst CE, Novak A, Kumar S, Trapani JA, Bird PI (noviembre de 1998). «Selective regulation of apoptosis: the cytotoxic lymphocyte serpin proteinase inhibitor 9 protects against granzyme B-mediated apoptosis without perturbing the Fas cell death pathway». Molecular and Cellular Biology 18 (11): 6387-98. PMID 9774654. doi:10.1128/mcb.18.11.6387.
- Ray CA, Black RA, Kronheim SR, Greenstreet TA, Sleath PR, Salvesen GS, Pickup DJ (mayo de 1992). «Viral inhibition of inflammation: cowpox virus encodes an inhibitor of the interleukin-1 beta converting enzyme». Cell 69 (4): 597-604. PMID 1339309. doi:10.1016/0092-8674(92)90223-Y.
- Huntington JA, Stein PE (mayo de 2001). «Structure and properties of ovalbumin». Journal of Chromatography. B, Biomedical Sciences and Applications 756 (1-2): 189-98. PMID 11419711. doi:10.1016/S0378-4347(01)00108-6.
- Grigoryev SA, Bednar J, Woodcock CL (febrero de 1999). «MENT, a heterochromatin protein that mediates higher order chromatin folding, is a new serpin family member». The Journal of Biological Chemistry 274 (9): 5626-36. PMID 10026180. doi:10.1074/jbc.274.9.5626.
- Whisstock JC, Skinner R, Carrell RW, Lesk AM (febrero de 2000). «Conformational changes in serpins: I. The native and cleaved conformations of alpha(1)-antitrypsin». Journal of Molecular Biology 296 (2): 685-99. PMID 10669617. doi:10.1006/jmbi.1999.3520.
- Jin L, Abrahams JP, Skinner R, Petitou M, Pike RN, Carrell RW (diciembre de 1997). «The anticoagulant activation of antithrombin by heparin». Proceedings of the National Academy of Sciences of the United States of America 94 (26): 14683-8. PMC 25092. PMID 9405673. doi:10.1073/pnas.94.26.14683.
- Whisstock JC, Pike RN, Jin L, Skinner R, Pei XY, Carrell RW, Lesk AM (septiembre de 2000). «Conformational changes in serpins: II. The mechanism of activation of antithrombin by heparin». Journal of Molecular Biology 301 (5): 1287-305. PMID 10966821. doi:10.1006/jmbi.2000.3982.
- Li W, Johnson DJ, Esmon CT, Huntington JA (septiembre de 2004). «Structure of the antithrombin-thrombin-heparin ternary complex reveals the antithrombotic mechanism of heparin». Nature Structural & Molecular Biology 11 (9): 857-62. PMID 15311269. doi:10.1038/nsmb811.
- Johnson DJ, Li W, Adams TE, Huntington JA (mayo de 2006). «Antithrombin-S195A factor Xa-heparin structure reveals the allosteric mechanism of antithrombin activation». The EMBO Journal 25 (9): 2029-37. PMC 1456925. PMID 16619025. doi:10.1038/sj.emboj.7601089.
- Walenga JM, Jeske WP, Samama MM, Frapaise FX, Bick RL, Fareed J (marzo de 2002). «Fondaparinux: a synthetic heparin pentasaccharide as a new antithrombotic agent». Expert Opinion on Investigational Drugs 11 (3): 397-407. PMID 11866668. doi:10.1517/13543784.11.3.397.
- Petitou M, van Boeckel CA (junio de 2004). «A synthetic antithrombin III binding pentasaccharide is now a drug! What comes next?». Angewandte Chemie 43 (24): 3118-33. PMID 15199558. doi:10.1002/anie.200300640.
- Lindahl TL, Sigurdardottir O, Wiman B (septiembre de 1989). «Stability of plasminogen activator inhibitor 1 (PAI-1)». Thrombosis and Haemostasis 62 (2): 748-51. PMID 2479113.
- Mushunje A, Evans G, Brennan SO, Carrell RW, Zhou A (diciembre de 2004). «Latent antithrombin and its detection, formation and turnover in the circulation». Journal of Thrombosis and Haemostasis 2 (12): 2170-7. PMID 15613023. doi:10.1111/j.1538-7836.2004.01047.x.
- Zhang Q, Buckle AM, Law RH, Pearce MC, Cabrita LD, Lloyd GJ, Irving JA, Smith AI, Ruzyla K, Rossjohn J, Bottomley SP, Whisstock JC (julio de 2007). «The N terminus of the serpin, tengpin, functions to trap the metastable native state». EMBO Reports 8 (7): 658-63. PMC 1905895. PMID 17557112. doi:10.1038/sj.embor.7400986.
- Zhang Q, Law RH, Bottomley SP, Whisstock JC, Buckle AM (marzo de 2008). «A structural basis for loop C-sheet polymerization in serpins». Journal of Molecular Biology 376 (5): 1348-59. PMID 18234218. doi:10.1016/j.jmb.2007.12.050.
- Pemberton PA, Stein PE, Pepys MB, Potter JM, Carrell RW (noviembre de 1988). «Hormone binding globulins undergo serpin conformational change in inflammation». Nature 336 (6196): 257-8. PMID 3143075. doi:10.1038/336257a0.
- Cao C, Lawrence DA, Li Y, Von Arnim CA, Herz J, Su EJ, Makarova A, Hyman BT, Strickland DK, Zhang L (mayo de 2006). «Endocytic receptor LRP together with tPA and PAI-1 coordinates Mac-1-dependent macrophage migration». The EMBO Journal 25 (9): 1860-70. PMC 1456942. PMID 16601674. doi:10.1038/sj.emboj.7601082.
- Jensen JK, Dolmer K, Gettins PG (julio de 2009). «Specificity of binding of the low density lipoprotein receptor-related protein to different conformational states of the clade E serpins plasminogen activator inhibitor-1 and proteinase nexin-1». The Journal of Biological Chemistry 284 (27): 17989-97. PMC 2709341. PMID 19439404. doi:10.1074/jbc.M109.009530.
- Soukup SF, Culi J, Gubb D (junio de 2009). «Uptake of the necrotic serpin in Drosophila melanogaster via the lipophorin receptor-1». En Rulifson, Eric, ed. PLoS Genetics 5 (6): e1000532. PMC 2694266. PMID 19557185. doi:10.1371/journal.pgen.1000532.
- Kaiserman D, Whisstock JC, Bird PI (1 de enero de 2006). «Mechanisms of serpin dysfunction in disease». Expert Reviews in Molecular Medicine 8 (31): 1-19. PMID 17156576. doi:10.1017/S1462399406000184.
- Hopkins PC, Carrell RW, Stone SR (agosto de 1993). «Effects of mutations in the hinge region of serpins». Biochemistry 32 (30): 7650-7. PMID 8347575. doi:10.1021/bi00081a008.
- Beauchamp NJ, Pike RN, Daly M, Butler L, Makris M, Dafforn TR, Zhou A, Fitton HL, Preston FE, Peake IR, Carrell RW (octubre de 1998). «Antithrombins Wibble and Wobble (T85M/K): archetypal conformational diseases with in vivo latent-transition, thrombosis, and heparin activation». Blood 92 (8): 2696-706. PMID 9763552.
- Gooptu B, Hazes B, Chang WS, Dafforn TR, Carrell RW, Read RJ, Lomas DA (enero de 2000). «Inactive conformation of the serpin alpha(1)-antichymotrypsin indicates two-stage insertion of the reactive loop: implications for inhibitory function and conformational disease». Proceedings of the National Academy of Sciences of the United States of America 97 (1): 67-72. PMC 26617. PMID 10618372. doi:10.1073/pnas.97.1.67.
- Fay WP, Parker AC, Condrey LR, Shapiro AD (julio de 1997). «Human plasminogen activator inhibitor-1 (PAI-1) deficiency: characterization of a large kindred with a null mutation in the PAI-1 gene». Blood 90 (1): 204-8. PMID 9207454.
- Owen MC, Brennan SO, Lewis JH, Carrell RW (septiembre de 1983). «Mutation of antitrypsin to antithrombin. alpha 1-antitrypsin Pittsburgh (358 Met leads to Arg), a fatal bleeding disorder». The New England Journal of Medicine 309 (12): 694-8. PMID 6604220. doi:10.1056/NEJM198309223091203.
- Lomas DA, Evans DL, Finch JT, Carrell RW (junio de 1992). «The mechanism of Z alpha 1-antitrypsin accumulation in the liver». Nature 357 (6379): 605-7. PMID 1608473. doi:10.1038/357605a0.
- Kroeger H, Miranda E, MacLeod I, Pérez J, Crowther DC, Marciniak SJ, Lomas DA (agosto de 2009). «Endoplasmic reticulum-associated degradation (ERAD) and autophagy cooperate to degrade polymerogenic mutant serpins». The Journal of Biological Chemistry 284 (34): 22793-802. PMC 2755687. PMID 19549782. doi:10.1074/jbc.M109.027102.
- Yamasaki M, Li W, Johnson DJ, Huntington JA (octubre de 2008). «Crystal structure of a stable dimer reveals the molecular basis of serpin polymerization». Nature 455 (7217): 1255-8. PMID 18923394. doi:10.1038/nature07394.
- Bottomley SP (octubre de 2011). «The structural diversity in α1-antitrypsin misfolding». EMBO Reports 12 (10): 983-4. PMC 3185355. PMID 21921939. doi:10.1038/embor.2011.187.
- Yamasaki M, Sendall TJ, Pearce MC, Whisstock JC, Huntington JA (octubre de 2011). «Molecular basis of α1-antitrypsin deficiency revealed by the structure of a domain-swapped trimer». EMBO Reports 12 (10): 1011-7. PMC 3185345. PMID 21909074. doi:10.1038/embor.2011.171.
- Chang WS, Whisstock J, Hopkins PC, Lesk AM, Carrell RW, Wardell MR (enero de 1997). «Importance of the release of strand 1C to the polymerization mechanism of inhibitory serpins». Protein Science 6 (1): 89-98. PMC 2143506. PMID 9007980. doi:10.1002/pro.5560060110.
- Miranda E, Pérez J, Ekeowa UI, Hadzic N, Kalsheker N, Gooptu B, Portmann B, Belorgey D, Hill M, Chambers S, Teckman J, Alexander GJ, Marciniak SJ, Lomas DA (septiembre de 2010). «A novel monoclonal antibody to characterize pathogenic polymers in liver disease associated with alpha1-antitrypsin deficiency». Hepatology 52 (3): 1078-88. PMID 20583215. doi:10.1002/hep.23760.
- Sandhaus RA (octubre de 2004). «alpha1-Antitrypsin deficiency . 6: new and emerging treatments for alpha1-antitrypsin deficiency». Thorax 59 (10): 904-9. PMC 1746849. PMID 15454659. doi:10.1136/thx.2003.006551.
- Lewis EC. «Expanding the clinical indications for α(1)-antitrypsin therapy». Molecular Medicine 18 (6): 957-70. PMC 3459478. PMID 22634722. doi:10.2119/molmed.2011.00196. Archivado desde el original el 20 de junio de 2019. Consultado el 17 de junio de 2016.
- Fregonese L, Stolk J (2008). «Hereditary alpha-1-antitrypsin deficiency and its clinical consequences». Orphanet Journal of Rare Diseases 3: 16. PMC 2441617. PMID 18565211. doi:10.1186/1750-1172-3-16.
- Yusa K, Rashid ST, Strick-Marchand H, Varela I, Liu PQ, Paschon DE, Miranda E, Ordóñez A, Hannan NR, Rouhani FJ, Darche S, Alexander G, Marciniak SJ, Fusaki N, Hasegawa M, Holmes MC, Di Santo JP, Lomas DA, Bradley A, Vallier L (octubre de 2011). «Targeted gene correction of α1-antitrypsin deficiency in induced pluripotent stem cells». Nature 478 (7369): 391-4. PMC 3198846. PMID 21993621. doi:10.1038/nature10424.
- Mallya M, Phillips RL, Saldanha SA, Gooptu B, Brown SC, Termine DJ, Shirvani AM, Wu Y, Sifers RN, Abagyan R, Lomas DA (noviembre de 2007). «Small molecules block the polymerization of Z alpha1-antitrypsin and increase the clearance of intracellular aggregates». Journal of Medicinal Chemistry 50 (22): 5357-63. PMC 2631427. PMID 17918823. doi:10.1021/jm070687z.
- Gosai SJ, Kwak JH, Luke CJ, Long OS, King DE, Kovatch KJ, Johnston PA, Shun TY, Lazo JS, Perlmutter DH, Silverman GA, Pak SC (2010). «Automated high-content live animal drug screening using C. elegans expressing the aggregation prone serpin α1-antitrypsin Z». PloS One 5 (11): e15460. PMC 2980495. PMID 21103396. doi:10.1371/journal.pone.0015460.
- Cabrita LD, Irving JA, Pearce MC, Whisstock JC, Bottomley SP (septiembre de 2007). «Aeropin from the extremophile Pyrobaculum aerophilum bypasses the serpin misfolding trap». The Journal of Biological Chemistry 282 (37): 26802-9. PMID 17635906. doi:10.1074/jbc.M705020200.
- Fluhr R, Lampl N, Roberts TH (mayo de 2012). «Serpin protease inhibitors in plant biology». Physiologia Plantarum 145 (1): 95-102. PMID 22085334. doi:10.1111/j.1399-3054.2011.01540.x.
- Huntington J, Read R, Carrell R (2000). «Structure of a serpin-protease complex shows inhibition by deformation». Nature 407 (6806): 923-6. PMID 11057674.
- Carrell RW, Lomas DA. (1997). «Conformational disease.». Lancet. 350 (9071): 134-8. PMID 9228977.
- Lomas DA, Evans DL, Finch JT & Carrell RW (1992). «The mechanism of Z alpha 1-antitrypsin accumulation in the liver». Nature 357: 605-607. PMID 1608473.