Allotropie
L’allotropie[1] (du grec allos autre et tropos manière) est, en chimie, en minéralogie et en science des matériaux, la faculté de certains corps simples d’exister sous plusieurs formes cristallines ou moléculaires différentes[2]. C’est l'équivalent du polymorphisme des corps composés pour ce qui est des différentes formes cristallines (organisation des mêmes atomes dans différentes variétés cristallines) ou de l'isomérie pour ce qui est des différentes formes moléculaires (organisation des mêmes atomes dans une autre molécule). Par exemple, le carbone amorphe, le graphite, le diamant, la lonsdaléite, la chaoite, le fullerène et la nanomousse sont les variétés allotropiques du carbone au sens où ce sont différentes formes cristallines du corps simple correspondant à l'élément chimique carbone. Le dioxygène et le trioxygène (ou ozone) sont également des variétés allotropiques du corps simple correspondant à l'élément chimique oxygène, mais cette fois au sens où ce sont différentes formes moléculaires.
Le concept d’allotropie se réfère uniquement aux différentes formes d’un élément chimique au sein de la même phase ou état de la matière (solide, liquide, gaz). Les changements de phase d'un élément ne sont pas associés, par définition, à un changement de forme allotropique (par exemple l’oxygène liquide et le dioxygène gaz ne sont pas deux formes allotropiques). Pour certains éléments chimiques, les formes allotropiques peuvent exister dans différentes phases ; par exemple, les deux formes allotropiques de l’oxygène, le dioxygène et l’ozone peuvent exister dans les phases solide, liquide et gazeuse.
La notion d’allotropie a été élaborée par le chimiste suédois Jöns Jacob Berzelius.
Différences dans les propriétés physiques des formes allotropiques
Les formes allotropiques d'un élément chimique peuvent souvent avoir des propriétés physiques (couleur, dureté, point de fusion, conductivité électrique, conductivité thermique) et une réactivité chimique différentes, bien qu'elles soient constituées d'atomes identiques. Par exemple le dioxygène est peu réactif (et non toxique) dans des conditions où l'ozone est très réactif (et toxique).
Les transformations d'une forme allotropique d'un élément à une autre sont souvent induites par les changements de pression, de température ou même par une réaction chimique et certaines formes ne sont stables que sous certaines conditions de température et de pression ; par exemple :
- le fer existe sous la forme α au-dessous de 912 °C, sous la forme γ entre 912 et 1 394 °C et sous la forme δ au-dessus ;
- en revanche, le passage du dioxygène à l'ozone est une réaction photochimique qui se déroule dans la haute atmosphère où sont présents des UV suffisamment énergétiques pour produire des atomes O à partir de la molécule O2.
Exemples de formes allotropiques
Typiquement les éléments pouvant former un nombre de liaisons chimiques variable et ceux qui possèdent des facultés de concaténation tendent à avoir le plus grand nombre de formes allotropiques. C'est le cas du soufre qui, avant la découverte récente[Quand ?] des nombreuses formes allotropiques de carbone, détenait le record de variétés allotropiques moléculaire (S8, S2, etc.) et cristallographique (Sα, Sβ, etc.). Le phénomène d'allotropie est typiquement plus visible dans le cas des non-métaux puisqu'il peut être à la fois cristallin et moléculaire. Ce dernier cas n'étant pas possible avec les métaux.
Carbone
Les deux formes allotropiques les plus répandues :
- le diamant est une forme cristalline transparente extrêmement dure avec chaque atome de carbone entouré de quatre liaisons simples dans un arrangement tétraédrique. C'est un isolant électrique mais un excellent conducteur thermique ;
- le graphite est un solide noir mou, conduisant modérément l’électricité. Les atomes de carbone, reliés à trois de leurs voisins par liaison covalente, forment un réseau hexagonal bidimensionnel appelé graphène. L'empilement de ces couches constitue le graphite.
Ainsi que d’autres formes plus rares :
- la lonsdaléite est la forme dite hexagonale du diamant ;
- la chaoite est un allotrope se formant à haute pression ;
- les fullerènes, (dont l'« archétype » est C60) ;
- les nanotubes.
Phosphore
- Phosphore rouge - solide polymérique
- Phosphore blanc - solide cristallin
- Phosphore noir - semi-conducteur, présentant des similitudes avec le graphite.
Oxygène
- Dioxygène, O2 - incolore.
- Ozone, O3 - bleu, obtenu photochimiquement à partir du dioxygène.
Le tétraoxygène, O4 - rouge, et l'octaoxygène, O8 - rouge, parfois mentionnés comme variétés allotropiques de l'oxygène, sont des assemblages de molécules de dioxygène. Ils ne constituent pas une variété allotropique.
Soufre
Le cas du soufre est le plus complexe puisque d'une part la facilité avec laquelle le soufre se concatène lui permet d'exister dans une large variété de molécules de formules Sn et cyclo-Sn. D'autre part, ces différentes molécules cristallisent dans des variétés cristallines différentes[3].
- α-cyclo-S8 (solide) est la forme moléculaire la plus stable jusqu'à 95,3 °C. Elle est constituée de cycle de huit atomes de soufre, et ces molécules cycliques s'agencent dans un certain système cristallographique (noté α).
- β-cyclo-S8 (solide) est la forme moléculaire la plus stable entre 95,3 °C et la température de fusion (entre 112,8 et 115,1 °C, suivant la part de chaque variété allotropique effectivement présente).
- γ-cyclo-S8, forme nacrée, observée dès 1890, par refroidissement lent de soufre chauffé au-delà de 150 °C.
- ε-cyclo-S6, forme rhomboédrique, a été observé dès 1891. Il est formé par réaction d'une solution thiosulfate avec de l'acide chlorhydrique saturée à 0 °C.
- Sn (n = 2-5) sont des molécules peu stables dans les conditions habituelles, mais S2 (équivalent de O2) est une forme stable en phase gazeuse à haute température.
- cyclo-Sn (pour plusieurs autres valeurs de n : 6, 7, 10, 12, 18 ; 20).
- Sμ aussi noté S∞ polymérique, d'aspect caoutchouteux.
- Des variétés appelées caténa-Sn (chaîne, non cyclique) peuvent être synthétisées « à la demande ».
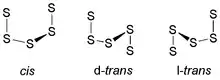
Cette énumération, pourtant longue, cache la complexité des trois conformations possibles des unités S3 se trouvant dans les enchaînements de soufre : cis, d-trans et l-trans (voir figure ci-contre).
Allotropie et diagramme de phase

Le diagramme de phase du corps pur fait apparaître, en plus des états solide, liquide et gaz, les différentes variétés allotropiques dans les zones de température et de pression où elles sont stables. C'est le cas sur le diagramme d'état simplifié du soufre ci-contre.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Allotropy » (voir la liste des auteurs).
- Jöns Jacob Berzelius, Progrès de la Chimie, 1840, t. 5, p. 2.
- (en) « allotropes », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
- (en) Greenwood N.N. et Eanrshaw A (2003), Chemistry of the elements, 2e éd., Elsevier, p. 652.
Voir aussi
- Portail de la chimie
- Portail des sciences des matériaux
- Portail des minéraux et roches
