Facteur induit par l'hypoxie
Les facteurs induits par l’hypoxie (ou HIF, de l'anglais : hypoxia inducible factors) sont des protéines agissant comme facteurs de transcription dans tous les tissus et qui sont régulées par l’absence de dioxygène. D’un point de vue physiologique, l’hypoxie tissulaire est traitée en stimulant la sécrétion de l’hormone érythropoïétine (EPO) qui engendre la production de globules rouges, et, par conséquent, améliore le transport du dioxygène aux tissus cibles. Au niveau moléculaire, ce travail est majoritairement assuré par HIF-1, le complexe le plus actif de la famille des HIFs. Cette protéine a été découverte en 1992 par l'Américain Gregg L. Semenza qui étudiait le gène de l'EPO. En fait, il a découvert une séquence située en position 3’ non codante dans le promoteur de l’EPO, séquence qui porte le nom d'« hypoxia response element » (HRE) et qui fixe la protéine HIF-1 en situation d’hypoxie. La séquence HRE a ensuite été localisée sur plus de 70 autres gènes, tels que le facteur de croissance de l’endothélium vasculaire.
Pour les articles homonymes, voir HIF.
Structure
HIF-1 est un hétérodimère obligatoire[1] qui comprend une composante alpha de 826 acides aminés. On la retrouve constituée de 15 exons, sur le chromosome 14 (14q21-q24). De son côté, la composante bêta contient 789 acides aminés et est située sur le chromosome 1 (1q21). Ces deux unités font partie de la grande famille des facteurs de transcription bHLH-PAS (basic-helix loop helix / Per-ARNT-SIM). Le domaine HLH de la protéine agit sur la dimérisation des deux sous-unités alors que la partie basique intervient dans la fixation et la spécificité de la liaison de la protéine sur l’ADN. La composante bêta est aussi appelée ARNT1, pour « aryl hydrocarbon receptor nuclear translocator » et est exprimée de façon constitutive dans le noyau de la cellule pour la détoxification de celle-ci. Par contre, on retrouve HIF-1α de façon stable, principalement en situation d’hypoxie.
Régulation
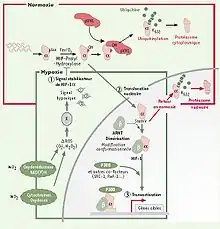
Très instable en normoxie, la sous-unité alpha subit une hydroxylation, par des prolyl-hydroxylases (PHD), dès sa sortie du noyau, puis est liée par la protéine pVHL (von Hippel Lindau protein), une protéine suppresseure de tumeur, qui induit une activité d’ubiquitination, ce qui mène à la dégradation de cette sous-unité alpha par le protéasome cytoplasmique. Cette étape se produit assez rapidement, puisque HIF-α possède une demi-vie de seulement 5 minutes dans le cytoplasme. De plus, la normoxie cellulaire entraîne aussi l'activation de la protéine factor inhibiting HIF-1 (FIH-1)[2] qui agit au niveau du noyau en bloquant la transcription de gènes cibles comme l’EPO. De son côté, la sous-unité bêta est toujours active, sous l’influence du facteur de transcription sp1. En situation d’hypoxie, la sous-unité alpha devient stable, car elle n’est plus hydroxylée par les PHD (son substrat étant le dioxygène), donc elle ne lie plus la protéine pVHL. Elle est alors transportée dans le noyau par translocation nucléaire où elle se liera à la sous-unité bêta ainsi qu’à certains cofacteurs comme le p300/CBP. Le complexe HIF-1 ainsi formé permettra la transcription des gènes cibles, par exemple en se fixant à la séquence HRE sur le promoteur de l’EPO[3]. Finalement, l’hypoxie agit aussi en bloquant l’activité de FIH-1. Lors d’un retour aux conditions normales de dioxygène, les protéines HIF-α se trouvant dans le noyau subiront aussitôt une ubiquitination et seront dégradées par le protéasome nucléaire.
Bien que l’hypoxie soit le principal activateur de HIF-α, il arrive parfois que d’autres inducteurs, tels que l’insuline, les phospholipides, les facteurs de croissance, les cytokines, les epidermal growth factors (EGF) et les insulin-like growth factors-1 (IGF), agissent par des récepteurs couplés à une protéine G en augmentant la transcription de la protéine en situation de normoxie. Ainsi, ce n’est pas toujours l’EPO qui est synthétisé[4], mais bien d’autres protéines comme le VEGF qui augmente l’angiogénèse, aussi lors du développement embryonnaire. C’est pourquoi un déficit en HIF-1 entraîne inévitablement un important retard de développement et souvent, la mort de l’embryon.
Physiopathologie
Des recherches ont mis en évidence l’active participation de HIF-1 dans les tumeurs cancéreuses humaines. Plusieurs mécanismes peuvent être à l’origine de cette surexpression de HIF-1, tel que la création d’une région hypoxique intratumorale qui stabilise HIF-1α et induit le complexe HIF-1 ou bien des mutations par gain de fonction qui activent certains facteurs de croissance induisant aussi la transcription de HIF-1α.
La principale maladie qui occasionne des problèmes au niveau de HIF-1 est la maladie de von Hippel Lindau, qui se définit par une mutation dans le gène de la protéine pVHL. Les personnes atteintes seront hétérozygotes pour l’allèle muté et des tumeurs apparaîtront au niveau de la rétine, des reins ou du système nerveux central. La protéine pVHL n’étant plus là pour inhiber la surexpression de HIF-1α, les tumeurs présentent une grande vascularisation et une forte tendance à créer des métastases.
On sait que dans un cancer la forte prolifération des cellules demande beaucoup d’énergie, et donc de dioxygène, pour progresser. Lorsqu'il y a diminution du dioxygène intratumoral, la protéine HIF-1 aide alors à la création de nouveaux vaisseaux sanguins pour l’apport de dioxygène. Par conséquent, il a été démontré que l’absence de la protéine HIF-1 entraîne une diminution de la prolifération cellulaire, du chimiotactisme, du réarrangement cellulaire et de l’angiogénèse au niveau de la tumeur.
Cible thérapeutique
Le vadadustat[5] et le roxadustat[6] sont des inhibiteurs de la prolyl hydroxylase du HIF, permettant la stabilisation de ce dernier et favorisant la synthèse d'érythropoïétine. Ces traitements pourraient constituer une alternative à l'EPO d'autant que leur administration est faite par voie orale[5].
Références
- (en) Semenza GL, « Hypoxia-inducible factors in physiology and medicine », Cell, vol. 148, no 3, , p. 399-408. (PMID 22304911, PMCID PMC3437543, DOI 10.1016/j.cell.2012.01.021, lire en ligne)
- (en) Kaelin WG Jr, Ratcliffe PJ, « Oxygen sensing by metazoans: the central role of the HIF hydroxylase pathway », Mol Cell, vol. 30, no 4, , p. 393-402. (PMID 18498744, DOI 10.1016/j.molcel.2008.04.009, lire en ligne)
- (en) Bernhardt WM, Wiesener MS, Scigalla P, Chou J, Eckardt K-U et al., « Inhibition of prolyl hydroxylases increases erythropoietin production in ESRD », J Am Soc Nephrol, vol. 21, no 12, , p. 2151-6. (PMID 21115615, PMCID PMC3014028, DOI 10.1681/asn.2010010116, lire en ligne)
- (en) « Regulation of erythropoiesis by hypoxia-inducible factors », Blood Rev, vol. 27, no 1, , p. 41-53. (PMID 23291219, PMCID PMC3731139, DOI 10.1016/j.blre.2012.12.003, lire en ligne)
- (en) Levin A, « Therapy for anemia in chronic kidney disease — New interventions and new questions », N Engl J Med, vol. 384, no 17, , p. 1657-8. (PMID 33913643, DOI 10.1056/nejme2103937)
- (en) Dhillon S, « Roxadustat: first global approval », Drugs, vol. 79, no 5, , p. 563-72. (PMID 30805897, DOI 10.1007/s40265-019-01077-1)
Voir aussi
- Portail de la biologie cellulaire et moléculaire
- Portail de la médecine
- Portail de la physiologie