Fièvre catarrhale
La fièvre catarrhale ovine (FCO), ou maladie de la langue bleue, est une arbovirose due au virus bluetongue (BTV pour BlueTongue Virus) transmis par des moucherons piqueurs du genre Culicoides, à des ruminants surtout domestiques, principalement les moutons, moins souvent les chèvres et les bovidés.
Cette maladie animale à déclaration obligatoire internationale, est répertoriée dans le code sanitaire pour les animaux terrestres de l'OIE. Elle n'est pas contagieuse et non transmissible à l'Homme, mais elle peut être grave pour les espèces de ruminants domestiques sensibles, surtout les races évoluées (par rapport aux rustiques), avec d'importantes répercussions économiques.
D'origine africaine, cette infection est endémique (enzootique) dans la ceinture intertropicale mondiale, où elle reste le plus souvent infraclinique. Des foyers de formes graves surviennent régulièrement, de façon saisonnière, aux limites des zones tempérées nord et sud. Depuis 1998, une extension rapide de la FCO a été constatée au niveau régional, en particulier en Europe. Ce phénomène s’explique probablement par des facteurs climatiques et anthropiques dont l'importance respective est encore mal comprise.
Les moyens de lutte sont fondés sur la surveillance et le contrôle : réactivité devant l'apparition de foyers épidémiques (épizootiques), vaccination des espèces sensibles d’élevage, restrictions imposées aux échanges et aux déplacements d’animaux.
Virus bluetongue
Ne doit pas être confondu avec Fièvre catarrhale maligne.
Pour les articles homonymes, voir FCO.

Histoire
Jusqu'aux années 1920, l'histoire de la maladie de la langue bleue se déroule en Afrique du Sud. Les premières descriptions chez le mouton sont publiées en 1876, mais il est probable que la maladie soit apparue à la fin du XVIIIe siècle, lorsque les moutons européens ont été introduits dans la même région pour un élevage intensif. L'origine virale de la maladie est démontrée en 1905, avec production d'un vaccin vétérinaire utilisé en Afrique du sud jusqu'en 1943. Durant cette période, le rôle de transmission par le moucheron piqueur Culicoides imicola est établi[1].
En 1924, la maladie touche les moutons de Chypre, et ceux des États-Unis dans les années 1950. Elle est reconnue en Méditerranée, en Asie, en Australie et dans toute la zone mondiale intertropicale. Au cours du XXe siècle, un modèle de la FCO s'impose : celui d'une maladie ovine émergente d'origine africaine, liée aux mouvements et au commerce d'animaux vivants, limitée à la zone intertropicale[1].
Au tournant du XXIe siècle, ce modèle est mis à mal par la survenue soudaine d'épizooties majeures en Europe, transmises par d'autres Culicoïdes autochtones, touchant aussi les bovins, et ce jusqu'à plus de 50 ° de latitude nord, ce qui a conduit l'OIE à réviser en 2013 les chapitres concernant la FCO du Code sanitaire pour les animaux terrestres[1],[2].
Agent de la maladie
| Type | Virus |
|---|---|
| Groupe | Groupe III |
| Famille | Reoviridae |
| Genre | Orbivirus |
— auteur incomplet —, date à préciser
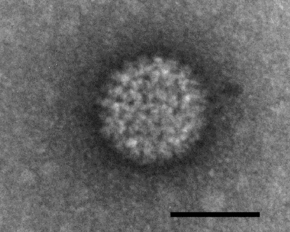
L'agent de la maladie est le bluetongue virus (BTV), un virus à ARN double brin de la famille des Reoviridae, et, comme le virus de la peste équine (african horse sickness) également transmis par des Culicoides, il appartient au genre Orbivirus.
Les orbivirus sont des virus non-enveloppés avec une capside icosaédrique à symétrie cubique d'ordre 3, qui contient un génome segmenté. Ce génome est composé de 10 segments S1-10 qui encodent 7 protéines de structure VP1-7 et au moins 4 protéines non-structurelles NS1-4[3].
Dans une cellule infectée, l'assemblage des nouvelles particules de BTV s'effectue dans le cytoplasme[3].
Propriétés
La résistance du virus bluetongue aux agents physiques et chimiques est la suivante[4] :
- inactivé après 180 minutes à 50 °C ou 15 minutes à 60 °C
- inactivé par la β-propiolactone et le phénol
- sensible à un pH inférieur à 6,0 et supérieur à 8,0
- peut survivre longtemps en présence de protéines
Sérotypes
Le pouvoir pathogène varie considérablement d'une souche à l'autre[5]. En 2019, 24 sérotypes différents (BTV1-24) sont reconnus par l'OIE, et soumis à notification obligatoire[4]. Il y a peu de protection croisée entre les sérotypes : l'infection par un sérotype (ou la vaccination contre un sérotype) ne protège pas (ou pas nécessairement) contre les autres sérotypes[3].
Dans les années 2010, en sus de ces sérotypes reconnus, au moins 5 nouveaux sérotypes ont été découverts : Les BTV25-27 dits « BTV atypiques » ne se trouvent que chez les petits ruminants, ne sont pas pathogènes, et sont transmissibles par contact. Le BTV-28 peut aussi se transmettre par contact mais avec des signes cliniques. Deux autres sérotypes ont été proposés, mais ils n'ont pas été étudiés en détail[3].
Le BTV-25 découvert en Suisse en 2008, sur une chèvre saine, a été appelé virus Toggenburg[6].
Le nombre de sérotypes découverts, typiques ou atypiques, chez les ruminants domestiques et sauvages, augmente avec l'effort de surveillance et les capacités de détection (utilisation de nouvelles technologies). Il est probable qu'ils soient peu pathogènes, mais ils sont à surveiller car susceptibles de recombinaison avec des sérotypes virulents[3].
Cette recombinaison ou réassortiment génétique, peut aussi survenir lorsque des sérotypes virulents différents circulent simultanément dans une même population d'hôtes[7].
Vecteurs
Vecteurs principaux

La maladie est non contagieuse, et se transmet par des vecteurs : des petits moucherons piqueurs du genre Culicoides, famille des Ceratopogonidae. Sur les 1315 espèces de Culicoides recensées en 2015[8], seule une quinzaine sont vectrices de BTV. La température optimum pour une activité maximale de ces moucherons est 24 °C, vers 15-18 °C, ils s'arrêtent de voler[9].
Un Culicoides infesté le reste à vie en multipliant le virus de manière intense dans ses glandes salivaires (période de réplication de 6 à 8 jours)[4]. Cette réplication s'arrête lorsque la température s'abaisse à moins de 15 °C. Une seule de ses piqûres suffit à infecter un hôte sensible[9].
Chaque espèce vectrice de Culicoides transmet des sérotypes préférentiels dans une zone géographique donnée, constituant ainsi différents « pathosystèmes » dans le monde[7].
Culicoides imicola est reconnu comme le vecteur majeur de la fièvre catarrhale ovine en région méditerranéenne[10] et en Afrique. Il transmet les BTV1-15, 18-19, 22 et 24-25.
En Europe non méditerranéenne, d'autres vecteurs ont été signalés : Culicoides dewulfi , Culicoides obsoletus et Culicoides Pulicaris sont susceptibles de transmettre le virus (BTV1, 4 et 8)[10].
En Amérique du nord, les vecteurs sont Culicoides sonorensis et Culicoides occidentalis (BTV 1-3, 5, 6, 11, 13-14, 17, 19 et 22) ; en Amérique centrale et du sud Culicoides insignis et Culicoides pusillus (BTV1, 3-4, 6, 8, 12, 14, 17 et 19-20).
Pour le sous-continent indien, les vecteurs principaux sont Culicoides oxystoma et C. imicola (BTV1-20 et 23).
En Extrême-orient, on trouve C. oxystoma, Culicoides brevitarsis et Culicoides Wadai (BTV1-4, 11-21 et 23) et dans le Pacifique C. brevitarsis, Culicoides fulvus, C. wadai et Culicoides actoni (BTV 1, 3, 9, 15-16, 20-21 et 23)[7].
Autres vecteurs
De manière anecdotique ou occasionnelle, d'autres vecteurs, comme les tiques Ixodidae et Argasidae, pourraient être incriminés dans la transmission du virus de manière passive (sans multiplication). Du fait de l'absence de multiplication virale dans ces hôtes, ces vecteurs ne sont pas responsables de la diffusion de la maladie à grande échelle, mais pourraient être incriminés dans des phénomènes ponctuels de transmission[11],[12]. Un passage transovarien (⇒ passage du virus à la descendance) chez la tique pourrait expliquer la survie hivernale de certains virus (comme le BTV8) en Europe, lorsque le climat ne permet pas aux Culicoïdes de survivre à l'hiver[11].
Transmission et contamination
Les moucherons Culicoïdes sont les seuls transmetteurs significatifs de BTV dans la nature. Les vecteurs s'infectent en ingérant le sang d'animaux contaminés. En l'absence de vecteurs, la maladie ne peut pas se propager d'un animal à l'autre[10].
Une transmission placentaire (de la gestante au fœtus) a été mise en évidence et une transmission par contact étroit (élevage intensif) a été documentée[13],[14]. Le virus a été retrouvé dans la semence des mâles, et peut se transmettre par là aux vaches et aux brebis sensibles, mais cette voie est peu importante[5].
La transmission virale peut se produire tout au long de l'année, elle est la plus forte en périodes chaudes et pluvieuses (survenues saisonnières). Les bovins et les veaux infectés in utero, jouent le rôle de réservoir. Ils permettent au virus de passer l'hiver (overwintering) dans les régions tempérées où l'hiver est souvent trop rigoureux pour permettre une survie du vecteur toute l'année.
Dès le printemps, la densité des Culicoides commence à augmenter, mais ils ne se nourrissent que sur les bovins, sur lesquels ils se contaminent. Ce n'est que plus tard qu'ils commencent à piquer les ovins[9].
Chez l'animal, le virus n'est pas excrété dans la salive, les mucus ou le jetage, ni dans les lésions buccales bénignes. On ne le retrouve donc pas dans le milieu extérieur, sauf en cas de présence de sang : blessures, mise bas[9]…
Le virus n'est pas transmissible à l'homme, par piqûre ou morsure d'insecte, par contact avec les animaux malades, la laine ou la consommation de lait : il n'existe aucun risque de santé publique (humaine) lié à la fièvre catarrhale ovine[5].
Espèces affectées
La fièvre catarrhale du mouton a été décrite pour la première fois en Afrique du Sud, où elle était probablement endémique chez les ruminants sauvages. Classiquement, la fièvre catarrhale était réputée n'affecter que les ovins.
L'infection était généralement inapparente et jugée sans effets significatifs chez les bovins et les caprins même quand le virus était retrouvé dans leur sang. Cependant une surmortalité a été démontrée chez les bovins dans les années 2000-2010. Cette maladie pourrait avoir été sous-estimée chez le bovins, en raison d'une « clinique peu spécifique »[15] et de problèmes de qualité des tests diagnostiques et parfois de réticences à déclarer des animaux malades par peur des conséquences socio-économiques[15].
Les races domestiques améliorées sont beaucoup plus sensibles au virus que les espèces domestiques rustiques[7]. Les ruminants sauvages susceptibles d'être atteints sont les buffles, les antilopes, les cerfs, les wapitis et les camélidés[5].
Clinique et traitement
Par gravité croissante, on distingue les formes inapparentes (sans symptômes), subaiguës, aiguës et suraiguës. La morbidité peut atteindre 80 % du troupeau, et la mortalité 5 à 10 %, et jusqu'à 40 % chez les animaux élevés dans de mauvaises conditions. Cette mortalité survient au 10e-12e jour suivant le début de la maladie[7].
En Europe, le BTV8 est responsable de la plus forte morbidité du bétail (jusqu'à 100 % d'un troupeau de moutons), mais sa mortalité est très faible (moins de 1 %)[4].
Symptômes et signes cliniques

La période d'incubation est de l'ordre de 5 à 10 jours. Un individu infecté, sans ou peu de signes cliniques, est virémique en 4 jours après l'infection (susceptible de transmettre le virus par insecte vecteur)[4].
Chez les ovins, les principaux symptômes sont une forte fièvre et des lésions du museau : salivation excessive, écoulement nasal, œdème, érosions et ulcérations des muqueuses, langue enflée et colorée en bleu[16].
Chez les ovins et les bovins, il existe en outre une raideur des membres et des boiteries, une fonte musculaire importante, un érythème des mamelles chez les bovins, ainsi que des avortements et malformations congénitales[4].
Diagnostic et traitement
Le diagnostic est suspecté sur la base de signes cliniques typiques, et de la présence des insectes vecteurs dans la zone concernée.
Il est confirmé par des tests de laboratoire. Les prélèvements se font à partir du sang, du lait, d'organes d'animaux morts, de produits d'avortement. L'identification se fait par méthodes immunologiques et virologiques. Plusieurs de ces tests sont obligatoires pour le commerce international[4].
S'agissant d'un virus, il n'existe encore aucun traitement efficace. Il existe par contre des traitements symptomatiques. Les animaux ne doivent être traités qu’avec des médicaments vétérinaires ayant une Autorisation de mise sur le marché (AMM), sur prescription vétérinaire.
Conséquences économiques
La fièvre catarrhale ovine entraîne des pertes économiques directes liées à la morbidité et la mortalité : les animaux guéris ont des problèmes des voies respiratoires, de retard de croissance et de baisse de fertilité des mâles et des femelles (avortements précoces).
Ainsi en France, une étude a montré une baisse faible, mais significative de la productivité des troupeaux En 2009, probablement à la suite des épizooties de FCO de 2007 puis de 2008, le nombre de naissances de veaux de races allaitantes a chuté de 2,7 % (déficit de plus de 59 000 veaux). Dans tous les bassins allaitants, les trois principales races à viande ont subi un décalage des naissances (par rapport à la campagne précédente, avec plus de mises bas de mai à juillet, qui ont partiellement compensé un taux diminué de naissances en hiver)[17].
D'autres répercussions tiennent au déclassement des carcasses, à la mauvaise qualité de la laine, et à la baisse de production laitière. Les mesures de contrôle ont aussi de graves conséquences économiques : vaccination, tests diagnostiques, visites vétérinaires, restrictions des mouvements d'animaux et arrêt des exportations[7].
Répartition géographique

Avant 1998, la fièvre catarrhale ovine, d'origine africaine, était considérée comme enzootique dans la ceinture mondiale intertropicale. Il y avait quelques incursions épizootiques, dans le bassin méditerranéen : les épizooties notables, plutôt rares et non persistantes du XXe siècle, furent celle de Chypre (1943), d'Israël (1951), du Portugal et de l'Espagne (1956-1960), de l'île grecque de Lesbos (1980)[5],[7].
Les divers « pathosystèmes » (sérotype local de BTV/espèce locale de moucheron) paraissaient stables, confinés dans leur aire géographique[3].
Depuis la fin du XXe siècle, la maladie s'étend, voire s'installe, à des latitudes supérieures au nord et au sud. Les limites nord sont désormais : en Amérique autour de la frontière canadienne avec les États-Unis, des Pays-Bas en Europe, de la Corée du nord en Extrême-Orient ; la limite sud va de la Terre de Feu à la Nouvelle-Zélande[7].
Extensions
Europe méditerranéenne

De 1998 à 2005, plusieurs souches de 5 BTV différents (1, 2, 4, 9 et 16) sont détectées dans le bassin méditerranéen. Deux voies principales d'introduction sont observées : une voie occidentale à partir du Maghreb vers l'Espagne et les îles de la méditerranée occidentale (la Corse est touchée en 2000[10] par le BTV-2), et une voie orientale (BTV-4 et 16) à partir des Balkans et de la Turquie vers la Grèce et l'Italie[2].
En 2007, des BTV-1, d'abord détectés au Maroc, circulent en Espagne et touchent le Pays basque français, en circulant jusqu'en Bretagne[7]. En 2012, de nouveaux BTV-4 sont identifiés en Sardaigne, proches de ceux signalés en Tunisie, et probablement réassortis avec des BTV-1[2]. En 2013, de nouveaux cas de BTV-1 sont signalés en Corse, alors qu’aucun foyer n’avait été signalé dans l’île depuis 2006[19].
Toutes ces souches méditerranéennes sont d'origine africaine, elles parviennent en Europe du sud, mais de façon périodique sans s'y installer[2].
Depuis 2016, un BTV-3 de forme virulente circule en Tunisie, en étant détecté en Sicile et en Sardaigne. Le risque d'extension à la Corse est élevé[2].
Europe du nord
En 2006, un nouveau variant de BTV-8 est signalé aux Pays-Bas, d'origine inconnue, en provoquant cette année là, 456 foyers épizootiques. En Europe du Nord, plus de 2000 foyers sont alors identifiés, presque tous globalement situés sur les régions frontières Pays-Bas[20], Allemagne (885 foyers) et Belgique (695 foyers). La France (6 foyers) et le Luxembourg (5 foyers) sont aussi touchées dans les zones limitrophes de la Belgique[2].
En 2008, des BTV-6 et -11 émergent dans la même zone précédente, mais de façon limitée, sans manifestations cliniques. Toutefois, la France compte alors de 24 000 cas de BTV-8[2]. Ce nombre comprend les animaux malades mais aussi les animaux infectés séropositifs mais n'ayant pas déclaré la maladie (prise de sang obligatoire pour les animaux destinés à l'exportation, notamment vers l'Italie).
Après plusieurs années de lutte contre la maladie, la France se déclare indemne de FCO (BTV-8) en 2012. Mais trois ans plus tard, un nouveau foyer est détecté dans l'Allier[21]. Le génome de ce BTV-8 est très proche du BTV-8 des années 2006-2010, ce qui suggère une circulation à bas bruit depuis cette période, donc une installation endémique de ce BTV en France métropolitaine[2].
Depuis 2015, près de 3 000 cas de BTV-8 ont été signalés en France en 2019, mais il s'agit surtout d'animaux testés positifs (sans commune mesure avec les animaux malades des épizooties de 2006-2008).
Europe de l'est
Des BTV-14 sont détectés pour la première fois en Russie en 2011 et en Pologne en 2012, et des BTV-4 en Hongrie en 2014. Le BTV-4 isolé en Hongrie se retrouve dans les Balkans, la Grèce et l'Italie, et touche la Corse en 2016 et la Haute-Savoie en 2017. Ce BTV-4 est peu pathogène pour les bovins, mais peut rendre malade des ovins non vaccinés[2].
Analyses
Chez les ovins, les manifestations cliniques furent très variables, bénignes à très graves, en fonction du sérotype du BTV.
La souche BTV-8 est exceptionnelle dans la mesure où elle entraîne l'apparition de signes cliniques chez les bovins[15], en ayant aussi la capacité d'infecter les ruminants sauvages. En France, après une surmortalité chez les veaux de moins de 7 jours lors de l'épidémie de 2006-2008, la résurgence épidémique d'après 2015 a donné très peu de signes cliniques. Ce qui pourrait s'expliquer par une immunité partielle (vaccination obligatoire pour l'exportation) ou une baisse de virulence du virus[2].
En 2018, les autorités vétérinaires françaises décident de considérer que les BTV-4 et BTV-8 sont désormais enzootiques (installés) en France. En 2019, le BTV-8 reste présent en Allemagne, Suisse et Belgique[2].
Facteurs d'émergence
De nombreux facteurs contribuent à l'extension d'une arbovirose comme la FCO : des hôtes infectés, des vecteurs compétents, et des conditions climatiques favorables, notamment de température, qui permettent au vecteur de se multiplier et de transmettre l'agent pathogène. La capacité de certaines souches de BTV à s'adapter à des culicoïdes ou autres, capables de passer l'hiver (d'avoir une activité hiver-printemps) pourrait être déterminante.
Réchauffement climatique
En méditerranée occidentale, la FCO se répand vers le nord, à la suite d'une extension de son principal vecteur d'origine africaine C. imicola, facilitée par les changements liées au réchauffement climatique[22],[23]. Mais des études plus récentes tendent à démontrer une existence ancienne de C. imicola en Europe du sud, et ce serait plutôt le BTV qui se serait adapté à des C. imicola autochtones [7].
Ces hypothèses n'expliquent pas l'apparition du BTV-8 en Europe du nord où C. imicola est absent[7]. La circulation du BTV-8 est alors rapportée à d'autres Culiculoides autochtones identifiés comme vecteurs : C. obsoletus, dewulfi, scoticus et chioreptus[2].
Commerce agroalimentaire
La mondialisation des réseaux agroalimentaires et de l'élevage en particulier augmente le risque de diffusion de cette maladie. Deux hypothèses d'introductions sont avancées : celle des animaux infectés, et celle des moucherons exotiques infectés via le transport de marchandises. Les culicoïdes locaux prennant ensuite le relais de la transmission[7].
Recombinaison virale
Des BTV de sérotypes différents, circulant simultanément en infectant un même hôte, peuvent se recombiner entre eux, aboutissant à de nouveaux variants, comme ceux entre les BTV-1 et BTV-4.
Cette recombinaison peut se faire aussi entre un BTV sauvage et un BTV vaccinal provenant de vaccins vivants utilisés. Ce fut le cas des BTV-16 détectés en 2004 de la Turquie à la Corse. L'analyse de leur génome a montré qu'ils étaient proches d'un vaccin vivant sud-africain, produit à partir d'un BTV-16 atténué, isolé au Pakistan. Ce BTV-16 a disparu de lui-même en moins d'un an, mais ces observations ont conduit l'Union Européenne à abandonner le vaccin vivant contre le BTV-16 pour n'utiliser que le vaccin inactivé.
L'origine du BTV-8 européen reste indéterminée, mais l'analyse de son génome semble indiquer une origine africaine subsaharienne. Le fait qu'il puisse être tératogène chez la brebis gestante pourrait aussi indiquer une origine vaccinale, de tels faits similaires ayant été décrits aux États-Unis et en Afrique du Sud[2].
Moyens de lutte
La FCO est une maladie animale à déclaration obligatoire, répertoriée dans le code sanitaire pour les animaux terrestres de l'OIE. La FCO (BTV1 à 24) doit faire l'objet d'une notification obligatoire auprès de l'OIE [5], les BTV25 et suivants, peu pathogènes, ne sont pas concernés[2].
Surveillance et prévention
La surveillance consiste à faire des prélèvements réguliers sur un échantillon d'individus dit « troupeau sentinelle » à la recherche d'une présence du virus[10]. D'autres programmes identifient les insectes vecteurs dans une zone donnée : localisation, distribution et prévalence[10], par exemple par des piégeages d'insectes de façon à repérer rapidement l'apparition des vecteurs dans les zones où ils ne sont pas endémiques[10].
La prévention est assurée par la mise en quarantaine des exploitations touchées ou la restriction des déplacements de bétail lors de la période d'activité des insectes. Le contrôle de l'insecte vecteur se fait par désinsectisation au niveau des animaux (bovins et ovins) ainsi que des bâtiments et véhicules, en particulier les avions[4]. En France, la liste des désinfectants autorisés est disponible sur un site public de l'ANSES[24].
Vaccination

La vaccination est la mesure la plus efficace et la plus simple pour réduire les pertes liées à la malade ou interrompre le cycle entre les animaux contaminés et les vecteurs[5]. Les sérotypes vaccinaux doivent correspondre aux sérotypes sauvages causant l'affection dans une région donnée. On distingue deux types de vaccins, ayant chacun leurs avantages et inconvénients[3].
Les vaccins vivants atténués ont l'avantage d'être peu coûteux et de couvrir la plupart des sérotypes. Mais ils sont plus difficiles à utiliser (3 vaccins pentavalents couvrant 15 sérotypes au total), avec un risque tératogène pour la gestante vaccinée, et un risque de réassortiment avec un virus sauvage (animal infecté à la fois par un virus vaccinal et un virus sauvage) avec émergence de nouvelles souches virales. Ces vaccins restent utilisés dans la plupart des pays du monde, en fonction des objectifs et des situations locales.[3],[4].
Les vaccins inactivés ont l'avantage de leur sureté, mais ils sont plus chers, et ne couvrent que quelques sérotypes (BTV-1, 2, 4 et 8). Depuis 2008, les vaccins inactivés sont les seuls à être autorisés en Europe[3],[2].
Le 14 février 2008 le ministre de l'Agriculture Michel Barnier annonce un plan de vaccination contre la fièvre catarrhale en France[25]. Dans plusieurs pays européens, les campagnes de vaccination massive ont démontré leur efficacité à éliminer les épizooties les plus graves[3], mais pas à éradiquer le virus. En Europe, les vaccins inactivés sont disponibles : ils sont recommandés pour les éleveurs (qui en décident d'eux-mêmes) et obligatoires pour le commerce d'animaux vivants[2].
En 2013, René Riesel publie un livre sur la nocivité des vaccins après avoir été entendu à la gendarmerie du Collet-de-Dèze (Lozère) pour avoir refusé, en 2009, de faire vacciner son cheptel contre la fièvre catarrhale ovine[26].
En 2019, de nombreux nouveaux vaccins contre les BTV sont en cours de recherches[3].
Notes et références
- N. J. Maclachlan, C. E. Mayo, P. W. Daniels et G. Savini, « Bluetongue », Revue Scientifique Et Technique (International Office of Epizootics), vol. 34, no 2, , p. 329–340 (ISSN 0253-1933, PMID 26601438, DOI 10.20506/rst.34.2.2360, lire en ligne, consulté le )
- Cindy Kundlacz, Grégory Caignard, Corinne Sailleau et Cyril Viarouge, « Bluetongue Virus in France: An Illustration of the European and Mediterranean Context since the 2000s », Viruses, vol. 11, no 7, (ISSN 1999-4915, PMID 31340459, PMCID 6669443, DOI 10.3390/v11070672, lire en ligne, consulté le )
- Piet A. van Rijn, « Prospects of Next-Generation Vaccines for Bluetongue », Frontiers in Veterinary Science, vol. 6, (ISSN 2297-1769, PMID 31824966, PMCID 6881303, DOI 10.3389/fvets.2019.00407, lire en ligne, consulté le )
- (en) OIE, « Bluetongue - fiche technique »
- « Langue bleue: OIE », sur www.oie.int (consulté le )
- Martin A. Hofmann, Sandra Renzullo, Markus Mader et Valérie Chaignat, « Genetic Characterization of Toggenburg Orbivirus, a New Bluetongue Virus, from Goats, Switzerland », Emerging Infectious Diseases, vol. 14, no 12, , p. 1855–1861 (ISSN 1080-6040, PMID 19046507, PMCID 2634640, DOI 10.3201/eid1412.080818, lire en ligne, consulté le )
- Gérard Duvallet, Entomologie médicale et vétérinaire, Marseille, Versailles, IRD - QUAE, (ISBN 978-2-7099-2376-7), p. 358-359.
- Gérard Duvallet 2017, op. cit., p. 346.
- « Epidémiologie de la FCO », sur agriculture.gouv.fr
- Jacques Barnouin, Ivan Sache et al. (préf. Marion Guillou), Les maladies émergentes : Épidémiologie chez le végétal, l'animal et l'homme, Quæ, coll. « Synthèses », , 444 p. (ISBN 978-2-7592-0510-3, ISSN 1777-4624, lire en ligne), IV. Facteurs environnementaux des émergences, chap. 24 (« L'émergence de la fièvre catarrhale ovine en France : approche interdisciplinaire du compartiment "vecteurs" »), accès libre.
- Chantal Bouwknegt, Piet A. van Rijn, Jacqueline J. M. Schipper et Dennis Hölzel, « Potential role of ticks as vectors of bluetongue virus », Experimental & Applied Acarology, vol. 52, no 2, , p. 183–192 (ISSN 0168-8162, PMID 20358393, PMCID 2928921, DOI 10.1007/s10493-010-9359-7, lire en ligne, consulté le )
- Stott JL, Osburn BI, Alexander L (1985) Ornithodoros coriaceus (pajaroello tick) as a vector of bluetongue virus. Am J Vet Res 46:1197–1199
- (en) Menzies FD, McCullough SJ, McKeown IM. et al. « Evidence for transplacental and contact transmission of bluetongue virus in cattle » The Veterinary Record 2008;163(7):203–209.
- Mirjam Tineke Willemijn van der Sluijs, Abraham J. de Smit et Rob J. M. Moormann, « Vector independent transmission of the vector-borne bluetongue virus », Critical Reviews in Microbiology, vol. 42, no 1, , p. 57–64 (ISSN 1549-7828, PMID 24645633, DOI 10.3109/1040841X.2013.879850, lire en ligne, consulté le )
- INRA, AFSSA, École nationale des services vétérinaires (2010) Présentation faite par JB Perrin, P Hendrikx, C Ducrot et D Calavas et intitulée [Impact de la FCO sur la mortalité des bovins], Réunion d'information et d'échanges sur la restitution des résultats de la recherche opérationnelle FCO en France ; 18 mars 2010, Afssa, 20 pages
- Une langue bleue peut se voir chez des patients humains atteints de cyanose, mais sans rapport aucun avec la maladie vétérinaire de la langue bleue par virus bluetongue.
- B. Mounaix ; Institut de l'élevage) ; « Impact de la fièvre catarrhale sur le nombre de naissances de veaux dans les élevages allaitants » et Synthèse [PDF].
- (en-US) Claude Saegerman, « Bluetongue Epidemiology in the European Union », Emerging Infectious Diseases journal - CDC, vol. 14, no 4, , p. 539-544. (DOI 10.3201/eid1404.071441, lire en ligne, consulté le )
- http://agriculture.gouv.fr/Fievre-catarrhale-ovine, 1701
- (en) « Blue Tongue confirmed in Belgium and Germany », Commission européenne, (consulté le )
- « Un foyer de fièvre catarrhale ovine, la « maladie de la langue bleue », découvert dans l’Allier », sur Le Monde.
- (en) Bethan V. Purse, Philip S. Mellor, David J. Rogers, Alan R. Samuel, Peter P. C. Mertens et Matthew Baylis, « Climate change and the recent emergence of bluetongue in Europe », Nature Reviews Microbiology, vol. 3, no 2, , p. 171-181. (DOI 10.1038/nrmicro1090, lire en ligne, consulté le )
- M. Baylis, « The role of climate change in a developing threat: the case of bluetongue in Europe », Revue Scientifique et Technique OIE, vol. 36, no 2, , p. 467-478. (lire en ligne)
- « ephy | », sur ephy.anses.fr (consulté le )
- source : site Web-agri Fièvre catarrhale Premières précisions sur la mise en place du plan de vaccination
- Lettre ouverte à la Direction des Services Vétérinaires, 17 octobre 2009
Voir aussi
Bibliographie
- René Riesel, Surveiller et guérir (les moutons) ; l'administration du désastre en action : une étude de cas, Éditions de l'Encyclopédie des Nuisances, Paris, 2013.
Liens externes
- « Fièvre catarrhale ovine », sur agriculture.gouv.fr
- Rappels de la législation depuis 2000
- Fil d'informations fièvre catarrhale (sur le site professionnel agricole Web-agri)
- Vacciner pour régner, la gestion sanitaire de la fièvre catarrhale des ruminants (2010), Z, revue itinérante de critique sociale
- Portail de l’agriculture et l’agronomie
- Portail de l’élevage
- Portail de la virologie
- Portail de la médecine vétérinaire