Glycoside hydrolase
Les Glycoside hydrolases (ou glycosidases) catalysent l'hydrolyse de liaisons glycosidiques et libèrent au moins un composé osidique. Ce sont des enzymes extrêmement communes, dont les rôles sont aussi divers que la dégradation des glucides complexes (cellulose et hémicellulose), les défenses anti-bactériennes (ex. le lysozyme), la pathogénicité (ex. les neuraminidases virales) ou le métabolisme cellulaire (amylases ou enzyme de débranchement du glycogène pour le métabolisme énergétique, mannosidases comme modulateur de glycosylation des protéines, ...). Les glycosyltransférases et les glycosides hydrolases sont les deux classes majeures d'enzymes impliquées dans la synthèse et la rupture des liaisons osidiques.
Occurrence et importance
Les glycosidases sont ubiquitaires. Chez les procaryotes on retrouve des glycosides hydrolases intracellulaires et extracellulaires, ces dernières étant largement impliquées dans les processus d'assimilation des nutriments. Une glycosidase notable du règne bactérien est la β-galactosidase LacZ: Cette enzyme est impliquée dans la régulation de l'opéron lactose longtemps étudié chez E. coli. Chez les organismes supérieurs nombre de glycoside hydrolases sont localisées au niveau du réticulum endoplasmique ou de l'appareil de Golgi où elles jouent différents rôles dans les processus de maturation des protéines. Le lysosome est un organite spécialisé dans la dégradation des macromolécules biologiques. Ils contiennent des glycosides hydrolases actives à pH acides. Plusieurs maladies sont reliées à des déficiences de ces enzymes, pouvant conduire à des problèmes au cours du développement, voire à la mort. Les glycosidases du tractus intestinal et de la salive ont pour rôle la dégradation des glucides complexes, dont l'amidon, en sucres "simples" (une ou deux unités osidiques) qui pourront être assimilés. Par exemple la lactase est indispensable à la dégradation du lactose présent dans le lait. Elle est fortement exprimée chez le nourrisson, mais son taux décroit généralement au après le sevrage, ce qui peut conduire à une intolérance au lactose à l'âge adulte.
Classification
Les glycosides hydrolases sont classifiées dans le groupe EC 3.2.1.x correspondant aux enzymes catalysant l'hydrolyse des liaisons O- ou S-glycosidiques. La rétention (ou l'inversion) de la configuration absolue du carbone anomérique au cours de l'hydrolyse permet de séparer les enzymes en fonction de leur mécanisme[1]. De la même manière il est possible de classifier les glycosides hydrolases en fonction de leur spécificité à hydrolyser les sucres terminaux d'une chaîne (exo-glycosidases), ou au contraire, à libérer des oligosaccharides (endo-glycosidases) en attaquant une liaison osidique au sein d'une chaîne. La majorité des exo-glycosidases sont actives sur les extrémités non réductrices de leur substrat. Finalement, les glycosides hydrolases peuvent être classées en fonction de leur séquence, ou encore de leur structure tridimensionnelle[2].
Classification basée sur la séquence
En biologie, les méthodes de classification basées sur la comparaison de séquences sont des outils extrêmement puissants pour apporter une première hypothèse concernant le rôle d'une protéine dont la séquence est connue, mais pour laquelle la fonction n'a pas encore été démontrée. La classification des glycosides hydrolases en fonction de similarité de séquence a abouti à la définition de 115 familles () accessibles depuis la base de données CAZy (pour Carbohydrate Active enZymes : Enzymes actives sur les sucres)[3],[2],[4],[5],[6]. La base de données, régulièrement mise à jour, fournit une classification des glycosides hydrolases ayant pour but de prédire, pour une enzyme nouvellement séquencée, d'une part le mécanisme catalytique (inversion/rétention), d'autre part les résidus du site actif et enfin, les substrats probablement reconnus. CAZy, accessible gratuitement en ligne, est supportée par Cazypedia, une encyclopédie en ligne visant à rassembler les connaissances autour des enzymes actives sur les sucres[7].
Classification basée sur la structure
Différentes familles de glycosides hydrolases partagent une même organisation spatiale globale, ce qui a permis de définir la notion de clans[8]. Ainsi le clan GH-K regroupe les familles 18, 20 et 85, qui possèdent toute un repliement de type tonneau bêta. À ce jour () 14 clans sont définis, certaines familles ne faisant partie d'aucun clan, comme la famille 9.
Mécanismes
Koshland a publié, en 1953, les mécanismes catalytiques expliquant comment la configuration absolue d'une molécule pouvait être changée -ou non- au cours d'une réaction d'hydrolyse enzymatique[9]. Ces mécanismes sont les plus fréquemment rencontrés au sein des glycosides hydrolases, même si quelques familles d'enzymes possèdent des mécanismes catalytiques particuliers[10],[11].
Inversion
Les glycosidases dont le produit a, pour son carbone anomérique, une configuration absolue inverse de celle maintenue dans le substrat, utilisent un mécanisme inverseur. Ces enzymes utilisent typiquement deux résidus catalytiques, l'un faisant office d'acide et l'autre de base. Le schéma ci-dessous décrit le mécanisme d'une β-glucosidase au mécanisme inverseur, tel que décrit par Koshland. On notera qu'il manque une étape de transfert de proton, qui a généralement lieu via une ou des molécules d'eau, pour régénérer l'enzyme.

Rétention
Les glycosidases dont le produit a, pour son carbone anomérique, une configuration absolue identique à celle maintenue dans le substrat, ont un mécanisme rétenteur (ou conservateur). Typiquement ces glycosidases ont un mécanisme en deux temps, chacune des étapes aboutissant à l'inversion de la configuration absolue du carbone anomérique du produit. Ce sont à nouveau deux résidus -portant généralement un groupe acide carboxylique (acide aspartique ou glutamique)- qui catalysent ces deux étapes. Dans la première partie, une base joue le rôle de nucléophile et attaque le carbone anomérique (carbone 1' du produit), ce qui aboutit à la formation d'un intermédiaire covalent glycosyl-enzyme. L'acide participe à l'élimination de la partie aglycone du substrat en lui fournissant un proton. Une molécule d'eau peut alors prendre la place de l'oxygène de la liaison osidique rompue, et activée par l'acide aminé déprotoné au cours de la première étape, réaliser l'hydrolyse du conjugué glycosyl-enzyme, en inversant à nouveau la configuration absolue du produit. Le produit final possède donc la même configuration absolue que celle observée au sein du substrat. Le mécanisme est illustré ci-dessous pour le lysozyme de blanc d'œuf[12].
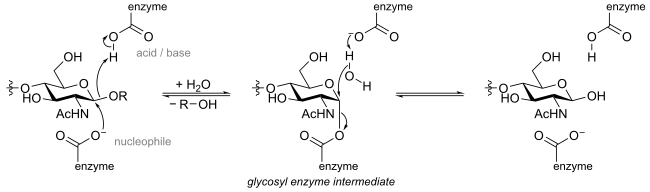
Un mécanisme alternatif rétenteur fait intervenir un groupe nucléophile du substrat plutôt qu'appartenant à l'enzyme. Ce mécanisme peut être rencontré chez certaines N-acetylhexosaminidases, dont le groupe acétamido du substrat, à proximité du centre actif, peut participer à la catalyse. Décrit pour les familles 4 et 109, un autre type de mécanisme fait intervenir un cofacteur d'oxydoréduction : le NAD. L'hydrolyse est alors catalysée par l'oxydation du substrat, ce qui génère, en intermédiaire, un sucre insaturé, lors de la béta élimination de la partie aglycone du substrat. Lors de l'attaque d'une molécule d'eau sur l'intermédiaire, le produit saturé est régénéré et libéré[10].
Notes et références
- Sinnott, M. L. "Catalytic mechanisms of enzymatic glycosyl transfer". Chem. Rev. 1990, 90, 1171-1202.
- CAZy Family Glycoside Hydrolase
- Henrissat, B. and Coutinho P.M. "Carbohydrate-Active Enzymes server". 1999.
- (en) Henrissat B, Callebaut I, Mornon JP, Fabrega S, Lehn P, Davies G, « Conserved catalytic machinery and the prediction of a common fold for many families of glycosyl hydrolases », Proc. Natl. Acad. Sci. U.S.A., vol. 92, no 15, , p. 7090–7094 (PMID 7624375, DOI 10.1073/pnas.92.15.7090)
- (en) Henrissat B, Davies G, « Structures and mechanisms of glycosyl hydrolases », Structure, vol. 3, no 9, , p. 853–859 (PMID 8535779, DOI 10.1016/S0969-2126(01)00220-9)
- Bairoch, A. "Classification of glycosyl hydrolase families and index of glycosyl hydrolase entries in SWISS-PROT". 1999.
- CAZypedia, an online encyclopedia of carbohydrate-active enzymes.
- Naumoff, D.G. "Development of a hierarchical classification of the TIM-barrel type glycoside hydrolases". Proceedings of the Fifth International Conference on Bioinformatics of Genome Regulation and Structure. 2006, 1, 294-298.
- Koshland, D.E. (1953). Stereochemistry and the mechanism of enzymatic reactions. Biol. Rev. Cam. Phil. Soc. 28, 416–436.
- Shyamala S. Rajan,1 Xiaojing Yang,1 Frank Collart,Vivian L.Y. Yip, Stephen G. Withers,Annabelle Varrot,4 John Thompson,Gideon J. Davies,4 and Wayne F. Anderson, Structure, Vol. 12, 1619–1629, September, 2004
- Liu, Q. P., Sulzenbacher, G., Yuan, H., Bennett, E. P., Pietz, G., Saunders, K., Spence, J., Nudelman, E., Levery, S. B., White, T., Neveu, J. M., Lane, W. S., Bourne, Y., Olsson, M. L., Henrissat, B., and Clausen, H. (2007) Nat. Biotechnol. 25, 454 – 464d
- Vocadlo, D. J.; Davies, G. J.; Laine, R.; Withers, S. G. Nature 2001, 412, 835.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Glycoside hydrolase » (voir la liste des auteurs).
- Portail de la biochimie
- Portail de la biologie cellulaire et moléculaire