Hippocampe (cerveau)
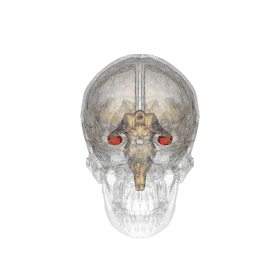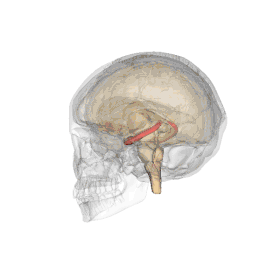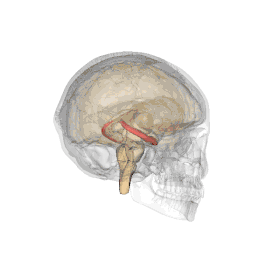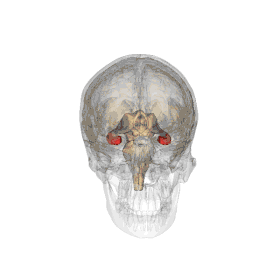
L'hippocampe est une structure du télencéphale des mammifères. Il appartient notamment au système limbique et joue un rôle central dans la mémoire et la navigation spatiale. Chez l'Homme et les autres primates, il se situe dans le lobe temporal médian, sous la surface du cortex, au-dessus de la cinquième circonvolution (replis du cortex) temporale T5. Comme le cortex avec lequel il est en étroite relation, c'est une structure paire, présente de manière symétrique dans chaque hémisphère, dont les deux parties sont reliées entre elles par la commissure hippocampique du corps calleux localisée dans le fornix. Il se compose de trois sous-structures : le subiculum, la corne d'Ammon (composée des aires CA1, CA2 et CA3) et le gyrus denté. Il est également le prolongement du fornix ou trigone et les amygdales sont à ses extrémités.
Pour les articles homonymes, voir Hippocampe.

L'hippocampe a été très étudié chez le rongeur pour son implication dans les systèmes de l'inhibition du comportement, de l'attention, de la mémoire spatiale et de la navigation. Une des conséquences d'une lésion à l'hippocampe sur le comportement du rat est l'augmentation de l'activité (déplacement, exploration, etc.). Beaucoup des cellules de l'hippocampe du rat ou de la souris répondent comme des cellules de lieu : elles émettent des trains de potentiel d'action lorsque l'animal passe à des endroits précis de son environnement. Ces cellules de lieu interagissent fortement avec des cellules codant la direction de la tête dans l'espace et avec les cellules de grille du cortex entorhinal voisin et sont supposées jouer un rôle clé dans la navigation spatiale (formation de carte cognitive).
Les différents types de neurones de l'hippocampe sont extrêmement bien organisés, principalement sous forme de strates distinctes. C'est pourquoi, il est fréquemment utilisé comme système modèle pour étudier la neurophysiologie. Une des formes de la plasticité neuronale, connue sous le nom de LTP ou potentialisation à long terme, a été découverte et est très bien caractérisée dans cette structure. La LTP est notamment reconnue pour être un des mécanismes principaux utilisés par le cerveau pour stocker les souvenirs.
L'hippocampe est une des premières structures atteintes dans la maladie d'Alzheimer, ce qui explique les problèmes de mémoire et de désorientation qui caractérisent l'apparition de cette pathologie neurodégénérative. L'hypoxie (la privation d'oxygène), les encéphalites et les épilepsies du lobe temporal sont également des conditions présentant des lésions au niveau de l'hippocampe. Les personnes subissant de graves dommages à l'hippocampe sont susceptibles de souffrir de différents types d'amnésie.
Enfin, l'hippocampe est, avec la zone sous-ventriculaire, une des seules structures cérébrales à présenter une activité de neurogenèse chez l'individu adulte. Cette production de nouveaux neurones fonctionnels a lieu dans le gyrus dentelé durant toute la vie de l'individu. Au contraire de la zone sous-ventriculaire, qui produit des neurones pour le bulbe olfactif, les neurones générés sont destinés à rester dans le gyrus dentelé.
Étymologie

La plus ancienne description de la crête courant le long du sol de la corne temporale du ventricule latéral vient de l'anatomiste vénitien Giulio Cesare Aranzio (1587), qui, le premier, la compara avec un hippocampe (latin : hippocampus, venant du grec ancien : ἵππος, « cheval », et du grec moderne : κάμπος, « monstre marin ») ou, alternativement, avec un ver à soie. L'anatomiste allemand Duvernoy (1729), le premier qui illustra cette structure, fut lui aussi indécis entre l'hippocampe » et le « ver à soie ». « La corne de bélier » fut proposé par l'anatomiste danois Jacob Winslow en 1732, et, une décennie plus tard, un chirurgien français, Garengeot, utilisa le terme cornu Ammonis en référence à la corne d'Ammon (Zeus Ammon, dieu de la Grèce ancienne, amalgame du dieu grec Zeus et du dieu égyptien Amon, qui portait une coiffe avec des cornes de bélier)[1].
Le terme pes hippocampi, également référence à la mythologie, vient probablement des travaux de Isbandis de Diemerbroeck en 1672, qui le compara avec la créature mythologique mi-cheval, mi-poisson. L'hippocampe fut alors décrit comme l'hippocampus major, et son renflement dans la corne occipitale, le calcar avis, fut nommé hippocampus minor par Félix Vicq-d'Azyr lorsqu'il voulut établir une nomenclature des parties du cerveau, en 1786[1]. Il fut notamment confondu en hippotamus en 1779 par Mayer et ses contemporains, jusqu'en 1829, quand Karl Friedrich Burdach rétablit le terme correct. En 1861, l'appellation hippocampus minor fut le centre d'une dispute, au sujet de l'évolution humaine, entre Thomas Huxley et Richard Owen, satiriquement appelée « La grande question hippocampique ». Le terme hippocampus minor disparut peu à peu des livres d'anatomie et fut officiellement supprimé en 1895 des Nomina Anatomica[2].
Aujourd'hui, seul le terme « hippocampe » est encore utilisé. Pes hippocampi est plutôt utilisé comme un synonyme de la corne d'Ammon de Garengeot[1], terme qui survit dans l'appellation des quatre principales divisions histologiques de l'hippocampe : CA1, CA2, CA3 et CA4[3].
Anatomie, structure et organisation
.jpg.webp)
.png.webp)
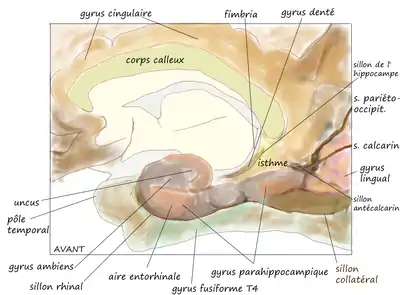
Anatomiquement, l’hippocampe est une élaboration des bords du cortex cérébral[4]. Les structures qui composent les bords intérieurs du cortex font partie du système limbique (du latin « limbus » = bords) : cela inclut l’hippocampe, le cortex cingulaire, le cortex olfactif et l’amygdale (cerveau). Il a longtemps été suggéré que ce système limbique constituait la base neuronale des émotions (voir la théorie du cerveau triunique). Néanmoins, le concept de système limbique est de plus en plus remis en question[5]. Cependant, l’hippocampe est bien connecté à des structures impliquées dans les comportements émotionnels : le septum, le corps mamillaire de l’hypothalamus et le complexe nucléaire antérieure du thalamus. Son rôle limbique ne peut donc pas être totalement écarté.
L’hippocampe a globalement la forme d’un tube courbé, souvent comparé à un hippocampe marin, à une corne de bélier ou encore à une banane[4]. Il peut être distingué comme la zone où le cortex se replie en une seule couche très dense de neurones pyramidaux (de 3 à 6 cellules de profondeur chez le rat) qui s’enroule sur elle-même et forme un U. Une des parties extrêmes de la courbe (CA3 ou CA4) vient s’enfoncer dans le creux du gyrus dentelé qui a lui-même une forme courbée, semblable à un V. L’hippocampe peut de plus être séparé en un hippocampe ventral et un hippocampe dorsal, qui sont similairement organisés mais font partie de circuits neuronaux différents (pour mieux visualiser, parcourir les différentes représentations exposées)[6].
Cette description générale est valable pour une majorité des espèces mammifères, bien que quelques détails varient. Chez le rat les deux hippocampes ressemblent à une paire de bananes reliées à leur extrémité par la commissure hippocampique. Celle-ci se situe au milieu du cerveau, juste sous la partie antérieure du corps calleux qui lui relie les deux hémisphères. Chez l’humain et le singe, l’hippocampe représente une plus petite proportion du cerveau et se retrouve déplacé par rapport au rat ; ce qui fait que l’on parle alors d’hippocampes inférieur et supérieur et non plus ventral et dorsal. De plus, la partie inférieure de l’hippocampe, presque à la base du lobe temporal est bien plus large que la partie supérieure. Cette anatomie compliquée fait que sa forme sur une coupe de cerveau varie beaucoup en fonction de l’axe choisi et de l’emplacement de la coupe.
Structurellement, la formation hippocampique se divise en trois parties :
- les structures para-hippocampiques d'entrée : le cortex entorhinal et le subiculum ;
- l'hippocampe à proprement parler, formé des champs ammoniens (CA1, CA2, CA3 et CA4) et du gyrus dentelé ;
- la fimbria qui est une fibre de sortie des axones reliant les deux hippocampes entre eux et avec les structures de sortie.
Au niveau cellulaire, l'hippocampe est caractérisé par un circuit neuronal trisynaptique : les axones du cortex entorhinal constituent la voie d'entrée de l'information dans l'hippocampe. Appelés fibre perforante, ces axones contactent directement les cellules granulaires contenues dans le gyrus dentelé. Celui-ci envoie massivement ses axones (qui constituent les fibres moussues) vers la zone CA3 : il y a synapse avec les dendrites des cellules pyramidales de cette zone. Puis les axones des cellules pyramidales de la zone CA3 se projettent vers les dendrites des cellules pyramidales de la zone CA1 (voie appelée collatérale de Schaeffer). Celles-ci projettent enfin à leur tour leurs axones vers le subiculum ou le cortex entorhinal complétant ce circuit tri-synaptique[4].
En parallèle à cette boucle trisynaptique, il existe des connexions directes depuis les couches 2 et 3 du cortex entorhinal vers les dendrites de CA3 et de CA1. Le rôle de cette double connectivité est encore mal compris. Les connexions depuis CA1 ou depuis le subiculum vers les neurones des couches profondes du cortex entorhinal ainsi que les connexions entre ces couches profondes et les couches superficielles du cortex entorhinal font que la boucle trisynaptique est incluse dans une boucle plus vaste qui comprend le cortex entorhinal, l'hippocampe proprement dit, le subiculum, qui se referme au niveau du cortex entorhinal, porte d'entrée et de sortie principale entre le néo-cortex et l'hippocampe.
Il existe également une connexion avec des zones plus antérieures du cerveau, à travers la fimbria et qui regroupe divers axones du gyrus dentelé de CA1 et de CA3.
La distinction des zones CA2 et CA4 est assez débattue et leur contour reste difficile à définir sur des seuls critères structurels.
Physiologie
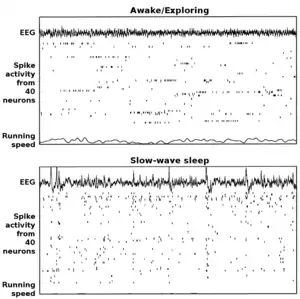
L’hippocampe présente deux modes principaux d’activité, chacun associé à différentes populations de neurones activés et à différents types d’activité électrique résultante mesurée par électro-encéphalographie (EEG). Ces deux modes sont nommés d’après la forme de leur EEG : thêta (présentant des ondes thêta) et activité irrégulière de large amplitude. Les caractéristiques de ces modes, décrites ci-dessous, sont celles obtenues chez le rat, qui est l’animal le plus étudié pour ces expériences[7].
Le mode thêta est celui que l’on observe lorsque l’animal est en activité ou dans des états d’alerte, notamment durant les tâches de locomotion, mais également durant la phase de sommeil à mouvements oculaires rapides (REM en terminologie anglo-saxonne)[8]. Durant le mode thêta, l’EEG est dominé par des ondes amples et régulières dans une gamme de fréquence allant de 6 à 9 Hz (caractéristique du rythme thêta). L’activité de population des neurones pyramidaux et des cellules en grain est alors éparse : la majorité de ces neurones est silencieuse alors que la fraction restante montre des pics à hautes fréquence (jusqu’à 50 Hz). Une cellule reste active entre une demi-seconde et quelques secondes. Ainsi lorsque le rat est en activité, différentes populations de cellules s’activent puis sont remplacées par d’autres au gré du temps, la proportion globale de cellules actives restant plus ou moins constante. La position de l’animal influence beaucoup l’activité de ces neurones (cf. cellule de lieu), même si d’autres aspects du comportement entrent en compte dans l’activité électrique.
Le mode à activité irrégulière de large amplitude apparaît durant le sommeil profond (dit « à ondes lentes ») et également durant des états d’éveil inactifs, comme le repos ou lorsque l’animal mange[8]. Durant ce mode, l’EEG présente de grandes vagues d’activité non rythmées dites à « fronts raides » (« sharp waves » en anglais) qui durent entre 200 et 300 ms. Ces ondes de large amplitude déterminent le patron d’activité des populations neuronales. Entre deux vagues, les cellules pyramidales et les cellules en grain sont très peu actives (mais pas silencieuses). Durant la vague, 5 à 10 % de la population neuronale émet des potentiels d’action durant 50 ms, le plus souvent sous forme de burst (série de potentiel d’action à haute fréquence).
Ces deux modes d’activité de l’hippocampe sont observés aussi bien chez le rat que chez le primate, même si chez ce dernier, l’observation d’un rythme thêta net reste difficile. On retrouve la même forme d’onde électromagnétique avec des changements d’activités corrélés à l’activité de l’animal, comme chez le rat[9].
Fonctions
Trois fonctions principales de l'hippocampe se sont dégagées à travers la littérature de ces dernières décennies :
- la mémoire
- la navigation spatiale
- l'inhibition du comportement
L'implication de l'hippocampe dans la mémoire est une théorie qui, bien qu'elle ait des précurseurs historiques, dérive principalement des observations réalisées par Scoville et Brenda Milner[10] sur un patient, Henry Gustav Molaison, connu jusqu'à sa mort en 2008 sous ses initiales, H.M.. À la suite d'une chirurgie visant à diminuer ses crises épileptiques, H. M. eut l'hippocampe entièrement retiré. Une des conséquences inattendues de cette chirurgie fut une sévère amnésie antérograde, ainsi qu'une amnésie rétrograde partielle : H. M. était incapable de former de nouveaux souvenirs épisodiques et avait perdu la mémoire des événements précédant sa chirurgie, bien qu'il puisse toujours se souvenir des événements plus anciens, comme ses souvenirs d'enfance. Ce cas produisit un intérêt tel, que H.M. devint le patient le plus étudié de l'Histoire de la médecine[11]. Par la suite, plusieurs autres cas de patients présentant le même type de lésion à l'hippocampe (causée par accident ou maladie) et souffrant d'amnésie, furent relatés et étudiés. De nombreuses expérimentations ont par ailleurs été menées pour étudier la physiologie des changements activité-dépendants des connexions synaptiques dans l'hippocampe. L'ensemble de ces travaux ont ainsi montré un rôle central de l'hippocampe dans la mémoire[12]. Néanmoins, les mécanismes exacts dans le processus de mémorisation restent encore très débattus[13],[14].
La deuxième théorie de la fonction de l'hippocampe lui suppose un rôle majeur dans le codage des informations spatiales. Cette théorie est notamment défendue par O'Keefe et Nadel, qui se sont inspirés des théories de E.C. Tolman sur les « cartes cognitives » de l'humain et de l'animal. Ils découvrirent notamment, en 1971, certains types de neurones qui semblaient s'activer spécifiquement lorsque le rat se déplaçait à un endroit précis dans son environnement[15]. Ces cellules ont été baptisées cellules de lieu. Leur étude intensive ces trente dernières années suggère que l'hippocampe est également un acteur majeur dans le repérage et le codage de l'information spatiale (mémoire spatiale), même si, là encore, son rôle exact reste débattu[16]. Récemment, d'autres neurones ont été caractérisés dans le cortex entorhinal, qui déchargent chacun pour une position précise sur une grille virtuelle hexagonale[17]. Les rôles respectifs de ces cellules de grille et des cellules de lieu est encore incompris.
L'inhibition du comportement est une hypothèse qui fut très populaire durant les années 1960. Cette théorie était alors justifiée par deux observations principales. D'une part, les animaux présentant des dommages à l'hippocampe avaient tendance à être hyperactifs. D'autre part, ces animaux avaient également des difficultés à retenir les tâches qui impliquaient des réponses inhibitrices, notamment lorsque l'animal devait rester silencieux (comme dans un test d'évitement passif).
Jeffrey Gray développa cette ligne de pensée en une théorie liant hippocampe et mécanismes d'anxiété[18]. Néanmoins, la théorie de l'inhibition reste actuellement la plus controversée des trois[19].
Historiquement, une des premières théories sur la fonction de l'hippocampe fut de l'associer à l'olfaction. Pourtant, plusieurs expériences anatomiques du début des années 1970 ne mettaient pas en évidence de relations directes entre le bulbe olfactif et l'hippocampe[20]. Des travaux plus tardifs confirmèrent néanmoins que le bulbe olfactif projetait bien dans la partie ventrale du cortex entorhinal latéral et que la zone CA1 de l'hippocampe ventral envoyait en retour des axones vers le bulbe olfactif[21], le noyau olfactif antérieur et vers le cortex olfactif primaire. Les réponses de l'hippocampe au système olfactif continuent d'être investiguées, notamment pour leur implication dans la mémoire des odeurs ; néanmoins l'olfaction n'est pas reconnue pour être la fonction principale de l'hippocampe[22],[23].
Rôle dans la mémoire
Les psychologues et les neuroscientifiques sont généralement d'accord sur le rôle important de l'hippocampe dans la formation des nouveaux souvenirs des événements vécus (mémoire épisodique ou autobiographique)[14],[24]. Il serait notamment responsable de la détection de la nouveauté d'un événement, d'un lieu, ou d'un stimulus[25]. Certains chercheurs comprennent l'hippocampe comme un élément d'un système de mémoire plus large, établi dans le lobe temporal médian, qui serait responsable de la mémoire déclarative (la mémoire qui peut être verbalisée, par opposition à la mémoire des mouvements (ex. : faire du vélo), et qui comprend la mémoire des faits (ex. : « Napoléon est mort en 1821 »), en plus de la mémoire épisodique (ex. : « je me suis cassé une dent en faisant du vélo à 4 ans »))[13].
En raison de la présence d'un hippocampe dans chacun des deux hémisphères cérébraux, un dommage unilatéral sur un seul des hippocampes n'entraine pas de problèmes important de mémoire[26]. À l'inverse, de sérieux dommages aux deux hippocampes entrainent de profondes difficultés à former de nouveaux souvenirs (amnésie antérograde) et détériorent également une partie des souvenirs déjà présents avant la lésion (amnésie rétrograde). Bien que cette amnésie rétrograde couvre souvent plusieurs années avant le traumatisme, les souvenirs très anciens restent présents. Cette observation a conduit à l'hypothèse que, lors de la consolidation des souvenirs, ceux-ci sont peu à peu transférés vers une autre partie du cerveau[24].
Les lésions de l'hippocampe n'affectent pas tous les types de mémoire. Par exemple la capacité d'apprendre des mouvements complexes (comme faire du vélo) et celles des capacités cognitives (jouer d'un instrument, résoudre certains types de puzzle, etc.) restent le plus souvent intactes. Cette conservation de ces capacités suggère que celles-ci reposent sur un autre type de mémoire (la mémoire procédurale) dépendant d'une autre région cérébrale. De plus, certains patients amnésiques montrent des formes de mémorisation implicite, non consciente. Par exemple, pouvoir reconnaitre une certaine personne, qu'ils ont croisée récemment, comme familière et pourtant jurer qu'ils ne se souviennent pas l'avoir rencontrée. Certains chercheurs séparent donc le « rappel conscient », qui dépendrait de l'hippocampe, du sentiment de « familiarité », qui dépendrait d'une partie du cortex temporal médian[27].
État des connaissances actuelles
L'hippocampe est composé de plusieurs modules, chacun ayant une fonction spécifique encore mal élucidée ; chacune de ces fonctions contribue à la construction rapide (éventuellement en une seule fois) de mémoires évènementielles complexes, qualifiées de mémoire épisodique. Il doit cette fonction mémorielle particulière à certaines structures auto-associatives comme CA3, qui permettent d'établir des liens entre des informations reçues de couches corticales éloignées les unes des autres et qui convergent toutes vers la structure hippocampique par la porte d'entrée du cortex entorhinal. On lui fait jouer un rôle de répétiteur des informations rapidement apprises, pour le manteau cortical qui apprend beaucoup plus lentement, et avec lequel il a des connexions réciproques. Ces épisodes de réactivation de l'information apprise pourraient se faire au cours des phases de repos ou de sommeil (en particulier le sommeil paradoxal) pendant des phases où certaines structures hippocampiques émettent spontanément des « sharp waves » en direction du cortex. La plupart des auteurs pensent que le stockage définitif des souvenirs se fait plus au niveau du cortex que de l'hippocampe, et opposent la mémoire évènementielle ou mémoire épisodique consciente à la mémoire procédurale (des habiletés et des automatismes moteurs ou autres), majoritairement à dominance non-consciente stockés dans des structures sous corticales, tels les ganglions de la base. Cependant le dialogue entre les deux systèmes et le passage d'une forme de mémoire à l'autre est permanent.
Cependant, selon une étude faite en 2006 par une équipe de l'INSERM dirigée par Francis Eustache et Pascale Piolono, l'hippocampe serait en fait le siège de la mémoire épisodique à long terme, c’est-à-dire l'ensemble des évènements de l'existence dont le souvenir a été conservé. L'hippocampe ne serait donc pas une simple machine à fabriquer des souvenirs stockés ensuite ailleurs, mais bien le siège de ces souvenirs et ceci tout au long de la vie. Cette étude a été faite sur des femmes volontaires, dont le mari avait fourni, pour chacune d'entre elles, cinq souvenirs précis, étalés de l'enfance jusqu'à une période récente. Lorsque les chercheurs ont réactivé ces souvenirs par des indices, ils ont observé que l'hippocampe de ces femmes s'active et d'autant plus fortement que ces souvenirs étaient précis (détails, couleurs, odeurs). Néanmoins, l'activation de l'hippocampe au cours de cette tâche traduit très probablement que cette structure cérébrale joue un rôle dans les processus de rappel, c'est-à-dire de récupération de la trace mémorielle. Cela ne signifie pas que l'hippocampe est le siège de la mémoire à long terme. Il est d'ailleurs connu depuis quelques années qu'avec le temps, cette trace quitte l'hippocampe pour siéger dans le néocortex[28].
Développement
L'hippocampe apparait au niveau du diencéphale médian durant le développement embryonnaire. Sa spécification est initiée par des facteurs de différenciation qui diffusent depuis une structure appelée ourlet cortical (cortical hem en anglais)[29]. La présence de l'ourlet cortical est nécessaire et suffisante pour induire la formation de l'hippocampe. Ainsi des expériences de greffe ectopique d'ourlet cortical à un autre niveau du cortex provoquent l'apparition de tissus hippocampiques autour du site de greffe. L'ourlet cortical, qui régule également l'apparition des plexus choroïdes, est donc le centre de signalisation et d'organisation du diencéphale en développement. Cette initiation du développement de l'hippocampe a lieu au stade embryonnaire E8,5 chez la souris. Une fois cette spécification réalisée, le développement de l'hippocampe devient autonome, il produit ses propres facteurs de différenciation pour poursuivre l'organisation des champs ammoniens, CA1, CA2 et CA3.
Il a été montré que la signalisation par les Wnt était impliquée dans la différentiation des cellules du diencéphale en précurseur de neurones hippocampiques. De même d'autres facteurs diffusibles sont responsables de la spécification de chacune de ses sous-populations (celles du Gyrus dentelé, CA1, CA3 et du subiculum).
Les neurones de l'hippocampe se différencient et se mettent en place par un mécanisme commun à l'ensemble du cortex. Les neurones pyramidaux se différencient à partir de la glie radiaire et migrent radialement vers leur couches respectives. La neurogenèse des neurones pyramidaux atteint son paroxysme au stade E14,5 pour CA3 et E15,5 pour CA1. Certains défauts dans la migration embryonnaire des neurones pyramidaux pourraient être à l'origine d'une hyperexcitabilité, entrainant chez l'homme une lissencéphalie. Les interneurones migrent tangentiellement depuis les zones ventrales du cortex d'où ils se différencient vers E11-E14. Ils arrivent ensuite dans l'hippocampe à partir de E15 et s'intègrent vers E16,5 en migrant radialement.
Les différentes connexions que ces neurones établissent par la suite ne deviennent matures qu'après la naissance, une fois établies dans un réseau fonctionnel et après un intense élagage des connexions non utilisées.
Évolution
L’hippocampe a une apparence similaire à travers l’ensemble des mammifères, des monotrèmes aux primates[30]. La proportion de l’hippocampe par rapport à la taille de l’individu s’accroit au cours de l’évolution des mammifères, étant 2 fois plus importante chez les primates que chez les echidnés. Cette évolution reste néanmoins bien moins importante que l’augmentation parallèle du néocortex. En conséquence, l’hippocampe prend une plus grande part du manteau cortical chez le rongeur que chez le primate. Chez l’être humain adulte, le volume de l’hippocampe de chaque côté du cerveau est d’environ 3-3,5 cm3. En comparaison, le néocortex fait 320-420 cm3[31].
Il y a également une certaine corrélation entre la taille de l’hippocampe et la mémoire spatiale. Lorsque l’on compare différentes espèces, celles qui ont les plus grandes capacités de mémorisation spatiale ont tendance à posséder un plus grand volume hippocampique[32]. Cette relation s’étend même à la différence entre les sexes : chez les espèces où il existe une importante différence dans les capacités de mémorisation spatiale entre le mâle et la femelle, on retrouve cette différence dans le volume qu’occupe l’hippocampe[33].
En dehors des mammifères, les autres espèces ne possèdent pas strictement d’hippocampe mais possèdent parfois une structure considérée comme homologue. En effet, chez les autres vertébrés, le cortex est beaucoup moins développé et par extension l’hippocampe, qui occupe généralement la face médiane du cortex des mammifères, n’est pas présent. Néanmoins, la structure dont dérive le cortex, appelée pallium, est présente chez tous les vertébrés, jusqu'aux plus primitifs, comme les lamproies ou les myxines[34]. Le pallium est divisé en trois zones : médiale, latérale et dorsale. Le pallium médian forme une structure correspondant à un hippocampe primitif. Elle ne ressemble pas visuellement à l’hippocampe, elle n’a pas la forme caractéristique en S et n’est pas entourée du gyrus dentelé ; mais l’homologie de cette structure est fortement suggérée par ses ressemblances biochimiques et fonctionnelles avec l’hippocampe. Plusieurs études ont depuis montré l’implication de cette structure dans la cognition spatiale chez les oiseaux, les reptiles et les poissons[35].
Ainsi, la correspondance est suffisamment établie chez les oiseaux pour que l'on puisse parler pour le pallium médian d'« hippocampe aviaire »[36]. De nombreuses espèces d’oiseaux possèdent de très grandes capacités de mémorisation spatiale, notamment chez les espèces qui se créent et cachent des réserves de nourriture. Il a été montré chez ces dernières, que leur hippocampe était beaucoup plus développé que chez les autres oiseaux et qu’une lésion à celui-ci entrainait des défauts de mémorisation spatiale[37].
Chez le poisson, la localisation de l’équivalent de l’hippocampe est plus compliquée. En effet, chez les poissons téléostéens (qui constituent la majorité des espèces actuelles) le cerveau antérieur est déformé par rapport aux autres types de vertébrés : les neuroanatomistes considèrent que leur cerveau est inversé, de sorte que des structures habituellement interne, chez les vertébrés, se trouvent sur la face externe et inversement (comme une chaussette retournée à l’envers)[38]. En conséquence, la structure qui devrait correspondre à la zone de l’hippocampe se trouve dans le pallium latéral et non plus médian, comme pour les autres espèces. De nombreux types de poissons (particulièrement le poisson rouge) ont montré expérimentalement des capacités mnésiques spatiales importantes, et même la capacité de former des cartes cognitives de leur habitat[32]. En cohérence, une lésion au pallium latéral entraine des défauts dans ces capacités spatiales[39].
Le rôle de la région hippocampique dans la navigation et la mémorisation spatiale apparait ainsi très tôt dans l’évolution des vertébrés, précédent des séparations datant de centaines de millions d’années[40]. On ne sait pas encore si le pallium médian joue un rôle similaire chez des vertébrés plus primitifs, comme les requins ou les raies, ou même les lamproies et les myxines. Certains types d’insecte et de mollusque, comme la pieuvre, ont également des capacités de navigation et de mémorisations spatiales impressionnantes mais il ne semble pas qu’elles reposent sur les mêmes mécanismes que le système des mammifères. Il n’y a donc pas, a priori, d’évidence supportant une origine évolutive commune, même si certaines parties de leur cerveau partagent une fonction semblable[41].
Neurogenèse adulte
Datant des débuts des Neurosciences, le dogme stipulant que la neurogenèse n'avait lieu que durant le développement embryonnaire et s'arrêtait avant la puberté a repoussé la découverte de la neurogenèse chez l'adulte. C'est en 1962 que cette croyance a été finalement contredite par l'observation de la production de nouveaux neurones fonctionnels dans le cerveau des rongeurs adultes[42], puis des primates et enfin de l'homme adulte[43].
Pour démontrer la production de nouveaux neurones, les chercheurs ont utilisé un marqueur appelé BrdU. Le BrdU a la faculté de s'incorporer dans l'ADN des cellules en division et donc dans les seuls neurones du système nerveux capable de se multiplier, les cellules souches neuronales adultes. Cette technique a permis de montrer vers la fin des années 1980 que l'hippocampe était le siège d'une neurogenèse adulte. C'est, plus précisément, dans la zone sous-granulaire du gyrus denté que se situent les progéniteurs neuronaux capables de proliférer et de se différencier en neuroblastes (progéniteurs de neurones). Ces neuroblastes migrent ensuite dans la couche granulaire et se différencient en neurones granulaires, étendant leurs dendrites et leurs axones dans le réseau de neurones préexistant. Nombre d'entre eux ne persistent pas jusqu'à maturation et sont éliminés pour conserver un nombre de neurones à peu près constant au cours du temps.
De nombreuses études se sont penchées sur les facteurs capables de modifier ou d'altérer cette neurogenèse adulte. Ainsi, certains facteurs de croissance, le vieillissement, le manque de sommeil, le stress et l'exposition aux glucocorticoïdes tendent à diminuer la neurogenèse du gyrus dentelé. À l'inverse, les œstrogènes, les traitements antidépresseurs, l'activité physique, la présence d'un environnement enrichi et l'apprentissage dépendant de l'hippocampe ont montré des effets positifs sur la quantité de nouveaux neurones.
Il semble y avoir un lien entre l'apprentissage et la consolidation des souvenirs et la neurogenèse de l'hippocampe. Pour la dépression, une diminution de la neurogenèse ne déclenche pas en tant que telle une dépression, mais une neurogénèse importante est indispensable à l'action de la plupart des antidépresseurs[44]. En effet, chez des souris irradiées dans l'hippocampe qui ne peuvent plus faire de neurogénèse, les antidépresseurs n'ont plus d'effets sur des tests comportementaux liés à la dépression.
Pathologie
De nombreuses maladies sont liées à des atteintes de l'hippocampe, que cette atteinte en soit la cause ou la conséquence. La plus célèbre d'entre elles est certainement la maladie d'Alzheimer, qui ne sera pas décrite ci-dessous, qui débute par une dégénération de l'hippocampe[45]. Quelle que soit la pathologie concernée, une atteinte de l'hippocampe est toujours suggérée lorsque la mémoire ou la navigation spatiale est atteinte - et inversement toute modification de l'hippocampe est automatiquement étudiée par des tests et des expérimentations comportementales des différentes formes de mémoire et de navigation. Les troubles de l'humeur des patients atteints de la maladie de Huntington, tout particulièrement l'anxiété, sont sans doute liés à des défauts de neurogenèse adulte dans l'hippocampe[46].
Lien avec le vieillissement
Dans de nombreuses pathologies qui apparaissent avec l’âge, comme la maladie d’Alzheimer, on retrouve une altération des fonctions cognitives et, notamment, celles supposées être contrôlées par l’hippocampe (mémoires, navigation spatiale, etc.). Mais le vieillissement normal, lui-même, a un effet délétère progressif sur certains types de mémoire, incluant la mémoire épisodique et la mémoire de travail. Cette diminution des capacités mnésiques avec l’âge serait la conséquence d’une détérioration progressive et non pathologique de l’hippocampe[47].
Les premières études ont ainsi montré une perte substantielle des neurones de l’hippocampe chez les personnes âgées, même si de récentes études, plus précises, ont relativisé cette perte[47]. De la même manière, certaines études IRM ont montré une réduction de l’hippocampe avec l’âge, résultats pourtant non confirmés par d'autres études. Il est certain qu’il existe une corrélation entre la taille de l’hippocampe et les performances mnésiques – ce qui implique que parmi les personnes âgées, celles dont l’hippocampe a diminué ont de moins bonnes performances dans certaines tâches de mémorisation[47]. Certains facteurs sont susceptibles d’expliquer la différence de taille de l’hippocampe qu’on observe chez les personnes âgées, comme la pratique d’une activité sportive régulière ou d’activités cérébrales (ex: mots croisés) impliquant l’hippocampe[48].
Un des critères de différence entre une personne âgée « normale » mais qui voit ses capacités mnésiques réduites, et une personne atteinte de la maladie d’Alzheimer tient dans la capacité à encoder l’information : chez les sujets non-atteints, l’information est présente mais peut être difficile à récupérer sans l’aide d’indice, alors que chez les sujets atteints, l’information n’a pas été encodée et ne peut donc être retrouvée, même en présence d’indices.
Chez le rat, où l’étude de la physiologie cellulaire est possible, le vieillissement ne semble pas entrainer de perte de neurone mais altère plutôt les connexions synaptiques de différentes façons[49]. Le nombre de synapses fonctionnelles est ainsi diminué dans le gyrus dentelé et la région CA1, et la réponse induite par les récepteurs NMDA est diminuée. Ces altérations pourraient être la cause des problèmes d’induction et de maintien de la potentialisation à long terme, une des formes de plasticité synaptique impliquée dans la mémorisation. Il y a de plus une diminution, due à l’âge, de l’expression de certains des gènes associés aux mécanismes de la plasticité synaptique[50]. Enfin, les rats âgés présentent des différences de stabilité des champs de lieu assuré par les cellules de lieu. Alors que les jeunes rats sont capables de changer de carte cognitive lorsqu’ils changent d’environnement et de retrouver la même carte lorsqu’ils sont replacés dans ce même environnement, les rats âgés sont incapables d’effectuer ces modifications de carte, ni de pouvoir s’en souvenir.
Des recherches récentes dans le domaine de l'épidémiologie cognitive (parfois appelée santé cognitive) ont montré que le thréonate de magnésium, composé chimique breveté[51], induit dans l'hippocampe une augmentation de la densité synaptique et de la plasticité des synapses qui contribuerait à retarder les effets du vieillissement sur la mémoire et à limiter l'évolution de la maladie d'Alzheimer[51],[52],[53].
Stress chronique
L’hippocampe contient de hauts niveaux de récepteurs aux glucocorticoïdes, ce qui le rend plus vulnérable au stress, sur le long terme, que d’autres structures du cerveau[54]. Les stéroïdes liés au stress affectent l’hippocampe d’au moins trois façons connues :
- Tout d’abord, ils réduisent l’excitabilité de certains neurones hippocampaux.
- Ensuite, ils inhibent la neurogenèse qui a lieu dans le gyrus dentelé.
- Troisièmement, ils causent une atrophie des dendrites des cellules pyramidales de la région CA3.
Plusieurs études montrent que les personnes qui ont subi de longues quantités de stress traumatique présentent une atrophie renforcée de l’hippocampe par rapport à d’autres structures cérébrales[55]. On retrouve également cet effet après un stress post-traumatique[56] et dans certaines pathologies inductrices de stress, comme la schizophrénie[57] et les dépressions sévères[58]. Une étude récente a montré que la dépression entraine une atrophie qui peut être stoppée par la prise d’antidépresseurs, même si ceux-ci n’ont pas d’effets sur les autres symptômes[59]. Une atrophie de l’hippocampe est également souvent associée avec le syndrome de Cushing, une maladie qui provoque de forts taux de cortisol dans le sang.
Les effets du stress semblent au moins réversibles si celui-ci est discontinu. À l'inverse, des études menées chez le rat ont montré qu’un stress postnatal pouvait affecter le fonctionnement de l’hippocampe de manière irréversible chez l'adulte[60].
Épilepsie
L’hippocampe est souvent au centre des crises épileptiques : une sclérose de l’hippocampe est habituellement observée lors des épilepsies du lobe temporal. Il n’est pas encore établi si ces lésions de l’hippocampe sont la cause ou la conséquence des crises à répétition de l’épilepsie[61]. Chez l’animal, lorsque des crises sont induites artificiellement et à répétition, une lésion à l’hippocampe est également observée : ce qui peut être dû au fait que l’hippocampe est une des structures les plus excitables électriquement du cerveau. Il pourrait également y avoir un lien avec des altérations de la neurogenèse adulte de l’hippocampe[62].
Schizophrénie
Les causes de la schizophrénie sont loin d’être connues mais plusieurs anormalités de structures cérébrales ont été rapportées, la plupart concernent le cortex cérébral mais plusieurs effets sur l’hippocampe ont tout de même été décrits. Certains patients schizophrènes présentent un hippocampe de taille réduite[63]. Cette diminution serait probablement due à un défaut de développement plutôt qu’à une lésion du tissu et apparaît même chez des patients n’ayant jamais reçu de médication. Plusieurs éléments tendent à montrer un changement de l’organisation et de la connectivité des synapses[63].
Des études sur animaux ont suggéré qu’un dysfonctionnement de l’hippocampe pouvait causer une altération de la production de dopamine dans les ganglions de la base, causant indirectement des troubles d’intégration de l’information dans le cortex préfrontal[64]. D’autres études ont également suggéré que les dysfonctionnements de l’hippocampe pouvaient être la cause des défauts dans la mémoire à long terme qui sont fréquemment observés chez les patients atteints de schizophrénie[65].
Autres pathologies
Une des causes possible de l’ictus amnésique - une perte soudaine et temporaire de la mémoire à court terme – serait une congestion de veines du cerveau[66], provoquant une ischémie dans plusieurs structures, dont l’hippocampe[67].
Les infections à répétition par picornaviridae (rhumes, certaines gastro-entérites). Selon le professeur Charles Howe de la Mayo Clinic à Rochester qui a mené ses recherches sur des souris, les picornavirus auraient une action destructrice des cellules de l'hippocampe, à tel point que « des infections à répétition par picornavirus pourraient entamer le capital cognitif d'un individu. »
Le manque de sommeil aurait également des effets néfastes sur l'hippocampe[réf. nécessaire].
Effet de l'alcoolisme : une étude américaine du Colorado Health Sciences Center a cherché à savoir si la consommation excessive d'alcool a un effet sur l'hippocampe. Utilisant l'imagerie à résonance magnétique (IRM), ils ont constaté que l'hippocampe des alcooliques sévères est moins volumineux et « cette découverte pourrait expliquer le déficit cognitif et les problèmes de mémoire souvent observés chez ces derniers ». La suite de leur recherche porte sur le fait de savoir comment l'hippocampe réagit à l'arrêt de l'imprégnation alcoolique.
Des universitaires américains[68] ont découvert que le cannabis perturbe les processus de mémorisation du cerveau en désorganisant le fonctionnement électrique de l'hippocampe, structure clé du cerveau pour l'activation de la mémoire. Le cannabis aux doses usuellement présentes chez ses consommateurs supprime les oscillations électriques, essentielles dans le processus d'apprentissage et de mémorisation. Les processus cognitifs sont désorganisés. Selon le professeur Jean Costentin, la principale substance active dans le cannabis, le THC tétrahydrocannabinol, bloque aussi la libération d'un neurotransmetteur important dans l'hippocampe, l'acétylcholine, affectant le fonctionnement électrophysiologique du cerveau.
Bibliographie
Livres
- Jean-Paul Banquet, Ph. Gaussier, M. Quoy, A. Revel, Y. Burnod, A Hierarchy of Associations in Hippocampo-Cortical Systems: Cognitive Maps and Navigation Strategies, Neural Computation, 17, 6, June 2005.
- Professeur Jean Costentin : Halte au cannabis !, éd. Odile Jacob.
- Randall C. O’Reilly and Yuko Munakata, Computational Explorations in Cognitive Neuroscience : Understanding the Mind by Simulating the Brain, The MIT Press, 2000, (ISBN 0-262-65054-1)
- Larry R. Squire, Eric R. Kandel, La mémoire - De l'esprit aux molécules. Ed Flammarion, (ISBN 2-08-080139-2)
Articles
- Crusio, W. E., et H. Schwegler (2005). « Learning spatial orientation tasks in the radial-maze and structural variation in the hippocampus in inbred mice. » Behavioral and Brain Functions 1 (3)
- Florian, C., J. Foltz, et al. (2006). « Post-training intrahippocampal injection of synthetic poly-{alpha}-2,8-sialic acid-neural cell adhesion molecule mimetic peptide improves spatial long-term performance in mice. » Learn Mem.
- Florian, C. et P. Roullet (2004). « Hippocampal CA3-region is crucial for acquisition and memory consolidation in Morris water maze task in mice. » Behavioural Brain Research 154(2): 365-374.
Notes et références
- Duvernoy, HM (2005) Introduction. The Human Hippocampus (3e éd.). Berlin: Springer-Verlag. p. 1. (ISBN 3-540-23191-9).
- (en) Gross, Charles G. (1993) « Hippocampus Minor and Man's Place in Nature: A Case Study in the Social Construction of Neuroanatomy ». Hippocampus 3 (4): 403–416. DOI:10.1002/hipo.450030403
- (en) Wechsler RT, Morss, AM, Wustoff, CJ, & Caughey, AB (2004) Blueprints notes & cases: Neuroscience. Oxford: Blackwell Publishing. p. 37. (ISBN 1-4051-0349-3).
- Amaral, D; Lavenex P (2006). « Ch 3. Hippocampal Neuroanatomy ». In Andersen P, Morris R, Amaral D, Bliss T, O'Keefe J. The Hippocampus Book. Oxford University Press. (ISBN 978-0-19-510027-3).
- Kötter R, Stephan KE (1997). « Useless or helpful? The « limbic system » concept ». Rev Neurosci 8 (2): 139–45. doi:10.1515/REVNEURO.1997.8.2.139. .
- Moser, EI; Moser M-B (1998). « Functional differentiation in the hippocampus ». Hippocampus 8 (6): 608–19. .
- Buzsáki, G (2006). Rhythms of the Brain. Oxford University Press. (ISBN 0-19-530106-4).
- Buzsáki G, Chen LS, Gage FH (1990). « Spatial organization of physiological activity in the hippocampal region: relevance to memory formation ». Prog Brain Res 83: 257–68. doi:10.1016/S0079-6123(08)61255-8. .
- Skaggs WE, McNaughton BL, Permenter M, et al. (2007). « EEG sharp waves and sparse ensemble unit activity in the macaque hippocampus ». J Neurophysiol 98 (2): 898–910. doi:10.1152/jn.00401.2007. .
- Scoville, WB; Milner B (1957). « Loss of Recent Memory After Bilateral Hippocampal Lesions ». J. Neurol. Neurosurg. Psych. 20 (1): 11–21. doi:10.1136/jnnp.20.1.11. PMC 497229. .
- Squire LR (2009). « The legacy of patient H.M. for neuroscience ». Neuron 61 (1): 6–9. doi:10.1016/j.neuron.2008.12.023. PMC 2649674. .
- Draganski et al. « Temporal and Spatial Dynamics of Brain Structure Changes during Extensive Learning », The Journal of Neuroscience, June 7, 2006, 26(23):6314-6317
- Squire, LR (1992). « Memory and the hippocampus: a synthesis from findings with rats, monkeys, and humans ». Psych. Rev. 99: 195–231. doi:10.1037/0033-295X.99.2.195, .
- Eichenbaum, H; Cohen NJ (1993). Memory, Amnesia, and the Hippocampal System. MIT Press.
- O'Keefe J, Dostrovsky J (1971). « The hippocampus as a spatial map. Preliminary evidence from unit activity in the freely-moving rat ». Brain Res 34 (1): 171–75. doi:10.1016/0006-8993(71)90358-1. .
- Moser, EI; Kropf E, Moser M-B (2008). « Place Cells, Grid Cells, and the Brain's Spatial Representation System ». Ann. Rev. Neurosci. 31: 69. doi:10.1146/annurev.neuro.31.061307.090723. .
- Hafting, T.; Fyhn, M.; Molden, S.; Moser, M. -B.; Moser, E. I. (2005). « Microstructure of a spatial map in the entorhinal cortex ». Nature 436 (7052): 801. doi:10.1038/nature03721
- Gray, JA; McNaughton N (2000). The Neuropsychology of Anxiety: An Enquiry into the Functions of the Septo-Hippocampal System. Oxford University Press.
- Best PJ, White AM (1999). « Placing hippocampal single-unit studies in a historical context ». Hippocampus 9 (4): 346–51. .
- Finger, S (2001). Origins of Neuroscience: A History of Explorations Into Brain Function. Oxford University Press US. (ISBN 978-0-19-514694-3), p. 183.
- DeOlmos J, Hardy H, Heimer L (1978). « The afferent connections of the main and the accessory olfactory bulb formations in the rat: an experimental HRP-study ». Journal of Comparative Neurology 181 (2): 213–244. doi:10.1002/cne.901810202. .
- Eichenbaum, H; Otto TA, Wible CG, Piper JM (1991). « Ch 7. Building a model of the hippocampus in olfaction and memory ». In Davis JL, Eichenbaum H,. Olfaction. MIT Press. (ISBN 978-0-262-04124-9).
- Vanderwolf CH (2001). "The hippocampus as an olfacto-motor mechanism: were the classical anatomists right after all?". Behav Brain Res 127 (1-2): 25–47. doi:10.1016/S0166-4328(01)00354-0. .
- Squire, LR; Schacter DL (2002). The Neuropsychology of Memory. Guilford Press.
- anElzakker, MB; Fevurly RD, Breindel T, Spencer RL (2008). « Environmental novelty is associated with a selective increase in Fos expression in the output elements of the hippocampal formation and the perirhinal cortex ». Learning & Memory 15 (12) : 899–908. doi:10.1101/lm.1196508. PMC 2632843. .
- Di Gennaro G, Grammaldo LG, Quarato PP, Esposito V, Mascia A, Sparano A, Meldolesi GN, Picardi A. Severe amnesia following bilateral medial temporal lobe damage occurring on two distinct occasions. Neurol Sci. 2006 Jun;27(2):129–33.
- Diana RA, Yonelinas AP, Ranganath C. Imaging recollection and familiarity in the medial temporal lobe: a three-component model. (2007) Trends Cogn Sci 11 (9): 379–86. doi:10.1016/j.tics.2007.08.001. .
- Bontempi B, Laurent-Demir C, Destrade C, Jaffard R. (1999). Time-dependent reorganization of brain circuitry underlying long-term memory storage. Nature 1999 Aug 12;400(6745):671-5.
- Subramanian L, Tole S.Mechanisms underlying the specification, positional regulation, and function of the cortical hem. Cereb Cortex. 2009
- West, M.J., Stereological studies of the hippocampus: a comparison of the hippocampal subdivisions of diverse species including hedgehogs, laboratory rodents, wild mice and men. Prog. Brain Res. vol. 83, p. 13–36 (1990) doi: 10.1016/S0079-6123(08)61238-8
- Suzuki M, Hagino H, Nohara S, et al. (2005). « Male-specific volume expansion of the human hippocampus during adolescence ». Cereb Cortex 15 (2): 187–93. doi:10.1093/cercor/bhh121. .
- Jacobs, LF (2003). « The Evolution of the Cognitive Map ». Brain Behav. Evol. 62 (2): 128–39. doi:10.1159/000072443.
- Jacobs, LF; Gaulin SJ, Sherry DF, Hoffman GE (1990). « Evolution of spatial cognition: sex-specific patterns of spatial behavior predict hippocampal size ». PNAS 87 (16): 6349–52. doi:10.1073/pnas.87.16.6349. PMC 54531.
- Aboitiz, F; Morales D, Montiel J (2003). « The evolutionary origin of the mammalian isocortex: Towards an integrated developmental and functional approach ». Behav. Brain Sciences 26 (5): 535–52. doi:10.1017/S0140525X03000128.
- Rodríguez, F; Lópeza JC, Vargasa JP, Broglioa C, Gómeza Y, Salas C (2002). « Spatial memory and hippocampal pallium through vertebrate evolution: insights from reptiles and teleost fish ». Brain Res. Bull. 57 (3-4): 499–503. doi:10.1016/S0361-9230(01)00682-7.
- Colombo, M; Broadbent N (2000). « Is the avian hippocampus a functional homologue of the mammalian hippocampus? ». Neurosci. Biobehav. Rev. 24 (4): 465–84. doi:10.1016/S0149-7634(00)00016-6.
- Shettleworth, SJ (2003). « Memory and Hippocampal Specialization in Food-Storing Birds: Challenges for Research on Comparative Cognition ». Brain Behav. Evol. 62 (2): 108–16. doi:10.1159/000072441. .
- Nieuwenhuys, R (1982). « An Overview of the Organization of the Brain of Actinopterygian Fishes ». Am. Zool. 22: 287–310. doi:10.1093/icb/22.2.287
- Portavella, M; Vargas JP, Torres B, Salas C (2002). « The effects of telencephalic pallial lesions on spatial, temporal, and emotional learning in goldfish ». Brain Res. Bull. 57 (3-4): 397–99. doi:10.1016/S0361-9230(01)00699-2.
- Broglio, C; Gómez A, Durán E, Ocaña FM, Jiménez-Moya F, Rodríguez F, Salas C (2002). "Hallmarks of a common forebrain vertebrate plan: Specialized pallial areas for spatial, temporal and emotional memory in actinopterygian fish". Brain Res. Bull. 57 (4-6): 397–99.
- Mizunami M, Weibrecht JM, Strausfeld NJ (1998). « Mushroom bodies of the cockroach: their participation in place memory ». J Comp Neurol 402 (4): 520–37. doi:10.1002
- (en) Shahin Owji et Mohammadali M. Shoja, « The History of Discovery of Adult Neurogenesis », Clinical Anatomy, vol. 33, no 1, , p. 41–55 (ISSN 0897-3806 et 1098-2353, DOI 10.1002/ca.23447, lire en ligne, consulté le )
- Eriksson et al., 1998 Nature Neurosciences
- Samuels B. and Hen R. Neurogenesis and affective disorders. Eur J Neuroscience 33, 1152-1159 (2011) doi: 10.1111/j.1460-9568.2011.07614.x
- Hampel H, Bürger K, Teipel SJ, Bokde AL, Zetterberg H, Blennow K (2008). "Core candidate neurochemical and imaging biomarkers of Alzheimer's disease". Alzheimers Dement 4 (1): 38–48. doi:10.1016/j.jalz.2007.08.006. .
- Pla P et al. Mood disorders in Huntington's disease (2014). Frontiers in Behavioral Neuroscience 8, e135, doi: 10.3389/fnbeh.2014.00135
- Prull MW, Gabrieli JDE, Bunge SA (2000). "Ch 2. Age-related changes in memory: A cognitive neuroscience perspective". In Craik FIM, Salthouse TA. The handbook of aging and cognition. Erlbaum. (ISBN 978-0-8058-2966-2).
- Erickson KI et al (2011). Exercise training increases size of hippocampus and improves memory. Proc. Nat. Acad. Sci. 108 (7): 3017–3022. doi:10.1073/pnas.1015950108. .
- Rosenzweig ES, Barnes CA (2003). Impact of aging on hippocampal function: plasticity, network dynamics, and cognition. Prog Neurobiol 69 (3): 143–79. doi:10.1016/S0301-0082(02)00126-0. .
- Burke SN, Barnes CA (2006). "Neural plasticity in the ageing brain". Nat Rev Neurosci 7 (1): 30–40. doi:10.1038/nrn1809. .
- Breveté par Magceutics Inc. sous le nom Magtein
- (en) Wei Li, Jia Yu, Yong Liu, Xiaojie Huang, Nashat Abumaria, Ying Zhu, Xian Huang, Wenxiang Xiong, Chi Ren, Xian-Guo Liu, Dehua Chui et Guosong Liu (Chercheurs de l'université Tsinghua (Pékin), de l'université de Pékin ou de l'université Sun-Yat-sen (Canton)), « Elevation of brain magnesium prevents synaptic loss and reverses cognitive deficits in Alzheimer's disease mouse model. », Molecular Brain (en), Londres, BioMed Central, vol. 7, no 65, , p. 1–20 (ISSN 1756-6606, OCLC 233191053, PMID 25213836, PMCID 4172865, DOI 10.1186/s13041-014-0065-y, lire en ligne, consulté le ).
- (en) Guosong Liu, Jason G. Weinger, Zhong-Lin Lu, Feng Xue et Safaa Sadeghpour (Chercheurs de l'université d'État de l'Ohio (Columbus, Ohio), de l'université de Californie du Sud (Los Angeles), de l'université Tsinghua (Pékin), ou de l'entreprise Neurocentria, Inc. (Fremont, Californie)), « Efficacy and Safety of MMFS-01, a Synapse Density Enhancer, for Treating Cognitive Impairment in Older Adults : A Randomized, Double-Blind, Placebo-Controlled Trial », Journal of Alzheimer's Disease (en)., Amsterdam, (Clifton, Virginie), Pékin, IOS Press, vol. 49, no 4, , p. 971-990 (ISSN 1387-2877, e-ISSN 1875-8908, OCLC 41219744, PMID 26519439, PMCID 4927823, DOI 10.3233/JAD-150538, lire en ligne, consulté le ).
- Joels M (2008). "Functional actions of corticosteroids in the hippocampus". Eur J Pharmacol 583 (2–3): 312–321. doi:10.1016/j.ejphar.2007.11.064.
- Fu, W; Sood S, Hedges DW (2010). "Hippocampal volume deficits associated with exposure to psychological trauma and posttraumatic stress disorder in adults: A meta-analysis". Progress in Neuro-Psychopharmacology and Biological Psychiatry 34 (7): 1181–1188. doi:10.1016/j.pnpbp.2010.06.016. .
- Karl A, Schaefer M, Malta LS, Dörfel D, Rohleder N, Werner A. (2006). "A meta-analysis of structural brain abnormalities in PTSD.". Neurosci Biobehav Rev. 30 (7): 1004–31. doi:10.1016/j.neubiorev.2006.03.004.
- Wright IC, Rabe-Hesketh S, Woodruff PW, David AS, Murray RM, Bullmore ET. (2000). "Meta-analysis of regional brain volumes in schizophrenia.". Am J Psychiatry 157 (1): 16–25.
- Kempton MJ, Salvador Z, Munafò MR, Geddes JR, Simmons A, Frangou S, Williams SC. (2011). "Structural Neuroimaging Studies in Major Depressive Disorder: Meta-analysis and Comparison With Bipolar Disorder". Arch Gen Psychiatry 68 (7): 675–90. doi:10.1001/archgenpsychiatry.2011.60.
- Campbell S, Macqueen G (2004). "The role of the hippocampus in the pathophysiology of major depression". J Psychiatry Neurosci 29 (6): 417–26. PMC 524959.
- Garcia-Segura LM (2009). Hormones and Brain Plasticity. p. 170-171, Oxford University Press US. (ISBN 978-0-19-532661-1)
- Sloviter RS (2005). "The neurobiology of temporal lobe epilepsy: too much information, not enough knowledge". C R Biol 328 (2): 143–53. doi:10.1016/j.crvi.2004.10.010.
- Kuruba R, Hattiangady B, Shetty AK (2009). "Hippocampal neurogenesis and neural stem cells in temporal lobe epilepsy". Epilepsy Behav 14 Suppl 1: 65–73. doi:10.1016/j.yebeh.2008.08.020. PMC 2654382. .
- Harrison PJ (2004). "The hippocampus in schizophrenia: a review of the neuropathological evidence and its pathophysiological implications". Psychopharmacology (Berl.) 174 (1): 151–62. doi:10.1007/s00213-003-1761-y.
- Goto Y, Grace AA (2008). Limbic and cortical information processing in the nucleus accumbens. Trends Neurosci 31 (11): 552–8. doi:10.1016/j.tins.2008.08.002. .
- Boyer P, Phillips JL, Rousseau FL, Ilivitsky S (2007). "Hippocampal abnormalities and memory deficits: new evidence of a strong pathophysiological link in schizophrenia". Brain Res Rev 54 (1): 92–112. doi:10.1016/j.brainresrev.2006.12.008.
- Lewis S (1998). « Aetiology of transient global amnesia ». The Lancet 352 (9125): 397–9. doi:10.1016/S0140-6736(98)01442-1. .
- Chung C.-P., Hsu HY, Chao AC, Chang FC, Sheng WY, Hu HH (2006). « Detection of intracranial venous reflux in patients of transient global amnesia ». Neurology 66 (12): 1873–77. doi:10.1212/01.wnl.0000219620.69618.9d. .
- David Robbe et al., Nature Neurosciences, décembre 2006